
Музыка регенерации. Секретóм как основа бесклеточной терапии
14 марта 2025
Музыка регенерации. Секретóм как основа бесклеточной терапии
- 756
- 0
- 6
Сможем ли мы управлять регенерацией, если освоим молекулярное сольфеджио?
Рисунок в оригинальном разрешении.
иллюстрация Александры Мартыновой
-
Автор
-
Редакторы
-
Рецензент
-
Иллюстратор
Язык общения наших клеток — молекулярный. Сотни сигнальных молекул и частиц снуют между «работниками», отстраивающими ткань после повреждения. Отдельные команды сливаются в сигнальную симфонию, направляющую деятельность клеток. Сможем ли мы сочинять молекулярную музыку, чтобы управлять регенерацией? На этот вопрос мы и попытаемся здесь ответить. Продолжая историю регенеративной медицины, мы расскажем о терапии секретóмом — области, которая занимается изучением и разработкой «коктейлей» из сигнальных факторов, которые могли бы заставить наши собственные клетки взяться за восстановление поврежденных органов.
Регенеративная медицина

Медицина без преувеличения преобразила жизнь всего человечества, позволив спасать от ран и лечить от болезней, в том числе — в недавнем прошлом неизлечимых. И хотя ее развитие не прекращается, в отдельную новую дисциплину выделяют медицину регенеративную, цель которой — восстанавливать повреждения тканей и органов, а также продлевать их бесперебойную работу, активируя внутренний регенеративный потенциал организма. Применение в реальной клинической практике стволовых клеток и компонентов их секретома; тканевая инженерия; активация обновления и регенерации клеток — уже реальность или пока отдаленная фантастика?
Партнер проекта — российская фармацевтическая компания «Биотехфарм», занимающаяся поставкой и продвижением лекарственных средств и изделий медицинского назначения в сфере гинекологии, урологии и репродуктивной медицины. Компания продвигает высокотехнологичные препараты, в том числе на основе цитокинов, секретомов, гиалуроновой кислоты и лактобактерий.
Главные препараты компании — «Суперлимф®», созданный на кафедре иммунологии РНИМУ им. Н.И. Пирогова, применяющийся для регенеративного лечения раневых поверхностей и инфекционных заболеваний урогенитального тракта; а также средства для интимной гигиены — «Эстрогиал™» и «Ацилакт ДУО».
Цель регенеративной медицины — активируя внутренний потенциал организма, восстанавливать повреждения, перед которыми классическая медицина бессильна. На пути к этой цели мы соединяем клеточную и молекулярную биологию, физиологию, иммунологию, клиническую медицину, науки о материалах и другие дисциплины — читайте первую статью спецпроекта «Не можешь излечить — восстанови! Как появилась регенеративная медицина и какие у нее возможности сегодня» [1]. В статье о тканевой инженерии [2] мы описали, как создавать новые ткани, заселяя биоинженерные каркасы живыми клетками: печатать сосуды, выращивать трахеи и заменители кожи. Клеточные технологии [3] не отстают — мы учимся пересаживать стволовые клетки и использовать их потенциал в регенерации; и тренируем лимфоциты для поиска опухолей. Но можно ли обойтись препаратами без клеток?
Здесь мы расскажем о терапии секретóмом (или бесклеточной терапии). Она отличается от уже описанных подходов тем, что использует не сами клетки, а только выделяемые ими молекулы. Звучит обманчиво просто, но на деле подводных камней будет немало. Для начала проясним, что такое секретóм и какую роль он играет в нормальной физиологии и регенерации.
Итак, клетки — строители и строительные блоки в одном лице — трудятся, обеспечивая жизнедеятельность организма. Совместная работа требует постоянной связи друг с другом и обмена информацией. При описании клеточной коммуникации просится аналогия с музыкой. Для непрофессионала тонкости игры на музыкальном инструменте, не говоря уже об управлении оркестром, скрыты — он только слышит мелодию, не задумываясь, как она рождается. Так же обстоят дела с клеточным «общением» — ученые, хотя уже имеют представление о механике клеточной «музыки», еще далеки от полного понимания, не говоря уже о сочинении симфоний.
Клеточная коммуникация строится на широком спектре сигнальных молекул, немалую долю которых составляют белки и пептиды — отдельные «ноты» музыки клеток. Бесчисленные факторы роста, гормоны, цитокины, хемокины и другие молекулы, регулирующие деление, дифференцировку и функции, не просто роятся во внеклеточной жидкости. Это — тонко подобранные сочетания «звуков», которые клетки «слышат» и, повинуясь зову, работают слаженно и гармонично.
«Слышат» клетки в основном при помощи белков-рецепторов, которые в ответ на связывание лиганда могут открывать трансмембранные ионные каналы, активировать G-белки или фосфорилировать себе подобных — все это запускает каскад реакций, меняющих поведение клетки. При быстром ответе задействуется только белковая машинерия (например, макрофаг связывает рецептором молекулу клеточной стенки бактерии и фагоцитирует ее). Более масштабный ответ меняет также экспрессию генов (например, рецептор инсулина снижает экспрессию ферментов синтеза глюкозы).
Мы остановимся на локальной, паракринной, «камерной» сигнализации, формирующей микроокружение клеток — ореол сигнальных молекул и внеклеточного матрикса, в тесной связи с которыми существует каждая клетка [4]. Секретóм (та самая музыка) относится к первой — молекулярной — составляющей микроокружения. Давайте теперь составим более четкий портрет главного героя нашей статьи.
Секретóм
Впервые этот термин был употреблен в 2000 году в отношении бактерии Bacillus subtilis [5] — он объединял все секретируемые клеткой белки вместе с системой их секреции. Сейчас секретóм (и здесь последний раз ставим ударение) определяется как сумма молекул, секретируемых во внеклеточное пространство клеткой, тканью, органом или организмом. В состав секретома входят самые разные соединения: сигнальные белки, компоненты внеклеточного матрикса, липиды, ДНК, кодирующие и некодирующие РНК, о роли которых мы расскажем далее. А сейчас обсудим смысл суффикса — что это за -ом?
Еще один в семействе «-омов»
Изучением «-омов» и их практическим применением занимаются мультиомиксные технологии, суть которых в работе не с отдельными молекулами или структурами, а с их полными совокупностями — введение сделано в статье «„Омики“ — эпоха большой биологии» [6]. К примеру, геномика оперирует полностью секвенированным геномом организма и пытается изучить работу и взаимодействие всех генов; транскриптомика изучает совокупность РНК; а протеомика — все экспрессируемые белки клетки или организма. И, конечно, все эти «омы» активно взаимодействуют друг с другом — всю эту сверхсложную мозаику мы изучали в спецпроекте «Мультиомиксные технологии».
Фракции секретома — нотная грамота
Секретом регулирует пролиферацию и клеточную гибель, адгезию и миграцию клеток, организацию внеклеточного матрикса [7]; влияет на рост сосудов и нервов и обладает иммуномодулирующим действием. Всё это богатство функций выполняется различными его фракциями (рис. 1) [8]:
- Белковой (факторы роста, цитокины, хемокины, гормоны, белки внеклеточного матрикса и ферменты) — это, по большей части, отдельные ноты; и
- Внеклеточными везикулами, которые переносят разнообразные сигнальные белки, липиды, нуклеиновые кислоты и другие молекулы — их можно сравнить с аккордами. Почитайте: «Экзосомы: научная альтернатива сказочным молодильным яблокам» [9].
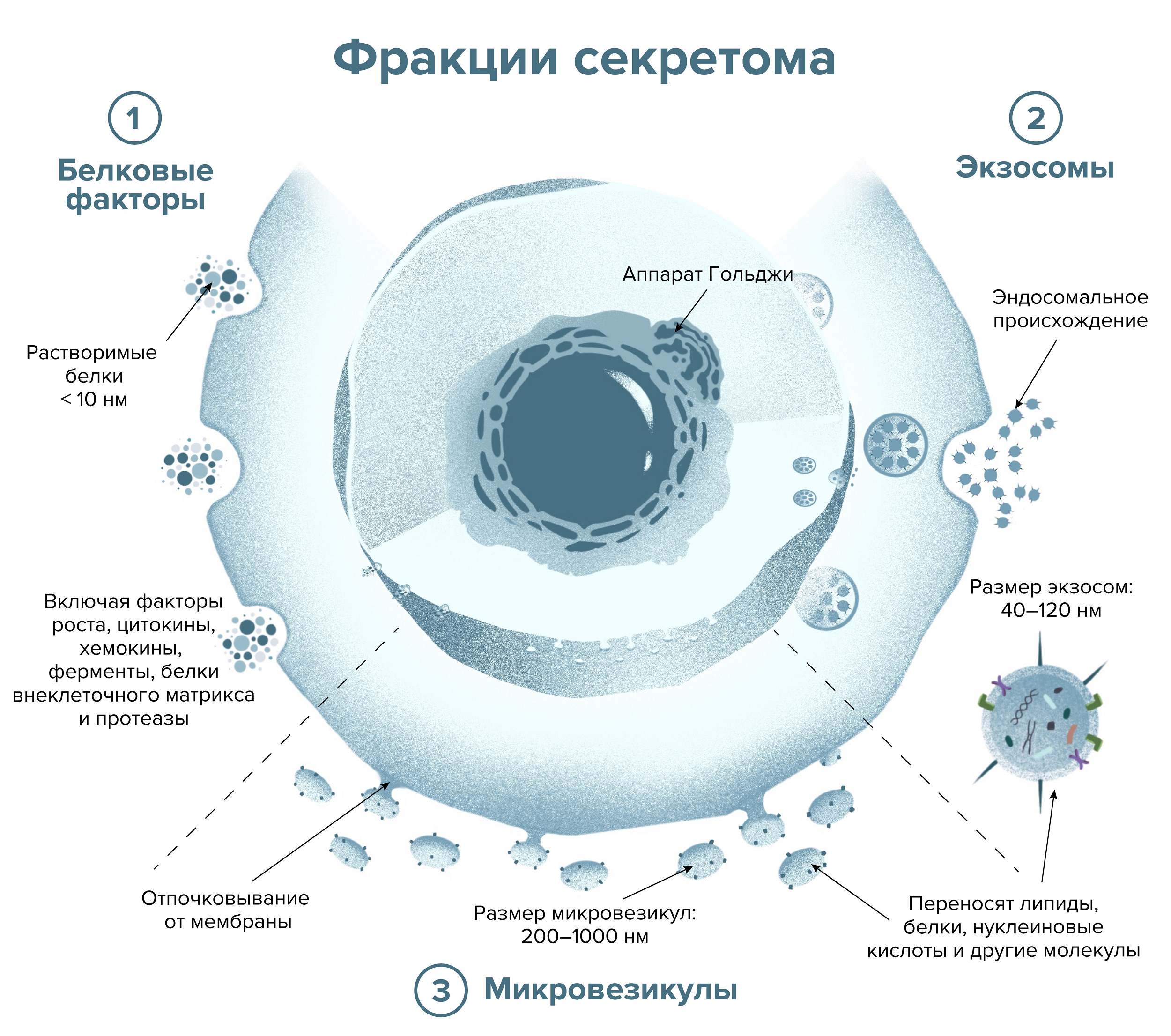
Рисунок 1. Какие фракции есть у секретома? Клетки выделяют отдельные молекулы и целые пузырьки: микровезикулы и миниатюрные экзосомы, несущие разные сигнальные соединения. Это и есть секретом.
иллюстрация Александры Мартыновой по [8]
Фракция белков — ноты
Давайте познакомимся с посредниками общения клеток поближе — рассмотрим основные классы белков секретома и широкими мазками опишем их роль в поддержании нормального функционирования ткани.
это биологически активные молекулы, стимулирующие или подавляющие митоз и направляющие дифференцировку клеток. Они могут быть пептидами, липидами (как некоторые гормоны: андрогены и эстрогены) и даже малыми молекулами: это оксид азота (II) или активные формы кислорода [10]. Несмотря на то, что обозначение «фактор роста» — скорее призвание молекулы, а не описание химической структуры, подавляющее большинство факторов роста — белки, о которых мы и будем говорить.
Цитокины —
группа небольших (5–25 кДа) сигнальных белков, регулирующих иммунные процессы. Они используются как внутри иммунной системы, так и для связи с другими клетками. Цитокиновая коммуникация разнообразна: есть как «средства массового оповещения», так и «каналы спецсвязи» — местные и дальние. В секретоме могут присутствовать следующие классы цитокинов:
- Колониестимулирующие факторы относятся к ростовым и стимулируют рост и пролиферацию различных линий иммунных клеток;
- Интерфероны — сигнал вирусного вторжения, в ответ на который клетки включают противовирусные гены [11];
- Интерлейкины регулируют пролиферацию, апоптоз, дифференцировку и активацию иммунных клеток; могут как стимулировать, так и подавлять воспаление [12];
- Цитокины семейства TNF (tumor necrosis factor — фактор некроза опухоли) также влияют на выживание клеток, играют роль в инициации, развитии и завершении воспаления и ремоделировании ткани [13].
Хемокины —
это сигналы «SOS». Клетки-бойцы первой линии обороны подают их при нарушении границ организма патогеном и при повреждении. В ответ происходит выход фагоцитов в кровеносное русло и облегчается их последующее перемещение в ткань. К «горячей точке» фагоциты движутся по градиенту концентрации хемокина и, добравшись до нее, выполняют свою работу по нейтрализации чужаков или уборке места повреждения [14].
Язык хемокинов включает разнообразные команды, большинство из которых регулируют движение. Причем отвечают на них не только иммунные клетки — хемокины контролируют клеточную подвижность при образовании плаценты и в эмбриогенезе, образовании кровеносных сосудов и перестройках ткани при патологиях [15–17].
Белки внеклеточного матрикса
Клетки ориентируются не только на «вербальные» знаки вроде цитокиновых сигналов — на них влияет также изменение структуры внеклеточного матрикса (ВКМ), компоненты которого составляют значительную часть белковой фракции. Но что такое внеклеточный матрикс и почему его все изучают [7], [18]? В рамках нашей музыкальной аналогии ВКМ — концертный зал и всё его оборудование: сцена, кресла для зрителей, пюпитры, нотная бумага. Это — пространство, наполненное информацией.
Сигналинг с помощью ВКМ может происходить как напрямую через клеточные рецепторы (например, интегрины и даже рецепторы ростовых факторов [19]), так и косвенно: матрикс сорбирует другие компоненты секретома, формируя их градиенты и запасая их. Фибриллярные белки, такие как коллаген и эластин, создают трехмерную сеть, погружаемую в гель на базе уже нефибриллярных белков. Жесткость, эластичность, пористость и другие физико-механические свойства матрикса также влияют на поведение клеток.
В состав секретома входят матриксные металлопротеиназы (MMP), сериновые протеазы, а также ингибиторы и активаторы протеолитических ферментов, участвующие в перестройке ВКМ [20]. При разборке ВКМ открываются новые пути для миграции клеток, высвобождаются из депо накопленные сигнальные факторы и выходят в раствор фрагменты структурных белков, модифицируются физические свойства микроокружения клеток. Взаимодействуя с постоянно меняющимся комплексом компонентов матрикса, клетки обмениваются информацией и получают сигналы о состоянии ткани, что необходимо для слаженной и осмысленной их работы [21], [22].
Мы разобрали основные группы молекул белковой фракции секретома. Однако не менее важную роль в клеточной коммуникации играют внеклеточные везикулы — своеобразные «посылки», включающие как разнообразные белки, так и другие типы биомолекул. Давайте разберемся, что они из себя представляют.
Фракция внеклеточных везикул — аккорды
Если белки — это отдельные простые сигналы наподобие нот, то внеклеточные везикулы можно сравнить с аккордами, ведь это более сложная форма коммуникации, чем отдельные молекулы: они переносят целые ансамбли биомолекул от клетки к клетке. Выделяют три класса внеклеточных везикул, различающихся по размерам и способу формирования:
- Микровезикулы диаметром 200–1000 нм отпочковываются от клеточной мембраны;
- Экзосомы невелики (50–100 нм) и выделяются при слиянии с клеточной мембраной мультивезикулярных телец («везикул с везикулами»; рис. 2) [23], [24];
- И, наконец, апоптотические тельца, на которые «разваливается» клетка при программируемой гибели, но о них мы говорить не будем.
Как мы уже упоминали, внеклеточные везикулы — не просто молекулярные «посылки»: они передают сигналы через несколько «подсистем». Одна из них — мембранные белки. Экзосома или микровезикула захватывает часть мембраны клетки-отправителя и сливается с мембраной получателя, передавая в том числе мембранные белки [25]. Кроме того, мембранный лиганд везикулы может действовать на клеточный рецептор мишени.
Еще один механизм везикулярного сигналинга связан с протеазами. Вооруженная этими мембранными белками экзосома или микровезикула превращается в автономный генератор сигнала и может расщеплять белки ВКМ (напоминаем, что матрикс — динамичная сигнальная среда) и мембранные лиганды клеток [26].
Также клетки могут захватывать внеклеточные везикулы путем фагоцитоза и макропиноцитоза («зачерпывание» мембранным выростом внеклеточной жидкости) [27]. Так что же в конечном итоге попадает в цитозоль из везикулы?
Что несут внеклеточные везикулы?
Они могут переносить белковые факторы: цитокины, хемокины и факторы роста и даже секретировать их самостоятельно в матрикс. Кроме белков, экзосомы и микровезикулы переносят липиды, сахара и даже нуклеиновые кислоты, роль которых в действии секретома не менее важна.
Липиды — не только структурный элемент везикул. Состав липидов мембраны определяет механизм отпочковывания везикул и тип клеток, которым они адресованы. При слиянии мембраны экзосомы или микровезикулы с клеткой ее мембране передаются липидные молекулы, способные модифицировать поведение. Так, например, церамид — сфинголипид мембраны экзосом — может запускать программируемую клеточную гибель. Фосфатидилсерин влияет на иммунные клетки, связываясь с рецепторами TIM1 и 4 (T cell immunoglobulin mucin domain). Липидóм внеклеточных везикул не статичен — экзосомы можно сравнить с фабрикой сигнальных липидов, содержащих ферменты синтеза эйкозаноидов (простагландинов, лейкотриенов и тромбоксанов), регулирующих свертывание крови, иммунный ответ, ангиогенез и другие процессы. И это только малая часть известных механизмов липидного сигналинга внеклеточных везикул [28].
Экзосомы несут целый спектр нуклеиновых — одно- и двухцепочечные ДНК (в том числе митохондриальные); и матричные и некодирующие РНК (транспортные, малые некодирующие и микроРНК) [29]. Было показано, что митохондриальная ДНК экзосом способна передаваться клеткам-реципиентам и поддерживать функционирование их митохондрий. Отдельного упоминания заслуживают малые некодирующие и микроРНК. Они регулируют транскрипцию и трансляцию белков (по последним данным, могут влиять на экспрессию 30–70% генов) [30], радикально меняя фенотип клеток. Например, микроРНК экзосом мезенхимных стромальных клеток (о которых мы поговорим позже) способны заставлять зрелые клетки (миофибробласты) дедифференцироваться [31]. Также микроРНК могут влиять на иммунный ответ и определять выживание клеток [32], направлять рост аксонов. Если хотите узнать о них больше — обратитесь к статьям «Обо всех РНК на свете, больших и малых» [27] и «Кодирующие некодирующие РНК» [33].
Итак, с нотной грамотой мы разобрались, пора познакомиться с секретомом в деле. Тут все группы инструментов будут звучать вместе, и, чтобы увидеть (услышать?) цельную картину, мы все-таки сосредоточимся на отдельных актах регенерации и конкретных функциях секретома.
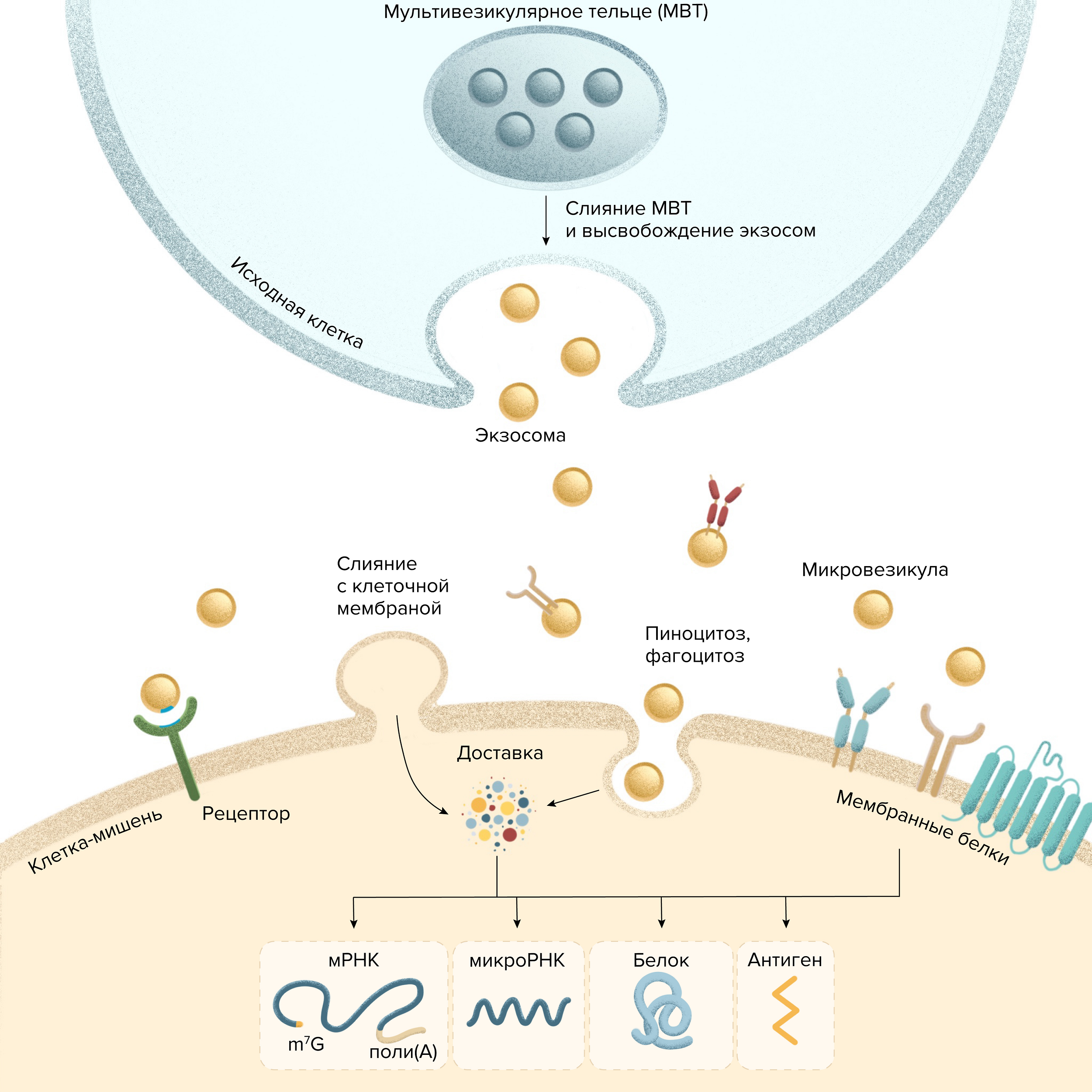
Рисунок 2. Механизм образования, принцип действия и транспортируемые факторы микровезикул и экзосом. Внеклеточные везикулы могут передавать сигнал разными способами: сливаться с мембраной клетки-мишени, передавать нуклеиновые кислоты, липиды, антигены и белки. А еще они умеют активировать мембранные рецепторы.
иллюстрация Александры Мартыновой по [24]
Секретом стволовых клеток в регенерации
За счет чего восстанавливаются испорченные структуры и обновляются клетки, откуда берется новый материал? Некоторые дифференцированные клетки способны к пролиферации, однако другим высокая специализация не позволяет свободно делиться. Тогда на помощь приходят соматические стволовые клетки, способные к самообновлению, пролиферации и дифференцировке в клетки одной ткани или одного зародышевого листка.
Среди соматических стволовых клеток (СК) выделяют нейральные, эпителиальные, гемопоэтические, эндотелиальные и другие. Подавляющее большинство исследований секретома последних лет связано с мультипотентными мезенхимными стромальными клетками (МСК) [34]. Важно отметить, что выделенные из стромы органа МСК — не однородная популяция СК, а набор разных по фенотипу клеток, составляющих нишу стволовой клетки, и в этот набор входит некоторое (небольшое) число истинных стволовых клеток. В состав этой ниши входят сами СК, а также их микроокружение, регулирующее их поведение. После повреждения ниша активируется, раскрывая свой регенеративный потенциал, в то же время поддерживая пул СК. За это как раз и отвечают мультипотентные мезенхимные стромальные клетки. Они секретируют различные паракринные факторы, изменяют структуру ВКМ и привлекают эффекторные клетки для восстановления ткани. Кроме того, МСК сами способны к дифференцировке и при необходимости дают начало таким клеткам соединительной ткани как адипоциты, хондробласты и остеоциты [19]. МСК популярны в использовании и хорошо изучены и поэтому будут в центре внимания статьи.
«Биомолекула» уже не раз обращалась к теме стволовых клеток: «Такие разные стволовые клетки» [35] и «Лаборатория стволовых клеток мозга: мир новых нервных клеток у взрослых животных» [36]; также рекомендуем прочитать статью «Секрет для стволовых клеток».
Регенеративным потенциалом СК обладают благодаря хоумингу (миграции к месту повреждения), дифференцировке и секреции паракринных факторов. Мы разберем последние по нескольким причинам: во-первых, паракринная регуляция преобладает над другими механизмами (рис. 3) [37], [38]; а во-вторых, мы говорим о терапии секретомом.

Рисунок 3. Применение стволовых клеток и их секретома в регенеративной медицине. Введенные в организм стволовые клетки регулируют регенерацию паракринно. Почему бы тогда не использовать готовый секретом?
Секретом в регенерации — голоса паракринной симфонии
Для того, чтобы обеспечивать слаженную работу клеток, секретому — нашей музыкальной композиции — тоже нужно иметь много голосов. В этом разделе мы разберем функции, которые контролирует секретом, и наборы сигнальных факторов, которые в этом участвуют — отдельные «партии» паракринной музыки (рис. 4) [39].
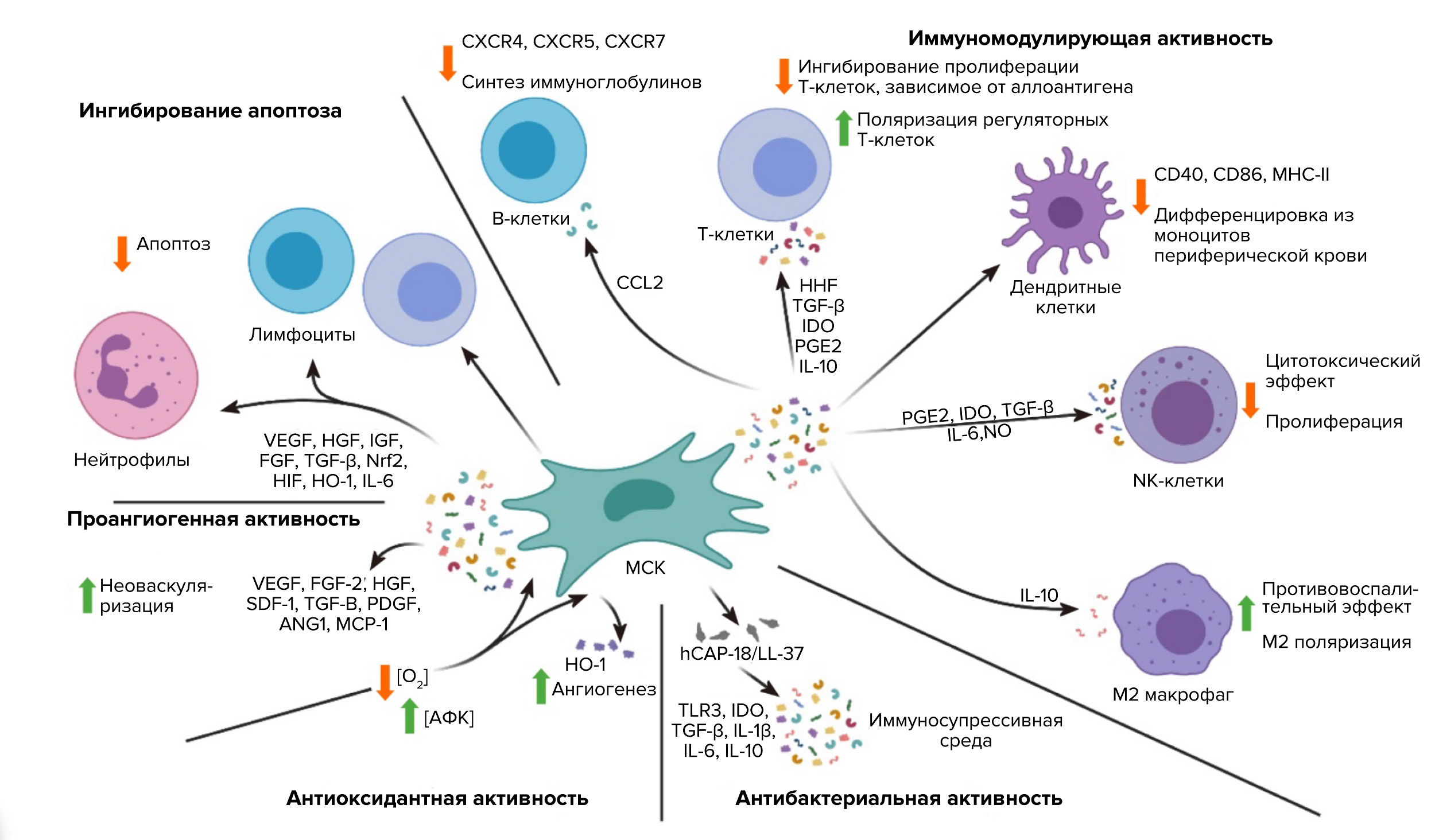
Рисунок 4. Секретом и его многогранное влияние на регенерацию: белковые факторы и везикулы командуют иммунными клетками, снижают агрессивность среды, направляют рост сосудов и нервных окончаний, защищают клетки от гибели и микробного вторжения.
Антимикробные свойства — на страже границ
Если представить классический случай регенерации, к примеру, заживление открытой раны, становится понятно, что место повреждения необходимо защитить от инфекции. На этот случай в арсенале секретома есть белки с антимикробной активностью, такие как кателицидины, дефензины, гепсидин и липокалин [40]. Кателицидины — амфифильные пептиды, связывающиеся с мембраной бактерий и разрушающие ее; так же работают и дефензины [41], [42]. Гепсидин и липокалин снижают концентрацию железа во внеклеточной среде, что тормозит рост бактерий [43]. Антимикробные пептиды также активируют и привлекают клетки иммунной системы. Об этих интересных молекулах вы сможете прочитать в статье «Антимикробные пептиды — возможная альтернатива традиционным антибиотикам» [44].
Иммуномодуляторные свойства — всему свое время
Иммунные клетки играют важную роль в защите организма при повреждении и последующем восстановлении, поэтому иммуномодулирующее действие секретома существенно для регенерации [39].
В зависимости от обстоятельств, секретом может обладать как про-, так и противовоспалительным действием. Так, сразу после повреждения в среде растет концентрация провоспалительных цитокинов, что повышает выделение провоспалительных агентов МСК. А при переходе к репарации ткани растет доля противовоспалительных факторов — это позволяет переключиться с разрушения на восстановление [39].
Первыми в очаг повреждения прибывают нейтрофилы, откликаясь на зов хемокинов из спектра секретома; а уже на месте некоторые внеклеточные везикулы и интерлейкин-10 (ИЛ-10) снижают их подвижность и подавляют воспалительную активность. Эти сигналы разнесены во времени: первый подается сразу после травмы, а второй — когда настает время восстанавливать повреждение [45].
Важным компонентом врожденного иммунитета являются макрофаги. Под влиянием того же ИЛ-10 они изменяют фенотип с провоспалительного М1 на противовоспалительный М2, вследствие чего принимают активное участие в перестройке и восстановлении ткани [46]. Такое же действие ИЛ-10 оказывает на дендритные клетки.
Секретом укрощает адаптивный (приобретенный) иммунитет: TGF-β, PgE2, ИЛ-10 и индоламиноксигеназа подавляют пролиферацию «воинствующих» (Т-киллеры) и стимулируют дифференцировку «миротворческих» (регуляторные Т-хелперы) клеток. Также секретом снижает чувствительность В-клеток к хемокинам и выработку ими антител. Фактически, МСК с помощью секретома сперва помогают иммунной системе в защите организма, а затем «успокаивают» ее, когда пора заканчивать сражаться и начинать восстанавливать повреждения [45].
Проангиогенные свойства: даешь кровь для регенерации!
При регенерации, как и в послевоенное время, необходимо прокладывать новые пути снабжения, чтобы обеспечивать нормальное питание клеток, предотвращать гипоксию и поставлять строительные материалы. В состав секретома входят многочисленные ангиогенные факторы, которые организуют и направляют рост сосудов (VEGF, FGF2, TGF-β и другие), — это необходимый этап в восстановлении тканей [47].
Зеленый свет аксонам — ростовые факторы и микроРНК улучшают реиннервацию после травмы
При повреждении ткани страдают и нервы — от механического повреждения аксонов до дегенерации в условиях ишемии. Для полного восстановления ткани необходимо возобновить ее иннервацию, что бывает сложно, особенно для взрослого организма. В области дегенерации поврежденного аксона развивается воспаление, активируется и пролиферирует глия, формируя рубец и выделяя факторы, работающие как «стоп-сигналы» для регенерирующего волокна. Однако некоторые факторы глиального секретома разрешают эту ситуацию. Среди них — сигнальные белки, стимулирующие рост аксона (например, Wnt), и экзосомы, которые передают конусу нарастания волокна направляющие его рецепторы и внутриклеточные факторы (такие как рецептор фактора роста нервов р75 и синапсин-1). МикроРНК тоже помогают: они снижают экспрессию тех белков, которые «мешают» росту аксона (фактора роста нервов NGF, ингибитора Wnt-сигналинга Kremen1 и других) и повышают ее у «про-ростовых» белков, таких как фосфатаза PTEN [48]. Сходным эффектом обладает секретом МСК.
Подавление гибели клеток и индукция пролиферации — секретом спешит на помощь
В агрессивных условиях часто запускаются программы клеточной гибели, хотя, казалось бы, для регенерации нужно наоборот наращивать клеточную массу. Апоптоз [49] позволяет удалить поврежденные и дефектные клетки и облегчает последующее восстановление ткани, но этот процесс нужно вовремя остановить. Первый способ — снизить агрессивность среды: обеспечить васкуляризацию и снизить уровень активных форм кислорода. Последним занимаются антиоксидантные белки, такие как гемоксигеназа-1. Кроме того, компоненты секретома, такие как факторы роста сосудов (VEGF), фибробластов (FGF), гепатоцитов (HGF) и инсулиноподобный фактор роста (IGF) напрямую «отговаривают» клетки уходить в апоптоз [50].
Секретомные препараты: от теории к практике
Теперь, когда мы познакомились c «языком» секретома, самое время попытаться научиться его использовать. Казалось бы, всё что осталось — это сформулировать систему молекулярных команд и применить их. Однако не всё так просто. Даже в рамках организма, без какого-либо врачебного вмешательства, клетки часто не могут договориться. Безобидное самообновление может обернуться раком, а при длительных или особо сильных повреждениях может начаться фиброз или хроническое воспаление [51].
Изготовление секретомных препаратов сродни сочинению музыки — только такой, которую клетки исполняют для клеток. Поэтому, во-первых, нужно создать произведение, которое слушатели поймут правильно; а во-вторых, заставить музыкантов его верно играть. Но сначала нужно собрать оркестр.
Источники секретома в регенеративной медицине — духовые или струнные?
Для того, чтобы создать сигнальную симфонию, нужно набрать музыкантов. У каких клеток заимствовать все необходимые факторы, на каких инструментах остановиться? Давайте посмотрим, что имеется в распоряжении и что доступнее:
- Мононуклеарные клетки периферической крови (PBMCs, peripheral blood mononuclear cells) — лимфоциты (Т- и В-клетки и натуральные киллеры), моноциты (будущие тканевые макрофаги) и дендритные клетки, которые циркулируют в крови. Интересно, что секретом «умирающих» мононуклеаров тоже используют в регенеративной медицине. Клетки вводят в апоптоз ионизирующей радиацией и собирают выделенные ими факторы. На «Биомолекуле» можно посмотреть видео со способом выделения мононуклеаров [52].
- Тромбоциты и плазма, богатая тромбоцитами (PRP, platelet-rich plasma) — достаточно доступный источник секретома. Наверное, это один из самых известных и первых методов бесклеточной терапии, не использующих стволовые клетки. Плазму, богатую тромбоцитами, получают из крови пациента путем центрифугирования. Впервые PRP начали использовать еще в 1980-х в челюстно-лицевой хирургии (было описано, что она имеет противовоспалительный эффект и стимулирует пролиферацию клеток) [53].
- Мезенхимные стромальные клетки — самый широко используемый источник секретома. Их получают из костного мозга, жировой, костной и хрящевой ткани, а также тканей и жидкостей плода: МСК пупочного канатика, амниотической жидкости, амниотической мембраны, Вартонова студня (слизистой пуповинного канатика) и других структур [54]. Такое изобилие источников МСК облегчает их получение и, соответственно, изготовление препаратов. Помимо секретома МСК, используются факторы, выделяемые эмбриональными стволовыми клетками, а также стволовыми клетками взрослого организма, такими как прогениторные клетки миокарда.
Итак, мы выбрали инструмент. Пусть это будет МСК — про секретом этих клеток уже много всего известно. У разных МСК — разный «голос» (состав секретома и его свойства), различающийся в зависимости от места и способа выделения [55], [56], а также между донорами клеток [57]. Однако состав паракринных факторов клетки не постоянен: его можно изменять, оказывая на культуру МСК определенные воздействия, и получать тот секретом, который нам нужен.
Конструирование секретома — репетируем с оркестром
Допустим, мы знаем, что нам нужно; «мелодия» уже играет в голове — осталось только обучить наш коллектив ее исполнять. Как это сделать? Как мы уже убедились, МСК подают разные молекулярные сигналы в зависимости от обстановки в микроокружении [58]. Воспользуемся этим свойством.
Прекондиционирование
Настраивать секретом МСК можно, «подгоняя» условия культивирования под ту или иную «ситуацию» в клеточной жизни. Например, в культивационную среду можно добавить провоспалительные цитокины (ИЛ-1, TNF, IFN-γ) и липополисахарид (компонент мембраны грамотрицательных бактерий). Случись такое в организме, по прошествии времени МСК начали бы выделять факторы, снижающие воспаление, что происходит и в культуре. Секретом таких клеток будет содержать противовоспалительные, антиапоптотические и ангиогенные факторы [45].
Так же работает воздействие на МСК гипоксией. Как и в ткани, лишенной кровоснабжения, клетки начинают выделять проангиогенные ростовые факторы, такие как VEGF, FGF, IGF и TGF-β и другие сигнальные регенераторные молекулы [59].
Влиять на клетки можно не только при помощи биомолекул. В месте повреждения, где должны начаться процессы восстановления ткани, создаются особые механические условия — к примеру, повышенное давление, изменение жесткости или геометрии матрикса. Такие изменения среды заставляют клетки обогащать секретом факторами, важными, например, при образовании и регенерации хряща и кости [60].
Еще один способ прекондиционирования — рост в сфероидных и других 3D-культурах, которые отличаются от 2D-культур тем, что клетки могут расти во всех направлениях и устанавливать больше контактов друг с другом и с матриксом (что ближе к условиям в организме). Секретом МСК, выращенных в таких культурах, более эффективен в регуляции воспаления и ангиогенеза и лучше защищает ткань от фиброза [61].
Использование генно-модифицированных МСК
Прекондиционирование — хороший способ «настроить» МСК на нужный лад, однако всё же он косвенный, и у клеток остается некоторая свобода выбора секретируемых факторов. Но можно вмешаться в этот процесс и напрямую — генная инженерия позволяет выключать, усиливать или ослаблять экспрессию нужных исследователю белков. В данном случае человек непосредственно может «настраивать» концентрацию отдельных факторов секретома. Модифицируют клетки при помощи лентивирусных [62] и аденовирусных [63] векторов, которые доставляют в клетки нужный ген или систему редактирования генома [44]. С методами генной инженерии предлагаем ознакомиться в статьях «12 методов в картинках: генная инженерия. Часть I, историческая» [64] и «12 методов в картинках: генная инженерия. Часть II: инструменты и техники» [65].
Помимо влияния культуральной среды и генной инженерии существуют и другие способы «настройки», такие как использование микрочастиц для доставки малых молекул в цитоплазму клеток [66].
Этапы получения секретома — от фабрики музыкальных инструментов до записи концерта
Итак, мы поняли, как извлекать из наших клеток (музыкантов или инструментов) желаемую мелодию. Осталось закрепить этот относительный успех так, чтобы наш оркестр выступал от раза к разу одинаково. В этом разделе мы пройдем от фабрики музыкальных инструментов до записи концерта. Давайте разберем главные шаги на пути к получению секретома с нужными нам свойствами (рис. 5) [67]:
- Получение первичной культуры МСК на сыворотке или бессывороточной среде. На этом этапе культура клеток должна как следует разрастись (до 70–80% площади подложки);
- Отмывка и прекондиционирование клеток. Сперва клетки переводят в среду без сыворотки, и все посторонние молекулы отмывают; затем их при необходимости обрабатывают набором провоспалительных цитокинов, гипоксией или механически;
- Отделение кондиционированной среды. Чаще всего среду с продуктами секреции клеток собирают на второй-третий день после запуска кондиционирования, но иногда максимальная концентрация белковых факторов наблюдается на 7–10 день [68]. На этом этапе среду отделяют от клеток, центрифугируют и очищают (например, ультрафильтрацией). Теперь у нас в руках — очищенный секретом, содержащий основные выделяемые клетками регенеративные факторы и везикулы;
- Концентрирование и очистка секретома. Далее можно разделить белковую и везикулярную фракцию и проанализировать их: по протеому обычно смотрят, насколько клетки «поняли», что им нужно выделять. Есть два подхода: таргетный (когда определяют заранее выбранные белки, например, иммунохимически); и шотган-протеомика, когда сначала грубо разделяют белки по массе (например, с помощью электрофореза), а потом определяют их методом масс-спектрометрии [69], [70].
Если нужный состав секретома уже достигнут, остается его очистить и концентрировать. В конце мы получаем свободный от клеток и прочего мусора секретом — по сути, раствор белковых факторов и везикул, биологическую активность которого сперва проверяют. Тест на биологическую активность имитирует предполагаемую ситуацию, в которой должен действовать препарат. Это может быть животная модель патологии либо оценка выделения фактора-маркера активности и эффектов препарата in vitro [71]. Например, если мы разрабатываем препарат на основе секретома МСК, улучшающий рост сосудов, нужно оценить содержание VEGF (как маркера активности) в секретоме и проследить, что в культуре клеток секретом МСК должным образом влияет на клетки сосудов, стимулируя ангиогенез. Только после оценки активности можно думать о путях введения.
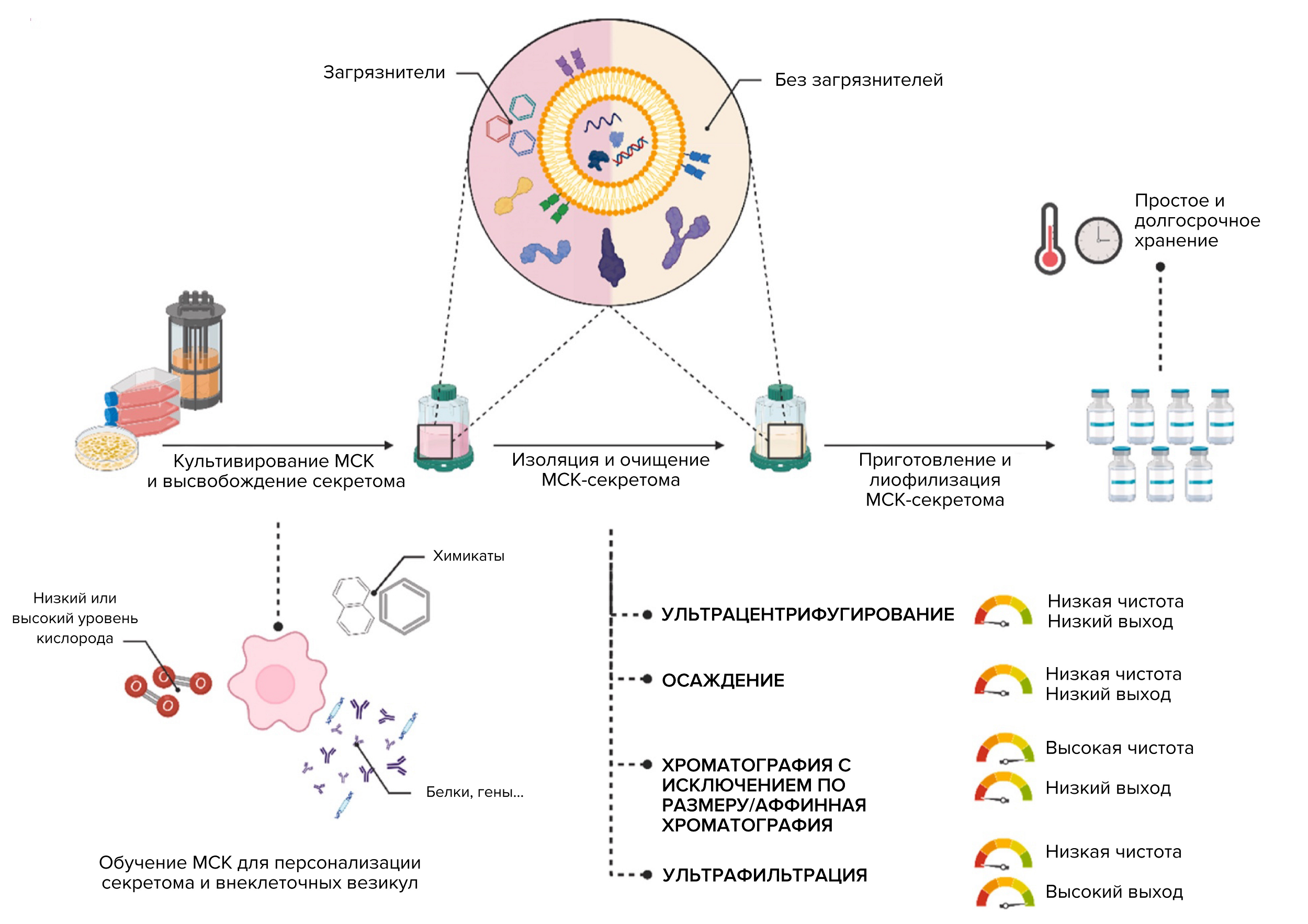
Рисунок 5. Как получить секретом с необходимыми свойствами? Процесс включает получение культуры МСК, рост культуры и прекондиционирование, выделение, очистку и концентрирование секретома.
Способы доставки секретома — винил или цифра?
После того, как мы обучили наш клеточный оркестр играть желанную музыку, осталось представить его публике. Способов много — можно записывать виниловые пластинки, которые ценят любители, оцифровать звук или передавать концерты по радио. Давайте рассмотрим, как можно доставлять сконструированный нами секретом для эффективного применения.
- Системное или местное введение. Самый очевидный метод доставки секретома — инъекция. Вводить препарат можно внутривенно, надеясь, что он достигнет места действия (по пути не отфильтровавшись и не деградировав). В научной литературе описано применение этого метода введения для лечения артрита и токсического повреждения миокарда в животных моделях [72], [73]. В рамках нашей музыкальной метафоры системное введение будет аналогично радиоэфиру, и тут уже эффект будет зависеть от того, есть ли в квартире приемник, какая у него громкость и чем заняты хозяева. Местное введение — более точный способ. Как пример можно привести введение в суставную сумку экзосом МСК для регенерации хряща у крыс. Экзосомы улучшали регенерацию хряща, повышая выживание и пролиферацию хондроцитов и снижая воспаление [60]. А локальное введение секретома МСК под белочную оболочку семенников позволило стимулировать восстановление сперматогенеза на животной модели и было сопоставимо по эффективности с введением самих клеток [74].
-
Микрочастицы. Из-за короткого времени жизни нашего препарата в крови (помним, что белки очень быстро расщепляются протеазами) необходимо хроническое его введение. Это неудобно, а поэтому прибегают к использованию различных полимерных конструкций, которые могут постепенно высвобождать сигнальные вещества. Особенно интересны «искусственные клетки» — микрочастицы полимера с секретомом 1–2 микрометра в диаметре, одетые в клеточную мембрану (рис. 6) [75]. В данном случае совмещается поддержание постоянной концентрации сигнальных факторов и таргетная доставка [76], [77].
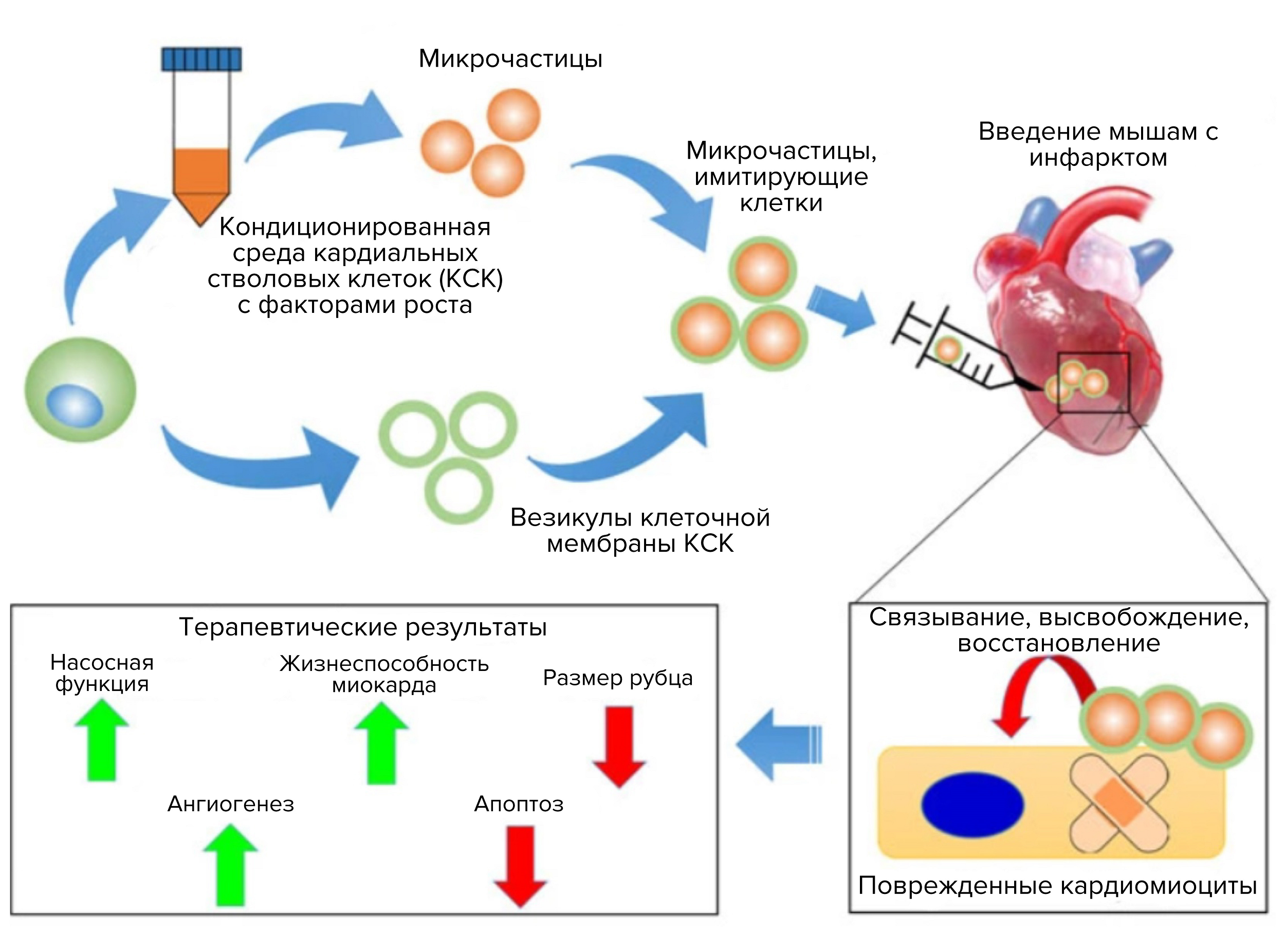
Рисунок 6. Микрочастицы на основе стволовых клеток миокарда имеют клеточную мембрану и полимерное ядро. Полимер пропитывается секретомом, который потом из него диффундирует наружу с определенной скоростью, а мембрана позволяет взаимодействовать с эндотелием сосудов и кардиомиоцитами — прямо как настоящим клеткам. Это обеспечивает таргетную доставку и постепенное высвобождение секретома.
Больше способов доставки — на рисунках 7—9.
-
Полимерные гели и скаффолды. Скаффолд — полимерная синтетическая (например, PLA, poly-lactic acid — полимер молочной кислоты) или органическая (альгинат, коллаген) матрица. Такие приспособления позволяют поддерживать постоянную концентрацию факторов в месте наложения. Так, в мышиной модели заживления раны альгинатная матрица с секретомом МСК обеспечивала постепенное высвобождение факторов в течение 48 часов и стимулировала пролиферацию фибробластов и васкуляризацию.
Благодаря развитию 3D-биопринтинга появилась возможность создавать конструкции сложной формы на основе полимерных матриц. Если вкратце: полимер смешивают с секретомом и печатают нужную форму. Также в качестве полимерной матрицы используют гидрогели (рис. 7) [78].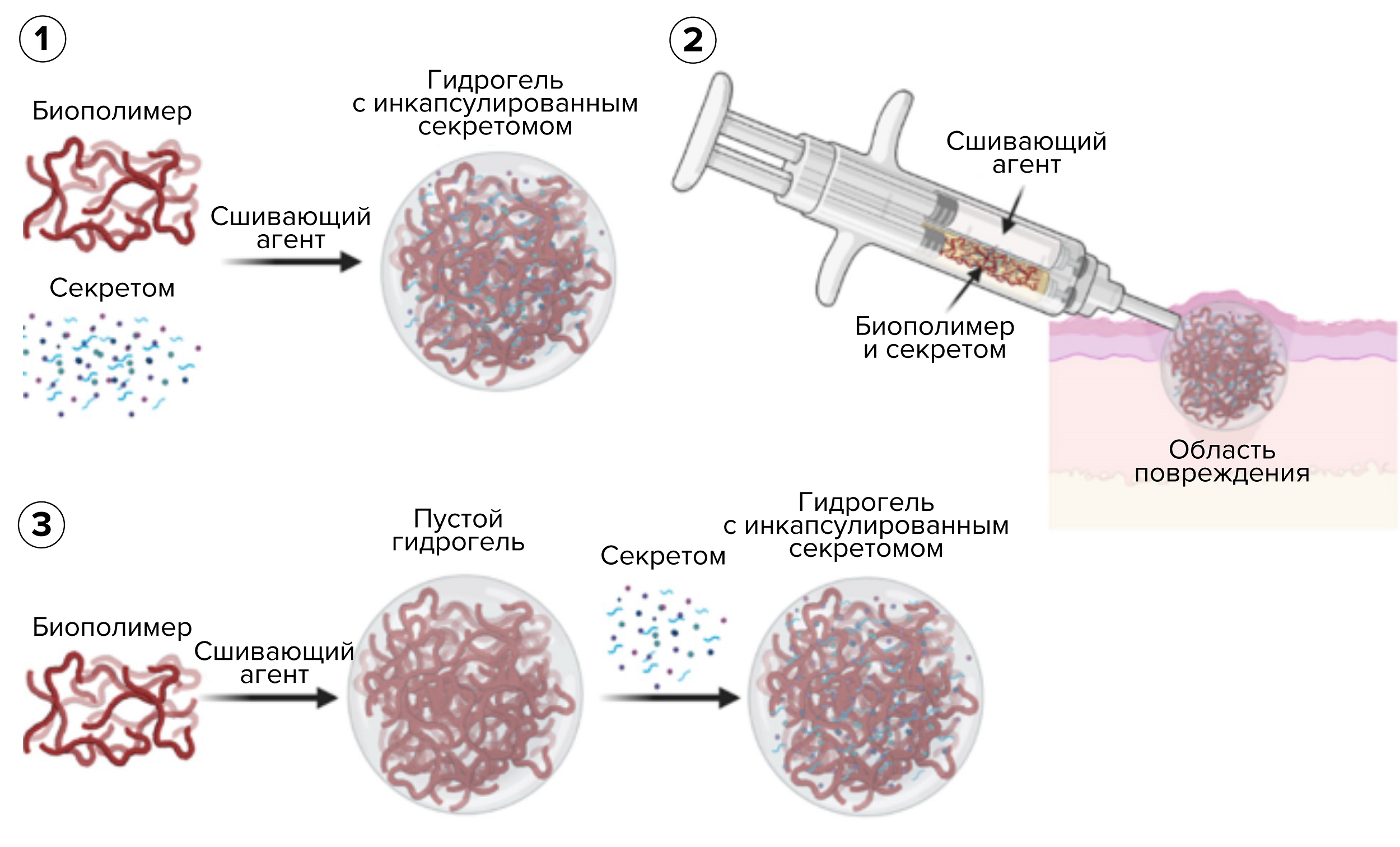
Рисунок 7. «Загрузка» гидрогеля секретомом и введение в место повреждения. Гидрогели используются для инъекций и локальной доставки белковых факторов и везикул. Что интересно, гидрогель сначала может использоваться для роста клеток, которые выделяют в него секретом. Затем гидрогель собирают и вводят в место повреждения.
-
Небулайзеры и ингаляторы. Довольно необычный, однако перспективный в респираторной медицине метод доставки. На сегодняшний день есть предложения применять ингаляции растворенным или лиофилизированным секретомом для регенерации тканей легкого, что, например, может пригодиться при терапии COVID-19 (рис. 8) [79].
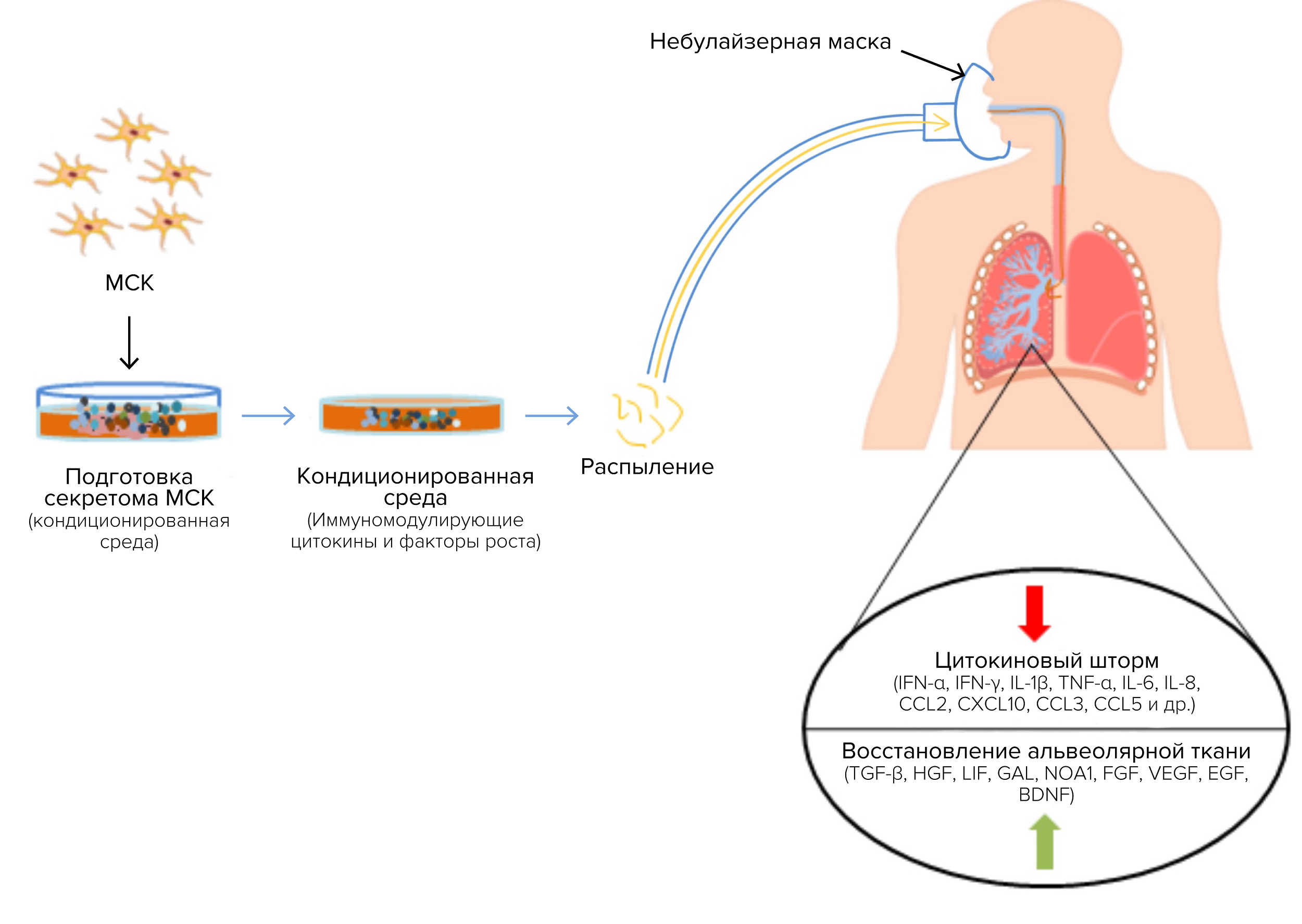
Рисунок 8. Секретомный небулайзер как удобный способ лечения респираторного дистресса при инфекции COVID-19. Распыленный секретом успокаивает цитокиновый шторм и запускает восстановление тканей легкого.
-
Спрей в некоторых случаях может быть эффективнее, чем наложение скаффолда, особенно когда речь идет о продуктах регенеративной медицины для заживления кожных дефектов. В распыляемую жидкость, обогащенную секретомом, можно включить полимерную составляющую, которая будет образовывать пленку для продления действия (рис. 9) [80].
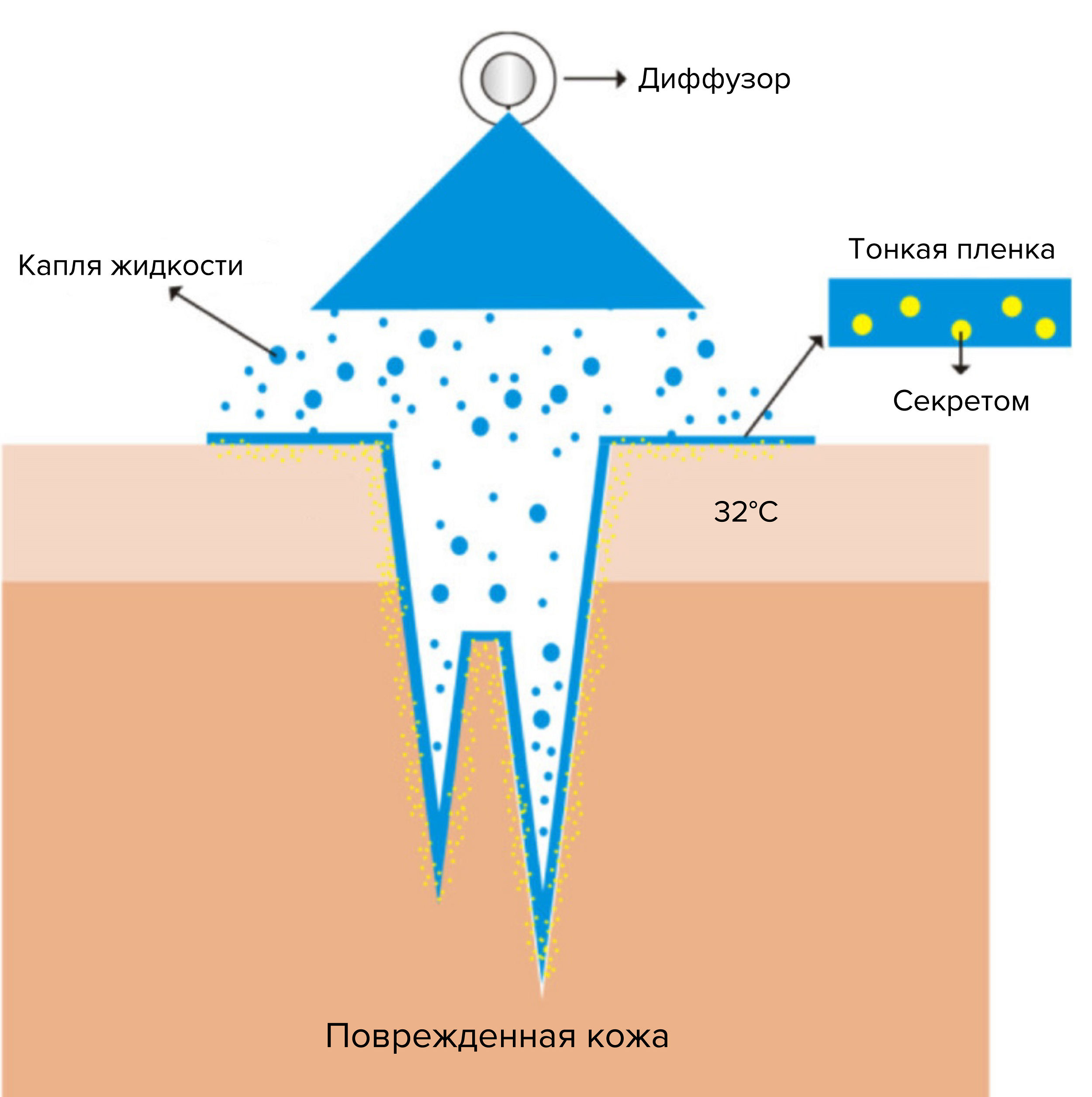
Рисунок 9. Принцип работы пленкообразующего спрея на основе секретома. Пленка доставляет меньше дискомфорта, чем полимерный скаффолд, и смывается водой.
Как вы видите, средств доставки довольно много — и это бесклеточные варианты. Но ведь сами клетки тоже можно рассматривать в качестве доставщиков секретома — это будет такой марширующий оркестр или гастролирующие музыканты. Однако, как и в случае с настоящими артистами, клетки бывают непредсказуемы: если музыкант может отказаться давать концерт, потому что организаторы не подготовили ему должным образом гримерку, клетка может «отказаться» секретировать нужные вещества. С бесклеточными технологиями проблем не меньше, но всё же давайте сначала рассмотрим их применение в регенеративной медицине.
Бесклеточные технологии в регенеративной медицине — суровая реальность
Казалось бы, после такого долгого рассказа этот раздел не должен нас разочаровать. Но, к сожалению, на данный момент одобренных FDA препаратов на основе секретома нет [81]. Однако как в США, так и в других развитых странах огромное количество продуктов на основе секретома клеток или его фракций (в первую очередь, экзомом) находится на доклинических или клинических стадиях исследований, и в ближайшие годы ожидается значительное увеличение количества зарегистрированных препаратов нового класса.
Стоит отметить, что широкое применение получило косметическое использование секретома (к примеру, для улучшения роста волос), которое не нуждается в одобрении, однако это не совсем медицина. Не FDA единой, скажете вы, но, тем не менее, на стандарты, используемые этой организацией, ориентируется весь мир.
Впрочем, в России зарегистрирован препарат на основе секретома мононуклеаров периферической крови — Суперлимф (см. партнерскую врезку далее), — но и он пока не получил одобрения за пределами нашей страны. В 2024 году Минздрав выдал разрешение на проведение регуляторных клинических исследований I/II фаз оригинального отечественного биологического лекарственного препарата на основе секретома МСК человека «МедиРег». Однако это единичные случаи. Поэтому здесь мы рассмотрим скорее перспективы применения секретома, которые в редких пока случаях реализуются в виде клинических испытаний.
- Патологии дыхательной системы. Секретом неплохо показал себя в животных моделях острого повреждения легких и астмы. Экзосомы МСК костного мозга способствуют переходу макрофагов в М2-фенотип, стимулируют репарацию ДНК и выведение из дыхательных путей бактерий [82]. В модели астмы внутривенное введение экзосом лучше снимало воспаление и инфильтрацию легких лейкоцитами, чем введение стволовых клеток [83].
Как мы уже упоминали, секретом подает надежды в терапии COVID-19. В исследовании 2022 года у пациентов ингаляция секретомом прошла без осложнений, и у четверых из семи участников поражение легких снизилось спустя пять дней применения небулайзера (рис. 8) [84]. Сейчас препарат проходит клинические испытания, результаты которых пока не опубликованы. В другом исследовании, где пациентам с COVID-19 системно вводили секретом МСК, у них росла сатурация и снижалось системное воспаление. Выживаемость при введении секретома выросла с 28% до 57% [85]. В МГУ разрабатывается новый препарат на основе внеклеточных везикул, секретируемых МСК человека, для борьбы с фиброзом легких, механизм действия которого основан на переносе специфических микроРНК, регулирующих дифференцировку фибробластов в миофибробласты — основные эффекторы фиброза. - Патологии кожных покровов. Если процесс заживления раны задерживается слишком долго на одном из этапов (гемостаз, воспалительная, пролиферативная фазы и ремоделирование ткани), это грозит развитием хронического повреждения. Например, на фоне сахарного диабета развивается диабетическая стопа: образуются язвы, значительно снижающие качество жизни пациентов. Гидрогель на основе гиалуроновой кислоты с секретомом МСК многообещающе ускоряет ангиогенез и регенерацию хронической раны, но пока только у мышей [86].
В 2020 году начались клинические испытания секретома апоптотических PBMC для лечения диабетической стопы. Препарат в составе гидрогеля не вызвал побочных эффектов — ждем публикации исследований эффективности [87]. - Патологии сердца. Сердечная недостаточность — одна из самых частых причин смертности населения, потому что регенеративный потенциал миокарда не позволяет полностью восстановиться после инфекции или инфаркта. Может ли секретом стать альтернативой пересадке сердца и кардиостимулятору?
Подвижки есть — например, у крыс секретом МСК, прекондиционированных гипоксией, снижает площадь инфаркта. Он стимулирует выживание и пролиферацию кардиомиоцитов, ангиогенез, предотвращает образование фиброзного рубца и снижает воспаление [88].
В 2023 году первый пациент с дилатационной кардиомиопатией прошел терапию секретомом прогениторных СК сердца. Спустя полгода внутривенного введения препарата иммунного ответа на компоненты не появилось, а фракция сердечного выброса (доля крови, которое сердце выбрасывает за минуту, от общего объема) выросла на 7% [89]. - Патологии ЦНС. Регенерация в пределах ЦНС у человека довольно ограничена, а заболеваний, которые вызывают смерть нервных клеток, немало [90]. Секретом МСК неплохо показал себя в животных моделях болезни Альцгеймера и Паркинсона, хореи Хантингтона, инсульта и травмы спинного мозга.
В случае нейродегенерации один из интересных механизмов действия секретома — протеиназы на мембране экзосом, которые могут расщеплять бета-амилоид [67]. Сейчас идут клинические испытания экзосом МСК для лечения болезни Альцгеймера (результаты не опубликованы), болезни Паркинсона (исследование планировалось завершить в 2021 году, результатов всё еще нет) и инсульта (набираются участники), в том числе в РФ разрабатывается препарат на основе секретома МСК для лечения геморрагического инсульта [91]. - Патологии репродуктивной системы. Мужское бесплодие — частая причина неспособности пар завести детей, и его терапия всё еще недостаточно развита. В МГУ сейчас проходят клинические испытания биологического лекарственного препарата «МедиРег», разработанного в Центре регенеративной медицины МНОИ МГУ на основе секретома МСК человека. В экспериментах на грызунах препарат оказался настолько же эффективен в восстановлении ткани семенников и сперматогенеза, как и МСК, стимулируя регенерацию ниши сперматогониальных стволовых клеток и предотвращая фиброз [92].
Видно, что бесклеточная терапия с использованием секретома отнюдь не идет семимильными шагами к массовому применению в медицине. Сейчас эта область находится на стадии исследований, и продвинуться дальше ей мешают проблемы, которые мы разберем в следующем разделе. Но пока обратимся к истории развития отечественной бесклеточной терапии. По ряду причин достижения отечественной науки в прошлом веке часто оставались неизвестными для международной аудитории, из-за чего происходила параллелизация научного прогресса в Советском Союзе и западных странах. Так, например, терапия секретомом в нашей стране имеет долгую и поучительную историю, начатую еще учеными из СССР.
Преимущества и недостатки терапии секретомом — за и против
Предыдущий раздел мог навеять на вас тоску. Давайте сменим тон и поговорим сначала, почему вообще люди берутся за разработку методов бесклеточной терапии? Почему не ограничиться однокомпонентными препаратами или клетками?
Чем хороша бесклеточная терапия
Секретом обладает большим преимуществом — это более физиологичное решение по сравнению с однокомпонентными препаратами, ведь говорить с клетками на их языке заманчивее, чем пытаться чего-то добиться одной молекулой-командой, а морфогенез — формирование ткани взамен поврежденной — в принципе требует скоординированного запуска многих процессов под действием комплекса сигналов. Более того, исследования подтверждают, что это может быть более эффективно. Например, одобренный FDA Regnarex (гидрогель, содержащий PDGF) уступает секретомному аналогу в заживлении диабетической язвы (естественно, в животной модели) [38].
А как насчет стволовых клеток? До недавнего времени считалось, что терапевтические свойства СК как продукта для клеточной терапии определяются их участием в замещении поврежденной ткани, но многие эксперименты говорят скорее об их посреднической роли, а всё больше ученых придерживается так называемой «паракринной гипотезы». Ее можно распространять и на МСК, так как эти клетки как раз специализируются на формировании подходящего для регенерации микроокружения; однако, несмотря на это, у них есть недостатки, присущие любым клеткам [45], [99].
Помимо паракринной гипотезы, есть еще несколько аргументов в пользу использования секретома для терапии. В отличие от введения клеток, в этом случае нет проблем с плохой выживаемостью при пересадке. Также при системном введении клеточных препаратов большая часть клеток накапливается в тонких капиллярах печени и легких. Потенциальное «застревание» клеток в сосудах чревато ишемией и тромбообразованием [24], [100].
Видно, что сильные стороны у секретома есть, однако теперь пора резюмировать проблемы, из-за которых бесклеточные технологии никак не могут выйти на рынок.
Недостатки бесклеточной терапии
Существует бутылочное горлышко, через которое новым методам и препаратам в медицине нужно пройти для применения на практике. Продукту нужно иметь постоянный состав, известный механизм действия, определенную динамику концентрации и локализации в организме. Та же проблема у фаговой терапии [101]. Вирусы, заражающие бактерий [102], могли бы стать подспорьем в борьбе с антибиотикорезистентностью [103] — антимикробный потенциал фагов разглядели более века назад. Но одобренных FDA фаговых препаратов до сих пор нет. Проблема в сложном их составе, непонятном поведении в организме и плохой масштабируемости. По схожим причинам схлопывается огромный потенциал секретома — давайте разбираться.
- Отсутствие стандартных методов производства. Свойства секретома зависят от типа клеток, возраста, пола и анамнеза донора, а также условий культивирования. Факторов много, а единой методики производства — нет. В результате не только у разных научных групп получается разный секретом, но и от одной партии к другой состав белковой и везикулярной фракции варьирует.
- Сложный состав секретома. Клетки — капризные работники, и иногда сложно понять, что повлияет на набор вырабатываемых факторов. Для этого нужно в процессе получения секретома оценивать его состав, а это недешево.
- Не до конца ясен механизм действия. Каждый из множества эффектов секретома, важных для регенеративной терапии, — результат работы сложной сигнальной конструкции. Учитывая изменчивость состава и неполную изученность факторов, однозначно сказать, как работает тот или иной секретом и оценить его эффективность затруднительно.
- Проблемы регулирования. Пока не установлено единого свода протоколов для производства препаратов на основе секретома, хотя формально они и относятся к биологическим лекарственным препаратам, регуляторные правила для которых есть. Кроме того, пока недостаточно научных данных для досконального описания механизмов действия таких препаратов, поэтому законодательно регулировать эту область очень сложно.
- Проблемы масштабирования. Процесс получения секретома — долгий и сложный. Из-за «чувствительности» клеток, изменчивости состава и небольшого выхода его постановка «на конвейер» сопряжена с немалыми денежными затратами.
Еще нужно принимать во внимание короткое время жизни препарата. Белковые факторы и везикулы быстро разрушаются и выводятся из кровотока, и поэтому нужно применять специализированные методы доставки: микрочастицы, гидрогели и так далее. Это значит — усложнять процесс разработки, производства и дозировки препарата. Кроме того, пока у нас не будет исчерпывающего понимания сигнальных путей, которые секретом запускает, мы не сможем предсказать точно его побочные эффекты. Все эти проблемы, конечно, обсуждаются учеными и разработчиками, и предложены их частичные решения, однако требуются серьезные исследования и разработка технологических ноу-хау, которые позволят ускорить трансляцию таких продуктов в клиническую практику.
Заключение
Искусство подражает жизни: это, конечно, касается и медицины, особенно регенеративной. Действительно, ее цель — раскрыть потенциал организма, сделать его более гибким, задействовать скрытые пути восстановления тканей и органов. Наша физиология строится на коммуникации клеток и их слаженной работе; и, хотя пройден уже долгий путь, мы только начинаем вслушиваться в это многоголосие. Мы уже понимаем красоту и сложность музыки молекул и клеток, но пока можем только подражать ей, пытаться повторить «на слух». Еще во многом предстоит разобраться, прежде чем мы сможем сами взять в руки дирижерскую палочку.
Бесклеточная терапия с использованием секретома клеток — очень интересная область, но при этом очень сложная. Разрыв между теорией и практикой огромен, однако даже если полный потенциал этого метода не будет реализован, мы получим ценный опыт, который сможем применить впоследствии для развития регенеративной медицины.
Литература
- Не можешь излечить — восстанови! Как появилась регенеративная медицина и какие у нее возможности сегодня;
- Тканевая инженерия и что она может предложить сегодня;
- Клеточные технологии в регенеративной медицине;
- Опухолевые разговоры, или Роль микроокружения в развитии рака;
- Harold Tjalsma, Albert Bolhuis, Jan D. H. Jongbloed, Sierd Bron, Jan Maarten van Dijl. (2000). Signal Peptide-Dependent Protein Transport in Bacillus subtilis : a Genome-Based Survey of the Secretome. Microbiol Mol Biol Rev. 64, 515-547;
- «Омики» — эпоха большой биологии;
- Что такое внеклеточный матрикс и почему его все изучают;
- Gina D. Kusuma, James Carthew, Rebecca Lim, Jessica E. Frith. (2017). Effect of the Microenvironment on Mesenchymal Stem Cell Paracrine Signaling: Opportunities to Engineer the Therapeutic Effect. Stem Cells and Development. 26, 617-631;
- Экзосомы: научная альтернатива сказочным молодильным яблокам;
- Stone W. L., Leavitt L., Varacallo M. A. (2023). Physiology, Growth Factor. Treasure Island: StatPearls.;
- Enkhhsaikhan Lkhagvasuren. (2017). Janeway’s Immunobiology, 9th Edition. Cent. Asian j. Med. Sci.. 3, 100-101;
- Mübeccel Akdis, Simone Burgler, Reto Crameri, Thomas Eiwegger, Hiroyuki Fujita, et. al.. (2011). Interleukins, from 1 to 37, and interferon-γ: Receptors, functions, and roles in diseases. Journal of Allergy and Clinical Immunology. 127, 701-721.e70;
- David Wallach. (2018). The Tumor Necrosis Factor Family: Family Conventions and Private Idiosyncrasies. Cold Spring Harb Perspect Biol. 10, a028431;
- Catherine E. Hughes, Robert J. B. Nibbs. (2018). A guide to chemokines and their receptors. The FEBS Journal. 285, 2944-2971;
- Pilar López-Cotarelo, Carolina Gómez-Moreira, Olga Criado-García, Lucas Sánchez, José Luis Rodríguez-Fernández. (2017). Beyond Chemoattraction: Multifunctionality of Chemokine Receptors in Leukocytes. Trends in Immunology. 38, 927-941;
- Julie W. Cheng, Zhina Sadeghi, Alan D. Levine, Marc S. Penn, Horst A. von Recum, et. al.. (2014). The role of CXCL12 and CCL7 chemokines in immune regulation, embryonic development, and tissue regeneration. Cytokine. 69, 277-283;
- Anna Dimberg. (2010). Chemokines in Angiogenesis. Current Topics in Microbiology and Immunology. 59-80;
- Natalia Kalinina, Daria Kharlampieva, Marina Loguinova, Ivan Butenko, Olga Pobeguts, et. al.. (2015). Characterization of secretomes provides evidence for adipose-derived mesenchymal stromal cells subtypes. Stem Cell Res Ther. 6;
- Georgy D. Sagaradze, Nataliya A. Basalova, Anastasia Yu. Efimenko, Vsevolod A. Tkachuk. (2020). Mesenchymal Stromal Cells as Critical Contributors to Tissue Regeneration. Front. Cell Dev. Biol.. 8;
- Helena Kupcova Skalnikova. (2013). Proteomic techniques for characterisation of mesenchymal stem cell secretome. Biochimie. 95, 2196-2211;
- A. Sainio, H. Järveläinen. (2020). Extracellular matrix-cell interactions: Focus on therapeutic applications. Cellular Signalling. 66, 109487;
- Е.С. Новоселецкая, О.А. Григорьева, А.Ю. Ефименко, Н.И. Калинина. (2019). ВНЕКЛЕТОЧНЫЙ МАТРИКС В РЕГУЛЯЦИИ ДИФФЕРЕНЦИРОВКИ СТВОЛОВЫХ КЛЕТОК. БМ. 84, 343-353;
- Matthias Mack, Andrea Kleinschmidt, Hilke Brühl, Christiane Klier, Peter J. Nelson, et. al.. (2000). Transfer of the chemokine receptor CCR5 between cells by membrane-derived microparticles: A mechanism for cellular human immunodeficiency virus 1 infection. Nat Med. 6, 769-775;
- Samir EL Andaloussi, Imre Mäger, Xandra O. Breakefield, Matthew J. A. Wood. (2013). Extracellular vesicles: biology and emerging therapeutic opportunities. Nat Rev Drug Discov. 12, 347-357;
- Masayuki Shimoda, Rama Khokha. (2013). Proteolytic factors in exosomes. Proteomics. 13, 1624-1636;
- R.G. Parton. (2016). Clathrin Independent Endocytosis. Encyclopedia of Cell Biology. 394-400;
- Обо всех РНК на свете, больших и малых;
- Jordan Fyfe, Ilaria Casari, Marcello Manfredi, Marco Falasca. (2023). Role of lipid signalling in extracellular vesicles-mediated cell-to-cell communication. Cytokine & Growth Factor Reviews. 73, 20-26;
- Ana Marote, Fábio G. Teixeira, Bárbara Mendes-Pinheiro, António J. Salgado. (2016). MSCs-Derived Exosomes: Cell-Secreted Nanovesicles with Regenerative Potential. Front. Pharmacol.. 7;
- Francisco Vizoso, Noemi Eiro, Sandra Cid, Jose Schneider, Roman Perez-Fernandez. (2017). Mesenchymal Stem Cell Secretome: Toward Cell-Free Therapeutic Strategies in Regenerative Medicine. IJMS. 18, 1852;
- Basalova Nataliya, Arbatskiy Mikhail, Popov Vladimir, Grigorieva Olga, Vigovskiy Maksim, et. al.. (2023). Mesenchymal stromal cells facilitate resolution of pulmonary fibrosis by miR-29c and miR-129 intercellular transfer. Exp Mol Med. 55, 1399-1412;
- Lianbo Shao, Yu Zhang, Beibei Lan, Juanjuan Wang, Zhiwei Zhang, et. al.. (2017). MiRNA-Sequence Indicates That Mesenchymal Stem Cells and Exosomes Have Similar Mechanism to Enhance Cardiac Repair. BioMed Research International. 2017, 1-9;
- Кодирующие некодирующие РНК;
- Arnold I. Caplan. (2017). Mesenchymal Stem Cells: Time to Change the Name!. Stem Cells Translational Medicine. 6, 1445-1451;
- Такие разные стволовые клетки;
- Лаборатория стволовых клеток мозга: мир новых нервных клеток у взрослых животных;
- Vasily A. Kudinov, Rafael I. Artyushev, Irina M. Zurina, Roman D. Lapshin, Ludmila B. Snopova, et. al.. (2021). Antimicrobial and Regenerative Effects of Placental Multipotent Mesenchymal Stromal Cell Secretome-Based Chitosan Gel on Infected Burns in Rats. Pharmaceuticals. 14, 1263;
- Greg Maguire. (2013). Stem cell therapy without the cells. Communicative & Integrative Biology. 6, e26631;
- Alberto González-González, Daniel García-Sánchez, Monica Dotta, José C Rodríguez-Rey, Flor M Pérez-Campo. (2020). Mesenchymal stem cells secretome: The cornerstone of cell-free regenerative medicine. WJSC. 12, 1529-1552;
- F. Weber. (2014). Antiviral Innate Immunity: Introduction☆. Reference Module in Biomedical Sciences;
- Ewa M. Kościuczuk, Paweł Lisowski, Justyna Jarczak, Nina Strzałkowska, Artur Jóźwik, et. al.. (2012). Cathelicidins: family of antimicrobial peptides. A review. Mol Biol Rep. 39, 10957-10970;
- Saeeda Al Jaberi, Athena Cohen, Crystal D’Souza, Yousef M. Abdulrazzaq, Shreesh Ojha, et. al.. (2021). Lipocalin-2: Structure, function, distribution and role in metabolic disorders. Biomedicine & Pharmacotherapy. 142, 112002;
- Anthony L. Mescher, Anton W. Neff, Michael W. King. (2017). Inflammation and immunity in organ regeneration. Developmental & Comparative Immunology. 66, 98-110;
- Антимикробные пептиды — возможная альтернатива традиционным антибиотикам;
- Catarina M. Trigo, Joana S. Rodrigues, Sérgio P. Camões, Susana Solá, Joana P. Miranda. (2024). Mesenchymal stem cell secretome for regenerative medicine: Where do we stand?. Journal of Advanced Research;
- Shuo Gao, Fei Mao, Bin Zhang, Ling Zhang, Xu Zhang, et. al.. (2014). Mouse bone marrow-derived mesenchymal stem cells induce macrophage M2 polarization through the nuclear factor-κB and signal transducer and activator of transcription 3 pathways. Exp Biol Med (Maywood). 239, 366-375;
- Andrew C. Newman, Wayne Chou, Katrina M. Welch-Reardon, Ashley H. Fong, Stephanie A. Popson, et. al.. (2013). Analysis of Stromal Cell Secretomes Reveals a Critical Role for Stromal Cell–Derived Hepatocyte Growth Factor and Fibronectin in Angiogenesis. ATVB. 33, 513-522;
- Bor Luen Tang. (2018). Promoting axonal regeneration through exosomes: An update of recent findings on exosomal PTEN and mTOR modifiers. Brain Research Bulletin. 143, 123-131;
- Апоптоз, или Путь самурая;
- F.J. Vizoso, L.A. Costa, N. Eiro. (2023). New era of mesenchymal stem cell-based medicine: basis, challenges and prospects. Revista Clínica Española (English Edition). 223, 619-628;
- MR Alison, S Islam, S Lim. (2009). Stem cells in liver regeneration, fibrosis and cancer: the good, the bad and the ugly. The Journal of Pathology. 217, 282-298;
- Способ выделения мононуклеаров;
- Rubina Alves, Ramon Grimalt. (2018). A Review of Platelet-Rich Plasma: History, Biology, Mechanism of Action, and Classification. Skin Appendage Disord. 4, 18-24;
- Nazmul Haque, Basri Johan Jeet Abdullah, Noor Hayaty Abu Kasim. (2018). Secretome: Pharmaceuticals for Cell-Free Regenerative Therapy. Stem Cells in Clinical Applications. 17-35;
- Yuriy Petrenko, Irena Vackova, Kristyna Kekulova, Milada Chudickova, Zuzana Koci, et. al.. (2020). A Comparative Analysis of Multipotent Mesenchymal Stromal Cells derived from Different Sources, with a Focus on Neuroregenerative Potential. Sci Rep. 10;
- Sarah Tzu-Feng Hsiao, Azar Asgari, Zerina Lokmic, Rodney Sinclair, Gregory James Dusting, et. al.. (2012). Comparative Analysis of Paracrine Factor Expression in Human Adult Mesenchymal Stem Cells Derived from Bone Marrow, Adipose, and Dermal Tissue. Stem Cells and Development. 21, 2189-2203;
- Georgy Sagaradze, Olga Grigorieva, Peter Nimiritsky, Nataliya Basalova, Natalia Kalinina, et. al.. (2019). Conditioned Medium from Human Mesenchymal Stromal Cells: Towards the Clinical Translation. IJMS. 20, 1656;
- Gina D. Kusuma, James Carthew, Rebecca Lim, Jessica E. Frith. (2017). Effect of the Microenvironment on Mesenchymal Stem Cell Paracrine Signaling: Opportunities to Engineer the Therapeutic Effect. Stem Cells and Development. 26, 617-631;
- Sarah T. Hsiao, Zerina Lokmic, Hitesh Peshavariya, Keren M. Abberton, Gregory J. Dusting, et. al.. (2013). Hypoxic Conditioning Enhances the Angiogenic Paracrine Activity of Human Adipose-Derived Stem Cells. Stem Cells and Development. 22, 1614-1623;
- Shipin Zhang, Shang Jiunn Chuah, Ruenn Chai Lai, James Hoi Po Hui, Sai Kiang Lim, Wei Seong Toh. (2018). MSC exosomes mediate cartilage repair by enhancing proliferation, attenuating apoptosis and modulating immune reactivity. Biomaterials. 156, 16-27;
- Xuan Zhang, Ming-Gen Hu, Ke Pan, Chong-Hui Li, Rong Liu. (2016). 3D Spheroid Culture Enhances the Expression of Antifibrotic Factors in Human Adipose‐Derived MSCs and Improves Their Therapeutic Effects on Hepatic Fibrosis. Stem Cells International. 2016;
- Лентивирусные векторы: как они стали лучшими векторами для терапии ex vivo;
- «Спутник V» и не только: сказ об аденовирусных вакцинах;
- 12 методов в картинках: генная инженерия. Часть I, историческая;
- 12 методов в картинках: генная инженерия. Часть II: инструменты и техники;
- Sudhir H. Ranganath, Zhixiang Tong, Oren Levy, Keir Martyn, Jeffrey M. Karp, Maneesha S. Inamdar. (2016). Controlled Inhibition of the Mesenchymal Stromal Cell Pro-inflammatory Secretome via Microparticle Engineering. Stem Cell Reports. 6, 926-939;
- Lorella Giovannelli, Elia Bari, Claudio Jommi, Fulvio Tartara, Daniele Armocida, et. al.. (2023). Mesenchymal stem cell secretome and extracellular vesicles for neurodegenerative diseases: Risk-benefit profile and next steps for the market access. Bioactive Materials. 29, 16-35;
- Georgy Sagaradze, Olga Grigorieva, Peter Nimiritsky, Nataliya Basalova, Natalia Kalinina, et. al.. (2019). Conditioned Medium from Human Mesenchymal Stromal Cells: Towards the Clinical Translation. IJMS. 20, 1656;
- Batoul Chouaib, Mandana Haack-Sørensen, Franck Chaubron, Frederic Cuisinier, Pierre-Yves Collart-Dutilleul. (2023). Towards the Standardization of Mesenchymal Stem Cell Secretome-Derived Product Manufacturing for Tissue Regeneration. IJMS. 24, 12594;
- 12 методов в картинках: протеомика;
- Georgy Sagaradze, Anna Monakova, Anastasia Efimenko. (2023). Potency Assays for Mesenchymal Stromal Cell Secretome-Based Products for Tissue Regeneration. IJMS. 24, 9379;
- Jun Ishikawa, Nobunori Takahashi, Takuya Matsumoto, Yutaka Yoshioka, Noriyuki Yamamoto, et. al.. (2016). Factors secreted from dental pulp stem cells show multifaceted benefits for treating experimental rheumatoid arthritis. Bone. 83, 210-219;
- Giuseppina Milano, Vanessa Biemmi, Edoardo Lazzarini, Carolina Balbi, Alessandra Ciullo, et. al.. (2019). Intravenous administration of cardiac progenitor cell-derived exosomes protects against doxorubicin/trastuzumab-induced cardiac toxicity. Cardiovascular Research;
- Georgy Sagaradze, Nataliya Basalova, Vladimir Kirpatovsky, Dmitry Ohobotov, Peter Nimiritsky, et. al.. (2019). A magic kick for regeneration: role of mesenchymal stromal cell secretome in spermatogonial stem cell niche recovery. Stem Cell Res Ther. 10;
- Junnan Tang, Deliang Shen, Thomas George Caranasos, Zegen Wang, Adam C. Vandergriff, et. al.. (2017). Therapeutic microparticles functionalized with biomimetic cardiac stem cell membranes and secretome. Nat Commun. 8;
- Thomas Später, Marisa Assunção, Kwok Keung Lit, Guidong Gong, Xiaoling Wang, et. al.. (2022). Engineering microparticles based on solidified stem cell secretome with an augmented pro-angiogenic factor portfolio for therapeutic angiogenesis. Bioactive Materials. 17, 526-541;
- Junnan Tang, Deliang Shen, Thomas George Caranasos, Zegen Wang, Adam C. Vandergriff, et. al.. (2017). Therapeutic microparticles functionalized with biomimetic cardiac stem cell membranes and secretome. Nat Commun. 8;
- Yoojin Seo, Tiep Tien Nguyen, Su-Jeong Oh, Jee-Heon Jeong, Hyung-Sik Kim. (2023). Formulation of secretome derived from mesenchymal stem cells for inflammatory skin diseases. J. Pharm. Investig.. 53, 235-248;
- Avinash Sanap, Ramesh Bhonde, Avinash Kharat, Supriya Kheur Intranasal Stem Cell Secretome therapy to prevent COVID-19 complications — Authorea, Inc.;
- Abd. Kakhar Umar, Maria Elvina Tresia Butarbutar, Sriwidodo Sriwidodo, Nasrul Wathoni. (2020). <p>Film-Forming Sprays for Topical Drug Delivery</p>. DDDT. Volume 14, 2909-2925;
- Huey Ho Jia, Teng Clayton Chu Jia, Kukumberg Marek, Rufaihah Abdul Jalil. (2024). Therapeutic Implications of Stem Cell Secretome. J Stem Cell Ther Transplant. 8, 029-032;
- Ying-gang Zhu, Xiao-mei Feng, Jason Abbott, Xiao-hui Fang, Qi Hao, et. al.. (2014). Human Mesenchymal Stem Cell Microvesicles for Treatment of Escherichia coli Endotoxin-Induced Acute Lung Injury in Mice. Stem Cells. 32, 116-125;
- Fernanda F. Cruz, Zachary D. Borg, Meagan Goodwin, Dino Sokocevic, Darcy E. Wagner, et. al.. (2015). Systemic Administration of Human Bone Marrow-Derived Mesenchymal Stromal Cell Extracellular Vesicles Ameliorates Aspergillus Hyphal Extract-Induced Allergic Airway Inflammation in Immunocompetent Mice. Stem Cells Translational Medicine. 4, 1302-1316;
- Ying-Gang Zhu, Meng-meng Shi, Antoine Monsel, Cheng-xiang Dai, Xuan Dong, et. al.. (2022). Nebulized exosomes derived from allogenic adipose tissue mesenchymal stromal cells in patients with severe COVID-19: a pilot study. Stem Cell Res Ther. 13;
- Mina Fathi-Kazerooni, Samrand Fattah-Ghazi, Maryam Darzi, Jalil Makarem, Reza Nasiri, et. al.. (2022). Safety and efficacy study of allogeneic human menstrual blood stromal cells secretome to treat severe COVID-19 patients: clinical trial phase I & II. Stem Cell Res Ther. 13;
- Fabio Salvatore Palumbo, Matteo Calligaris, Laura Calzà, Calogero Fiorica, Vito Antonio Baldassarro, et. al.. (2024). Topical application of a hyaluronic acid-based hydrogel integrated with secretome of human mesenchymal stromal cells for diabetic ulcer repair. Regenerative Therapy. 26, 520-532;
- Elisabeth Simader, Denise Traxler, Mohammad Mahdi Kasiri, Helmut Hofbauer, Michael Wolzt, et. al.. (2017). Safety and tolerability of topically administered autologous, apoptotic PBMC secretome (APOSEC) in dermal wounds: a randomized Phase 1 trial (MARSYAS I). Sci Rep. 7;
- Clara Gallina, Valentina Turinetto, Claudia Giachino. (2015). A New Paradigm in Cardiac Regeneration: The Mesenchymal Stem Cell Secretome. Stem Cells International. 2015, 1-10;
- P. Menasché, N. Renault, A. Hagege, T. Puscas, V. Bellamy, et. al.. (2024). FIRST-IN-MAN TREATMENT OF HEART FAILURE BY A CARDIOVASCULAR CELL-DERIVED SECRETOME.. Cytotherapy. 26, S32;
- Нейродегенерации, или Массовые вымирания нейронов;
- Stalik Dzhauari, Nataliya Basalova, Alexandra Primak, Vadim Balabanyan, Anastasia Efimenko, et. al.. (2023). The Secretome of Mesenchymal Stromal Cells in Treating Intracerebral Hemorrhage: The First Step to Bedside. Pharmaceutics. 15, 1608;
- Ефименко А.Ю. Роль мезенхимных стромальных клеток в регуляции ниш тканеспецифичных стволовых клеток: дисс. канд. биол. наук. — Москва, 2024.;
- Kate Da Silva, Pradeep Kumar, Yahya E. Choonara. (2025). The paradigm of stem cell secretome in tissue repair and regeneration: Present and future perspectives. Wound Repair Regeneration. 33;
- Гиляров М. С. Биологический энциклопедический словарь. — 2-е изд., исправл. — М.: «Сов. Энциклопедия», 1986;
- Biology Bulletin of the Academy of Sciences of the USSR. Том 12, выпуски 4–6;
- Ганковская Л. В. (2022). Памяти Леонида Васильевича Ковальчука: творческий путь педагога и ученого (к 85-летию со дня рождения). Иммунология. 1;
- Ковальчук Л.В., Ганковская Л.В. (1999). Локальная иммунокоррекция цитокинами. Аллергол. и клин. иммунол.. 1, 64–71;
- Abd. Kakhar Umar. (2023). Stem Cell’s Secretome Delivery Systems. Adv Pharm Bull. 13, 244-258;
- Halimeh Mobarak, Reza Rahbarghazi, Mahdi Mahdipour. (2023). Stem Cell- and Stem Cell-Free-Based Therapies: Pros and Cons. WKMJ. 65, 88-94;
- George Kolios, Yuben Moodley. (2013). Introduction to Stem Cells and Regenerative Medicine. Respiration. 85, 3-10;
- Бактериофаги в медицине;
- Огромный и загадочный мир бактериофагов;
- Антибиотики и антибиотикорезистентность: от древности до наших дней.







