
От любви к сыру до революции в пивоварении: CRISPR/Cas на службе дрожжей
11 марта 2025
От любви к сыру до революции в пивоварении: CRISPR/Cas на службе дрожжей
- 210
- 0
- 1
Дрожжи, веками служившие основой производства продуктов питания, получают новые возможности благодаря технологиям редактирования генома. Особенно ярко этот прогресс можно проследить в пивоварении, где традиционные штаммы Saccharomyces cerevisiae трансформируются в высокоэффективные производственные платформы с заданными характеристиками.
Рисунок в полном размере.
изображение сгенерировано в Dall-e по промпту автора
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Эра гаражных стартапов, которую когда-то начали IT-предприниматели, получает неожиданное продолжение в мире биотехнологий. Современные биоинженеры, вооружившись технологией редактирования генома CRISPR/Cas9, создают инновационные проекты по модификации пивных дрожжей. В статье мы рассмотрим практическое применение генного редактирования в пищевой промышленности и обсудим, как технология CRISPR меняет наше представление о создании генно-модифицированных продуктов — от пива до ферментированных продуктов.
Конкурс «Био/Мол/Текст»-2024/2025
Эта работа опубликована в номинации «Академия & Бизнес» конкурса «Био/Мол/Текст»-2024/2025.

Генеральный партнер конкурса и партнер номинации — международная инновационная биотехнологическая компания BIOCAD.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Когда я впервые услышал о системе редактирования генома CRISPR/Cas [1], меня, как и многих других, захватили перспективы, которые она открывает в медицине и генетике. Возможность точечного изменения ДНК казалась чем-то из области научной фантастики. Но когда я начал знакомиться ближе с историей этого открытия, особое впечатление на меня произвел один из ученых, внесших свой личный вклад в развитие этой технологии, — Рудольф Баррангу (рис. 1). Он рассказывал, что его интерес к науке был связан с любовью к сыру, и именно эта гастрономическая страсть привела его в мир микробиологии и генетики .
История открытия CRISPR подробно описана в статье «CRISPR-эпопея и ее герои». — Ред.

Рисунок 1. Рудольф Баррангу, апостол CRISPR/Cas.
Баррангу провел девять лет в компании Danisco (впоследствии вошедшей в состав DuPont), где занимался разработкой и исследованием заквасочных культур и пробиотиков. Одной из главных проблем, с которыми сталкивалась пищевая промышленность, были бактериофаги — вирусы, уничтожающие промышленные штаммы молочнокислых бактерий, необходимых для производства йогурта и сыра. По некоторым оценкам, фаговые атаки могли приводить к потере до 50% объемов на отдельных предприятиях.
Чтобы решить эту проблему, Баррангу и его коллеги начали изучать механизмы естественной защиты молочнокислых бактерий, а именно CRISPR (Clustered Regularly Interspaced Short Palindromic Repeats). Эта аббревиатура впервые была предложена в 2002 году голландской исследовательской группой под руководством Рууда Янсенса. В начале 2000-х годов исследователи начали предполагать связь между этими последовательностями и защитой бактерий от вирусов. Практический прорыв в изучении механизма произошел благодаря промышленным микробиологам, работавшим над улучшением штаммов Streptococcus thermophilus.
Группа Филиппа Хорвата первой показала, что устойчивость бактерий к фагам напрямую зависит от количества приобретенных вирусных спейсеров в CRISPR-локусе, причем даже единичные мутации в этих последовательностях могли нарушить защитный механизм. Развивая эти наблюдения, группа Баррангу провела серию элегантных экспериментов, опубликованных в 2007 году в журнале Science (рис. 2) [2]. В этой работе исследователи использовали S. thermophilus как модельный организм, подвергая бактерии воздействию различных фагов. Они обнаружили, что выжившие после инфекции бактерии приобретали новые спейсерные последовательности, точно соответствующие ДНК атаковавших их вирусов. Более того, через серию генетических манипуляций — удаление существующих и добавление новых спейсеров — ученые доказали, что именно эти последовательности определяют специфичность защиты против конкретных фагов. Эксперименты также показали критическую роль Cas-белков: без их активности система CRISPR не могла обеспечить эффективную защиту от повторных инфекций.
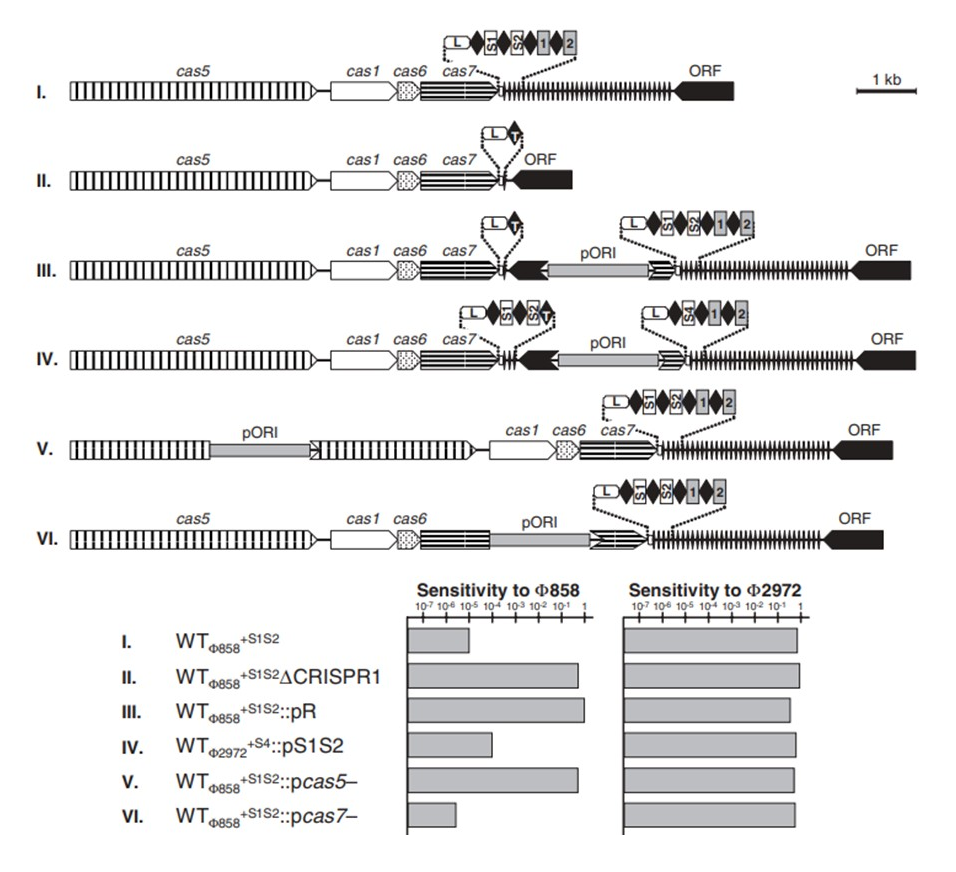
Рисунок 2. Структура CRISPR-Cas системы и чувствительность к бактериофагам. Верхняя часть изображения показывает схемы различных модификаций CRISPR-Cas кассеты, включая кассету с функциональными генами cas5, cas1, cas6, cas7, а также CRISPR-повторные элементы и специфические последовательности (спейсеры). Схемы отражают изменения, внесенные в систему: удаление компонентов, добавление плазмиды с функциональными генами или удаление отдельных генов cas.
К 2010 году уже были описаны основные молекулярные компоненты системы, включая белок Cas9 (изначально известный как Cas5 или Csn1), и была установлена важность PAM-последовательности (proto-spacer adjacent motif) для распознавания мишени.
Хотя группа Баррангу тогда не совершила той революции, которую позже осуществили Дженнифер Дудна и Эммануэль Шарпантье, адаптировавшие эту систему для редактирования генома, их вклад в эту область неоспорим. Команда Баррангу, работая в Danisco, смогла не только подтвердить предположения других ученых о защитной функции CRISPR, но и детально описать молекулярные механизмы этой системы. Их работа, мотивированная любовью к ферментированным продуктам, продвинула науку вперед и заложила основу для новых открытий в области редактирования генома [2].
В настоящее время Рудольф Баррангу продолжает исследования в Университете штата Северная Каролина, где изучает полезные микробы и молочнокислые бактерии, используя методы функциональной геномики.
И мне стало интересно, как эта технология, рожденная из стремления защитить традиционные продукты, возвращается в мир еды и напитков, но уже в новом качестве. Я задумался: какие продукты, полученные с помощью CRISPR, уже доступны на рынке? Как открытие системы редактирования генома может порадовать самого Баррангу в виде улучшенных ферментированных продуктов?
Сразу нужно сказать, что в меню «CRISPR-cuisine» пока не найти принципиально нового сыра. Однако на кухне уже приготовили салат с листьями горчицы, которые, благодаря точечному генному редактированию, утратили характерную остроту. Помимо этого, в ближайшем будущем могут появиться необычные фрукты, такие как «арбузная вишня» или «лимонное яблоко» — и пусть пока это звучит фантастически, в стартапе Pairwise уверены, что вскоре смогут предложить потребителям новые сортовые вариации, где привычные плоды получат особые вкусовые оттенки. Компания из США, основанная в 2017 году, активно работает над созданием новых сельскохозяйственных культур. Их амбициозные проекты направлены на то, чтобы расширить возможности генетического редактирования для более здорового и устойчивого питания [3].
Но новизна вкуса уже сейчас приходит и в мир напитков — причем безо всякой «химии»: генетически модифицированные дрожжи позволяют ощутить самые экзотические фруктовые ноты в обычном пиве.
Революция в пивоварении: дрожжи будущего
Первым на ум приходит именно пиво — напиток, история которого насчитывает тысячи лет. Причем рецепт приготовления пива также не изменился: любому пивовару понадобятся вода, хмель, дрожжи и ячменный солод. Однако современные технологии позволяют переосмыслить даже такие древние традиции. Berkeley Yeast, стартап из Калифорнии, использует технологию CRISPR/Cas9 для создания ГМ-дрожжей, способных придавать пиву вкус тропических фруктов без добавления ароматизаторов или хмеля (рис. 3) [4]. Изначально компания сосредоточилась на разработке дрожжей, которые могли бы синтезировать ароматические соединения, такие как линалоол и гераниол, de novo, то есть «с нуля» — непосредственно в процессе ферментации. De novo биосинтез означает, что клетки дрожжей сами создают необходимые ароматические молекулы из собственных метаболитов, устраняя потребность в хмеле — одном из самых дорогих компонентов пивоварения.
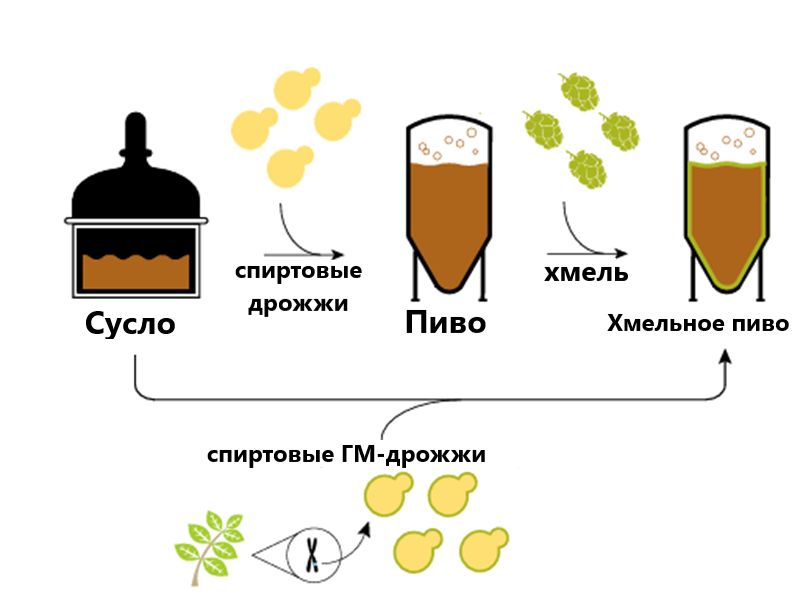
Рисунок 3. Графический абстракт экспериментального подхода.
Для этого в геном промышленных штаммов S. cerevisiae были интегрированы кодирующие последовательности генов монотерпен-синтаз из мяты и базилика, отвечающие за биосинтез ключевых ароматических соединений — линалоола и гераниола. Для достижения оптимального уровня экспрессии каждый ген находился под контролем специально подобранных промоторов, активность которых соответствовала условиям пивоварения. Некоторые промоторы обеспечивали конститутивную экспрессию, в то время как другие реагировали на изменения условий ферментации.
Проект по метаболической инженерии S. cerevisiae оказался непростой задачей. Были протестированы тысячи комбинаций генов, промоторов и регуляторных элементов, но только 5–10% из них оказались успешными. Эти штаммы спиртовых дрожжей, полученные в результате многочисленных экспериментов, могут синтезировать такие ключевые ароматические соединения, как:
- линалоол и гераниол (цветочные и фруктовые ноты),
- гумулен и мирцен (традиционные хмелевые ароматы),
- этиллактат и изоамиловый спирт (фруктовые и кисловатые оттенки).
Для повышения выхода целевых соединений ученые перенастроили метаболизм дрожжей, усилив мевалонатный путь — ключевой процесс для синтеза терпенов. Это перенаправило метаболические потоки на производство линалоола, гераниола и других соединений, делая дрожжи настоящими «биофабриками вкуса» [4].
Однако пивовары и потребители не были готовы полностью отказаться от традиционного хмеля, особенно из-за его уникальных свойств. Например, в хмеле есть альфа- и бета-кислоты, которые придают напитку знакомый вкус горечи. Поняв это, Berkeley Yeast изменила стратегию. Вместо полного отказа от хмеля компания разработала штаммы дрожжей, которые усиливают его ароматические свойства. Это стало возможным, потому что листья хмеля также содержат многочисленные ароматические соединения-предшественники. По сути, это связанные формы молекул, которые сами по себе не имеют никакого запаха. Добавление новых ферментов-участников в процесс биосинтеза позволяет «высвободить» такие молекулы из «заблокированного» состояния. Что и придает пиву желанный и ощутимый вкус. И теперь Berkeley Yeast адаптируют новые ГМ-штаммы под задачу помочь хмелю «благоухать» во всей красе. В пивоваренной индустрии такой подход назвали «биотрансформацией» (рис. 4). В результате пивовары смогли использовать меньше хмеля, сохраняя при этом насыщенный и яркий аромат, что значительно снижает затраты на сырье.
Но главное достижение стартапа — это то, что продукция Berkeley Yeast получила одобрение FDA после того, как компания доказала безопасность своих ГМ-дрожжей. Полное секвенирование генома подтвердило отсутствие непредвиденных мутаций, а также то, что дрожжи размножаются только асексуально (почкованием). Все компоненты и биомолекулы, полученные в процессе ферментации, хорошо изучены и широко применяются в пищевой промышленности. Это нетривиальный факт, потому что, опираясь на недавнее исследование по созданию штаммов дрожжей для биосинтеза псилоцибина (психоактивного соединения из «магических грибов», изучаемого для лечения депрессии), можно увидеть, насколько это важно. В той работе сотрудники Датского Технического университета пытались воссоздать биосинтетический путь из грибов Psilocybe cubensis в дрожжах S. cerevisiae. При введении одного из генов — фермента BtAANAT — дрожжи неожиданно начали производить совершенно новое, ранее неизвестное в природе соединение N-ацетил-4-гидрокситриптамин. Это произошло из-за того, что фермент, который в природе присоединяет ацетильную группу к серотонину, проявил неожиданную субстратную неспецифичность и начал работать с другой похожей молекулой — 4-гидрокситриптамином [5].
В случае пивных дрожжей Berkeley Yeast такая ситуация была бы неприемлема — появление новых, неизученных соединений автоматически закрыло бы путь к одобрению FDA. Именно поэтому компания тщательно подбирала гены только тех ферментов, которые производят хорошо известные ароматические соединения, уже присутствующие в пищевых продуктах. Более того, все метаболические пути были настроены таким образом, чтобы ферменты работали строго специфично, без образования побочных продуктов. Таким образом, успех Berkeley Yeast в получении одобрения FDA базируется не только на отсутствии генетических отклонений у самих дрожжей, но и на предсказуемости и изученности всех производимых ими соединений.
Результатом долгой и кропотливой работы стало создание нескольких линеек препаратов жидких дрожжей, уже доступных для заказа на сайте компании:
- Tropics™ — ГМ-дрожжи, специально созданные для биосинтеза соединений, характерных для тропических фруктов, таких как гуайява и маракуйя. Эти штаммы формируют ароматический профиль, напоминающий популярные сорта хмеля Citra, Galaxy и Mosaic. Это позволяет пивоварам использовать более доступные сорта хмеля или сокращать его количество, при этом сохраняя насыщенный вкус и аромат пива.
- Thiolized Yeasts — штаммы, экспрессирующие ферменты, способные высвобождать тиолы из хмеля, усиливая их ароматические свойства. Эта технология позволяет достичь яркого и интенсивного хмелевого аромата при меньшем расходе хмеля, что также снижает затраты на растительное сырье.
- Galactic™ — штамм ГМ-дрожжей, которые одновременно производят молочную кислоту и этанол в процессе ферментации. Эти штаммы упрощают производство кислых сортов пива (Sour), устраняя необходимость в дополнительных этапах подкисления, что делает процесс более экономичным и эффективным.
- NA Series — специализированные штаммы для производства безалкогольного пива, сохраняющие полноценный вкус традиционного напитка. В отличие от классических методов производства безалкогольного пива, где удаление спирта путем выпаривания приводит к потере летучих ароматических соединений, эти дрожжи модифицированы таким образом, что производят минимальное количество этанола при сохранении способности синтезировать ключевые ароматические соединения в процессе ферментации.

Рисунок 4. Сотрудники компании Berkeley Yeast за работой.
Интересно, что продукт стартапа быстро нашел своего покупателя в лице крафтовых пивоварен. Эти небольшие предприятия представляют собой активное сообщество, которое отлично понимает, чего оно хочет от ГМ-дрожжей. Каждая нотка вкуса — будь то персик, дыня или ананас — степень кислотности или устойчивость штамма к температурным режимам, все это становится предметом тщательной настройки. Запросы от крафтовых пивоварен только подталкивают научный прогресс в области изучения ГМ-дрожжей. Промышленные гиганты пока присматриваются к возможности варить классическое пиво с хмельным вкусом без добавления хмеля. Имена компаний, которые первыми начали сотрудничать со стартапом из Беркли, пока не раскрываются. Но, учитывая успешный опыт небольших пивоварен, можно предположить, что и они вскоре адаптируют свою рецептуру под ГМ-дрожжи.
Загадка мутности пива: генетическая детективная история
Представьте два бокала пива. В одном напиток прозрачный, как янтарное стекло, в другом — густой и мутный, словно фруктовый сок (рис. 5). Чем объясняется эта разница, если рецепты приготовления идентичны? Этот вопрос заинтересовал доктора Лауру Бернс, директора по исследованиям и разработкам чикагской компании Omega Yeast. В разгар популярности «сочных или мутных» IPA (India pale ale) в США и Великобритании ее команда начала систематическое исследование этого феномена.
«Всё началось с простого эксперимента по имитации ферментации IPA, — вспоминает доктор Бернс, — Мы заметили, что определенные штаммы дрожжей создавали мутность, в то время как другие — нет. Это было удивительно, ведь вся индустрия крафтового пива фокусировалась на роли солода и хмеля в создании мутности».
Команда Omega Yeast проводила эксперимент за экспериментом, варьируя рецептуры и время внесения сухого хмеля. Результаты были неизменны: образцы, которые становились мутными, всегда были связаны с определенной группой штаммов дрожжей, которую исследователи назвали haze-positive (положительными по мутности).
Полный анализ генома дрожжей показал, что ген HZY1 связан с производством мутности. Он кодирует маннопротеин — белок клеточной стенки дрожжей, который, подобно липкой сети, захватывает и удерживает частицы в пиве. Используя CRISPR/Cas9, ученые удалили этот ген в мутных штаммах, и пиво стало прозрачным, сохранив свои вкусовые характеристики [6].

Рисунок 5. На фото показаны два бокала пива, демонстрирующие разницу в мутности из-за наличия или отсутствия гена HZY1 в дрожжах. Слева пиво, полученное с использованием дрожжей дикого типа (WT), имеет характерную мутность благодаря маннопротеину, который удерживает частицы в суспензии. Справа: пиво, произведенное с использованием мутантных дрожжей (hzy1Δ) без гена HZY1, прозрачное, так как частицы оседают из-за отсутствия маннопротеина.
Эти исследования заложили основу для нового подхода в пивоварении. Если раньше главной задачей было устранение мутности для создания прозрачных сортов пива, то сегодня предпочтения потребителей изменились. Мутные IPA ассоциируются с «натуральностью», насыщенным вкусом и качеством, что делает их особенно популярными среди любителей нефильтрованных напитков.
Неудивительно, что эта работа в области генетики дрожжей быстро нашла коммерческое применение. Omega Yeast запатентовала свой генно-инженерный подход под брендом Lumina™ Technology и получила свой первый дрожжевой ГМ-штамм DayBreak-V. Компания создала его на основе British Ale V — одного из самых популярных штаммов для производства Hazy IPA. Так DayBreak-V примечателен своей способностью сочетать, казалось бы, противоположные характеристики: он позволяет получать прозрачное пиво в стиле West Coast IPA, сохраняя при этом насыщенный фруктовый профиль, за который ценят мутные NEIPA (New England IPA). Прозрачности конечного продукта способствует и еще одно важное свойство штамма — умеренная флокуляция, то есть способность дрожжевых клеток собираться в группы и оседать после завершения ферментации.
Важно отметить, что правовой статус Lumina™ Technology имеет свои особенности. При создании DayBreak-V использовалось точечное редактирование генома методом CRISPR/Cas9, которое лишь удаляет существующий ген без внесения чужеродной ДНК и минимально влияет на природный состав дрожжей. Поэтому по законодательству США такие изменения не попадают под классификацию ГМО. Это открывает широкие возможности для продаж на американском рынке. Однако в Европейском Союзе и Великобритании любое генетическое редактирование в пивоварении остается под запретом, что ограничивает географическую экспансию продукта.
История развития технологии показывает неоднозначность внедрения биотехнологий в традиционные производства. С одной стороны, компания успешно прошла путь от научного открытия до коммерческого продукта: защитила интеллектуальную собственность, учла особенности законодательства и создала решение, отвечающее запросам индустрии. С другой — сохраняется скептицизм профессионального сообщества относительно необходимости таких инноваций в пивоварении, где традиционные методы успешно применяются столетиями.
Однако Omega Yeast не останавливается на достигнутом. Компания активно развивает свою технологию, исследуя новые возможности ее применения. Например, комбинация Lumina с технологией DKO (Diacetyl Knock Out) открывает перспективы одновременного контроля мутности и нежелательных вкусовых компонентов. DKO предотвращает образование диацетила — соединения, придающего пиву нежелательный масляный привкус, что особенно важно для промышленного производства. Такой комплексный подход к инновациям демонстрирует, как современные биотехнологии могут не только решать отдельные задачи, но и создавать интегрированные решения для улучшения качества пива.
Природа против инженерии: два пути к инновациям
Berkeley Yeast, создавая дрожжи с помощью CRISPR, делает ставку на инженерный подход. Однако канадская компания Lallemand, один из крупнейших мировых производителей микроорганизмов для пищевой промышленности, демонстрирует, как можно успешно балансировать между передовыми биотехнологиями и поиском готовых решений.
В 2018 году Lallemand представила первый в пивоваренной отрасли коммерческий генетически модифицированный штамм Saccharomyces cerevisiae, известный как Sourvisiae® (рис. 6). С помощью встройки гена лактат-дегидрогеназы, заимствованного из пищевых микроорганизмов, этот модельный штамм стал способен одновременно синтезировать молочную кислоту и этанол во время ферментации. Это решение позволило пивоварам создавать кислое пиво в один этап вместо традиционного процесса, требующего внесения бактерий, таких как Lactobacillus. Казалось бы, задача решена: процесс эффективен, результат предсказуем.
Но природа преподнесла сюрприз. Во время обычной практики студенты Университета Филадельфии проводили сбор микробиологических образцов. На территории кампуса, где регулярно применялись фунгициды, поиски оказались безуспешными. И тогда команда отправилась на соседствующее с кампусом кладбище, где уже на коре дерева (это был кизил) обнаружила уникальный вид дрожжей Lachancea thermotolerans, или GY7B.
После посева на селективную среду и инкубации они обнаружили необычную колонию. При последующем культивировании в жидкой среде изолят проявил неожиданные свойства — активное образование молочной кислоты, что характерно для бактерий, но не для дрожжей. Это первоначально заставило исследователей заподозрить контаминацию молочнокислыми бактериями. Однако микроскопия и молекулярно-генетический анализ подтвердили, что выделенный штамм GY7B является чистой культурой дрожжей с уникальными метаболическими характеристиками.
Вид GY7B, выделенный студентами Университета Филадельфии, оказался настоящим прорывом в производстве кислых сортов пива. В первые 3–5 дней ферментации GY7B активно производит молочную кислоту, а к 7–14 дням завершает сбраживание сахаров, формируя нужный баланс кислотности и алкоголя. Эти уникальные свойства привлекли внимание доктора Мэтта Фаббера, специалиста в области пивоварения, который взял на себя дальнейшее руководство по исследованию этого нового вида.
Чтобы оценить потенциал GY7B в реальных условиях, доктор Фаббер наладил сотрудничество с канадской компанией Lallemand, известной своими инновациями в области пивоваренных и винодельческих дрожжей. Под руководством Фаббера и при поддержке Lallemand штамм прошел пилотные испытания в промышленных условиях, где подтвердил свои впечатляющие результаты: устойчивость к низкому pH и высоким концентрациям этанола, способность работать с суслом высокой плотности. Особенно важно, что процесс ферментации оказался легко масштабируемым — кислотность можно регулировать простым изменением концентрации глюкозы и количества дрожжей, без необходимости сложного контроля аэрации. Учитывая результаты, Lallemand решила вывести штамм на рынок под брендом WildBrew™ Philly Sour, подчеркивая его природное происхождение. Это стало стратегически верным решением: многие потребители и пивовары, особенно в Европе, настороженно относятся к ГМО, но с энтузиазмом принимают природные штаммы.
История GY7B и Sourvisiae® поднимает интересный вопрос: что эффективнее — долгий поиск природных штаммов или целенаправленная генетическая модификация? Чтобы ответить на него, стоит обратиться к быстрорастущему сегменту безалкогольного пива, где эта конкуренция проявляется особенно ярко.
С одной стороны, упомянутая ранее NA Series от Berkeley Yeast демонстрирует возможности генной инженерии. Эти штаммы специально сконструированы для минимального производства этанола при сохранении способности синтезировать ключевые ароматические соединения. С другой стороны, NEER® Poly и NEER® Punch от Chr. Hansen показывают альтернативный путь: эти штаммы принадлежат к роду Pichia, принципиально отличающемуся от традиционных пивоваренных дрожжей Saccharomyces. Изначально разработанные для виноделия, они успешно перешли в пивоварение благодаря уникальной способности ограниченно метаболизировать сахара. Это позволяет сократить расход солода на 65%, уменьшить потребление воды и снизить углеродный след. Важно, что эти дрожжи позволяют избежать энергоемкой стадии удаления алкоголя, обеспечивая при этом широкую палитру вкусов — от классической чистоты лагеров до яркой фруктовости IPA. При ежегодном росте рынка безалкогольного пива на 5–7%, такая конкуренция между природными и ГМ-штаммами стимулирует развитие обоих направлений, расширяя инструментарий современного пивоварения.

Рисунок 6. ГМО против натурального штамма. Слева: ГМ-дрожжи Sourvisiae® от Mascoma Corporation: инновационное решение для получения молочной кислоты во время первичной ферментации. Справа: как мог выглядеть кизил, расположенный на кладбище, где был найден уникальный штамм дрожжей Lachancea thermotolerans, способный производить молочную кислоту.
Подведем итог: у каждого подхода — поиска природных штаммов и генной модификации — есть свои преимущества. Первый дает неожиданно богатые результаты и способствует разработке оригинальных вкусов, второй — более предсказуем и позволяет быстрее получить желаемые характеристики. Важнее всего становится способность пивоварен грамотно адаптировать существующие решения под все более разнообразные группы потребителей.
Комбуча: вызовы и перспективы
Успех генетически модифицированных дрожжей в пивоварении заставляет задуматься: а можно ли применить подобный подход к другим ферментированным напиткам? Особенно интересен случай комбучи (чайного гриба) — популярного напитка, который многие помнят еще с советских времён. В теории, используя технологии редактирования генома, можно было бы создать версию с меньшей кислотностью или даже со вкусом колы.
Однако исследователи столкнулись с неожиданными сложностями. В отличие от чистой культуры пивных дрожжей, комбуча представляет собой сложное сообщество разных микроорганизмов. SCOBY (Symbiotic Culture of Bacteria and Yeasts) — это симбиоз различных видов бактерий и дрожжей. Основные участники этого «микробного оркестра» — уксуснокислые бактерии родов Acetobacter и Komagataeibacter, отвечающие за производство уксусной кислоты и целлюлозной плёнки; дрожжи рода Dekkera, производящие этанол и сложные эфиры, влияющие на аромат (при этом содержание этанола в готовой комбуче остается минимальным); а также другие микроорганизмы, такие как бактерии Bacillus, производящие молочную кислоту [7].
Эта сложная экосистема делает генетическую модификацию комбучи гораздо более трудной задачей, чем работу с чистыми культурами дрожжей. Каждому виду в SCOBY нужно обеспечить стабильность и совместимость с другими участниками симбиоза, что технически крайне сложно.
Тем не менее, ученые не оставляют попыток найти новые применения комбучи. Мы привыкли думать о чайном грибе как об освежающем напитке — полезном, но в то же время простом в своей сущности. Кто-то добавляет в комбучу новые вкусы, кто-то экспериментирует с ингредиентами. Но ученые из MIT и Imperial College London доказали, что этот привычный напиток скрывает гораздо больший потенциал: он может стать основой для создания биоматериалов. А именно — целлюлозной матрицы, материала с огромным потенциалом в медицине, экологии и промышленности.
Природные штаммы бактерий, такие как Komagataeibacter rhaeticus, уже давно известны своей способностью синтезировать бактериальную целлюлозу, состоящую из ультратонких волокон толщиной около 50 нанометров и длиной до 9 микрометров, которые формируют плотную и прочную структуру. Однако в рамках проекта Syn-SCOBY ученые разработали усовершенствованную версию симбиотической культуры, объединяющую генетически модифицированные дрожжи Saccharomyces cerevisiae и природные бактерии K. rhaeticus. Бактерии продолжают эффективно производить целлюлозу, которая служит основой материала, в то время как модифицированные дрожжи обеспечивают программируемые функции.
Эта синтетическая комбинация демонстрирует значительные преимущества перед природными аналогами. Syn-SCOBY растет быстрее, формируя толстые слои целлюлозы за считанные дни при комнатной температуре, достигая выработки более 10 граммов на литр (рис. 7). При этом структура получаемого материала обладает исключительными механическими свойствами. Такой материал также отличается высокой пористостью, способностью удерживать воду и очень большой площадью поверхности.
Особенно интересной особенностью Syn-SCOBY стала возможность создания «живых» материалов с программируемыми функциями. Ученые модифицировали дрожжи так, чтобы они реагировали на свет и другие внешние сигналы. Например, под воздействием света специальные гены активируют синтез люминесцентных белков, что позволяет материалу «запоминать» световые паттерны подобно биологической фотопленке. Это открывает возможности для создания биосенсоров и интерактивных биологических интерфейсов.
Разработанная технология позволяет получать целлюлозу с заданными свойствами, которую можно использовать для создания широкого спектра продуктов — от медицинских повязок с контролируемым высвобождением лекарств до биоразлагаемых упаковочных материалов и фильтров для воды.

Рисунок 7. Процесс извлечения листа бактериальной целлюлозы из питательной среды. Этот прочный и биосовместимый материал, синтезируемый бактериями, используется в медицине, пищевой промышленности и для создания экологичных упаковок.
Photo credit: Kertu Tenso
Исследователи полагают, что технология создания таких материалов будет работать даже в домашних условиях. Как отметил один из исследователей, Tzu-Chieh Tang, «выращивание Syn-SCOBY ничем не сложнее, чем приготовление обычной комбучи на кухне». Это значит, что в будущем любой желающий сможет создать на своем столе такие материалы, нужен только сахар, чай для питательных веществ и кусочек Syn-SCOBY. Дальнейшее развитие технологий генного редактирования открывает еще более захватывающие перспективы: появится возможность создавать новые штаммы микроорганизмов для производства целлюлозы с уникальными свойствами, встраивать в материал дополнительные функции или программировать его отклик на различные внешние сигналы. Таким образом, простая банка с чайным грибом вдохновила создание нового поколения умных биоматериалов, которые могут изменить наше будущее [8].
ГМО и потребитель: где грань?
В пищевой промышленности генетически модифицированные микроорганизмы применяются все шире, но с важными ограничениями. Законодательство большинства стран, включая Россию, разрешает генетическую модификацию только определенных видов микроорганизмов. Например, можно модифицировать промышленные штаммы пекарских дрожжей Saccharomyces cerevisiae или плесневого гриба Aspergillus niger, но многие другие виды, такие как Penicillium verruculosum, остаются под запретом для генетических манипуляций в пищевом производстве. Такой осторожный подход к регулированию отражает постепенную эволюцию в восприятии ГМО обществом. Если раньше любое упоминание о ГМО вызывало страх, то сегодня потребители начинают понимать, что продукты жизнедеятельности ГМ-организмов — это не то же самое, что прямое потребление ГМО.
Здесь важно провести тонкую грань. В отличие от ГМ-растений, дрожжи не могут спонтанно распространиться по полям, поскольку находятся в контролируемых условиях на предприятиях. Они размножаются почкованием, и их распространение легко контролировать. Кроме того, продукты, полученные с использованием дрожжей, обычно проходят дополнительные этапы обработки перед попаданием к потребителю. Фильтрация удаляет не только дрожжи, но и другие частицы, влияющие на мутность, обеспечивая прозрачность напитка. Пастеризация увеличивает срок хранения, уничтожая оставшиеся микроорганизмы. Для крафтовых стилей, таких как мутные IPA, возможно сохранение дрожжей в готовом продукте для усиления аромата, текстуры и уникального вкусового профиля. Решение об удалении или сохранении дрожжей зависит от желаемого стиля пива, предпочтений пивовара, и, как мы сейчас наблюдаем — ГМ-статуса микроорганизма.
Параллельно законодательные ограничения приводят к парадоксам. В США, например, можно купить пиво, сваренное с помощью ГМ-дрожжей от Berkeley Yeast. Но использовать эти же дрожжи для производства обогащенного дрожжевого экстракта, аналогичного Marmite (рис. 8), запрещено. Ирония заключается в том, что дрожжевой экстракт, исторически возникший как побочный продукт пивоварения, идеально подходит для внедрения новых технологий. Первоначально Marmite рассматривался как источник белка для рабочих, но со временем продукт завоевал кулинарный мир своим насыщенным «умами» вкусом. Применение ГМ-дрожжей в этом процессе открыло бы целый мир вкусовых и функциональных возможностей. Представьте Marmite с нотками тропических фруктов или усиленным содержанием витаминов группы B. Обычный дрожжевой экстракт не всем придется по вкусу...

Рисунок 8. Традиционно Marmite намазывают на тост с маслом.
Отдельного внимания заслуживает маркировка «не содержит ГМО», которая часто встречается на этикетках в российских магазинах. На первый взгляд она кажется информативной и свидетельствующей о высоком качестве продукта, но при более глубоком рассмотрении становится ясно, что она может искажать реальную ситуацию. Сложность заключается в следующем: хотя в России запрещено выращивание ГМ-культур, импорт более 20 видов генетически модифицированных сортов сельскохозяйственных растений разрешен для использования в пищевом производстве. Например, соевый соус может быть изготовлен из ГМ-сои, а в сыроделии допускается применение ферментов, полученных с помощью генетически модифицированных микроорганизмов.
Эта ситуация отражает важный переходный этап в развитии биотехнологий и их восприятии обществом. От категоричного отрицания ГМО мы движемся к более взвешенному подходу, основанному на понимании сути технологий редактирования генома. В будущем, когда эти технологии станут прозрачнее для общества, а регуляторные механизмы адаптируются к новым возможностям, потребители смогут делать по-настоящему осознанный выбор. Возможно предположить, что вместо упрощенной маркировки «не содержит ГМО» на этикетках появится содержательная информация о конкретных модификациях и их назначении — от улучшения питательных свойств до повышения устойчивости продукта.
Заключение: наука и гастрономия рука об руку
Вернемся к Рудольфу Баррангу. Его любовь к сыру привела к открытию, которое изменило биотехнологию. И теперь, благодаря CRISPR, возможно улучшать качество ферментированных продуктов, изменять метаболизм микроорганизмов и создавать новые вкусовые ощущения. А ведь мир ферментированных продуктов удивительно разнообразен: от привычных йогурта и сметаны до экзотических кимчи и комбучи, от соевого соуса до кефира и различных видов хлеба (чаллы, питы, наан). Каждый из этих продуктов потенциально может быть усовершенствован с помощью CRISPR/Cas — от улучшения их питательных свойств до создания новых вкусовых сочетаний. Возможно, в ближайшем будущем Баррангу сможет буквально вкусить плоды своих исследований, наслаждаясь сыром и вином, созданными с помощью генной инженерии, которые ученый продолжает изучать. Так наука и гастрономия идут друг друга навстречу, делая нашу жизнь ярче и вкуснее.
Литература
- CRISPR-эпопея и ее герои;
- R. Barrangou, C. Fremaux, H. Deveau, M. Richards, P. Boyaval, et. al.. (2007). CRISPR Provides Acquired Resistance Against Viruses in Prokaryotes. Science. 315, 1709-1712;
- Стартап-завтрак, который мы заслужили: фрикадельки из мамонта, кофе без кофеина, яйца не от куриц и многое другое;
- Charles M. Denby, Rachel A. Li, Van T. Vu, Zak Costello, Weiyin Lin, et. al.. (2018). Industrial brewing yeast engineered for the production of primary flavor determinants in hopped beer. Nat Commun. 9;
- N. Milne, P. Thomsen, N. Knudsen, P. Rubaszka, M. Kristensen, I. Borodina. (2020). Metabolic engineering of Saccharomyces cerevisiae for the de novo production of psilocybin and related tryptamine derivatives. Metabolic Engineering. 60, 25-36;
- Keith Lacy, Rita Mormando, Jeremy R. Smith, Patrick A. Gibney, Lance M. Shaner, Laura T. Burns Identification of the yeast mannoprotein geneHZY1as a key genetic determinant for yeast-derived haze in beer — Cold Spring Harbor Laboratory;
- Шоггот в банке;
- Charlie Gilbert, Tzu-Chieh Tang, Wolfgang Ott, Brandon A. Dorr, William M. Shaw, et. al.. (2021). Living materials with programmable functionalities grown from engineered microbial co-cultures. Nat. Mater.. 20, 691-700.








