
Генетическое тестирование и патернализм в медицине
14 марта 2014
Генетическое тестирование и патернализм в медицине
- 4540
- 6
- 5
Фотография René Maltête иллюстрирует «скрещивание», а также как у здоровых родителей может родиться ребенок с наследственным заболеванием
-
Автор
-
Редакторы
За что подверглась критике компания 23andMe? Какие возможности на сегодняшний день существуют у генетического тестирования? О чем не могут договориться между собой специалисты — врачи и генетики? Представляем вашему вниманию анализ плюсов и минусов популярной услуги — анализа ДНК.
Интернет активно обсуждает ситуацию, сложившуюся с американской компанией 23andMe — FDA предписывает ей прекратить прямую продажу клиентам наборов для генетического тестирования из-за отсутствия медицинской лицензии. Вышла большая российская статья на эту тему, заканчивающаяся так: «Спор 23andMe с FDA, по сути, сводится к вопросу о том, стоит ли давать людям свободный доступ к их генетическим данным или они настолько опасны, что лучше оставить это право только за специалистами. Трудно сказать, чем завершится этот не столько юридический, сколько мировоззренческий диспут» [1].
Я согласна, что диспут именно мировоззренческий, и хорошо, что дискуссия на эту тему возникла явно, а не кулуарно в недрах министерств и ведомств. Сейчас у всех сторон есть возможность быть услышанными, и широкая публика может сформировать свое отношение к генетике не на основе далеких от реальности художественных фильмов, а путем анализа высказанных в публичной прессе профессиональных мнений.
Я постараюсь описать несколько основных подходов и подчеркнуть как их сильные, так и уязвимые стороны. Мне кажется, их можно попытаться оценить объективно, даже если у тебя самого есть определенная, сформированная позиция.
Начнем с описания проблемы. Для этого прежде всего надо представлять, какие у нас есть технологические возможности получения и анализа генетических данных на сегодняшний день, с учетом цены и, следовательно, доступности. Так что
Часть 1. Какую информацию генетики могут сообщить человеку уже сейчас, а какую — не могут
Еще несколько десятилетий назад ученые научились проверять у человека наличие определенных (описанных в научной литературе) мутаций, приводящих к наследственным болезням, — таким как гемофилия. Традиционно для этого используются различные варианты технологии ПЦР (полимеразной цепной реакции), позволяющей «размножить» интересующий фрагмент ДНК в пробирке и, получив достаточное количество биологического материала, провести молекулярно-биологические исследования (фрагментный анализ, секвенирование и др.) В последнее десятилетие все бóльшую популярность набирает технология ДНК-микрочипов, предназначенных для одновременной проверки наличия большого количества описанных ранее мутаций, положение которых в геноме хорошо известно (рис. 1). Подробнее с методами молекулярной биологии можно ознакомиться в статье «Важнейшие методы молекулярной биологии и генной инженерии» [2].

Рисунок 1. Сравнение ведущих методов молекулярно-генетической диагностики. Все эти методы нацелены на то, чтобы узнать информацию, содержащуюся в ДНК человека. Подробнее о них рассказывается в статье [2].
Результаты такого анализа можно достаточно уверенно трактовать в терминах медицинской генетики. Известна связь исследуемых мутаций с болезнями и вероятность, с которой та или иная комбинация мутаций приведет к болезни. В помощь тем людям, у которых обнаружены опасные мутации, разработаны методы пренатальной диагностики и преимплантационной генетической диагностики (ПГД). В отдельных случаях создано специфическое лечение.
Новейшие методы генетического анализа, основанные на полногеномном секвенировании, расширяют диагностическое поле с набора отдельных мутаций (пусть и большого) до всей последовательности ДНК: здесь уже можно найти мутации, ранее в литературе не описанные и «невидимые» для метода микрочипов по причине отсутствия их точных «координат». Однако с трактовкой таких «новых» мутаций есть большие сложности. Отчасти они связаны со сложностью биоинформатической задачи обработки огромных массивов данных без потери значимой информации. Но самое большое препятствие состоит в том, что, не обладая информацией о здоровье людей, имеющих ту же самую мутацию, уверенные прогнозы насчет конкретного больного сделать нельзя.
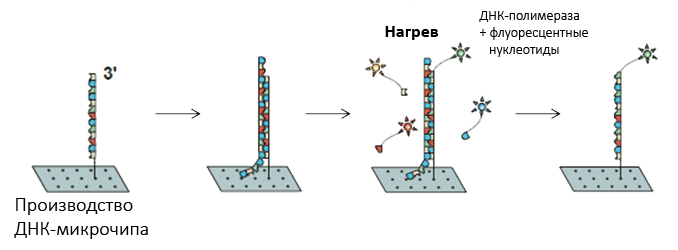
Рисунок 2. Технология ДНК-микрочипов. ДНК пациента гибридизуется с коротким фрагментом «референсной» ДНК, закрепленной на поверхности ДНК-микрочипа. После гибридизации происходит удлинение референсной цепи на один нуклеотид в том самом месте, где находится искомая мутация. Нуклеотиды, участвующие в достройке ДНК, помечены различными флуоресцентными метками, и по регистрации флуоресценции в лазерном луче можно определить, какой именно нуклеотид включился в ДНК и, следовательно, какую мутацию содержит ДНК пациента.
Кроме мутаций, среди генетических вариаций выделяют еще полиморфизм — присутствие в популяции нескольких вариантов гена. В медицинской генетике принято различать мутации, как клинически значимые варианты, а полиморфизмами называть такие варианты, у которых клиническое значение слабое или непонятное. Полиморфизмы в разных генах встречаются очень часто и в некоторой степени объясняют, почему, например, люди по-разному реагируют на лекарства или усваивают продукты питания (переваривают молоко, например). Есть такие полиморфизмы, анализ которых сообщает информацию скорее не для лечения, а для интереса — почему отличается вкусовая чувствительность, как гены влияют на характер или даже спортивные склонности. Практикуется также исследование аллелей в особых генетических локусах (аллель — более широкое понятие, чем полиморфизм, — обозначает любые варианты одного и того же гена), которое позволяет определить происхождение человека по отцовской и материнской линии.
А еще можно проводить тестирование на предрасположенность к многофакторным заболеваниям — таким как рак, диабет, ишемическая болезнь сердца. В каждом случае известно множество задействованных генов, в большинстве которых определены и существенные мутации, и полиморфизмы с неясным значением. Однако помимо этого на риск развития таких болезней огромное влияние оказывают негенетические факторы, так что однозначного прогноза по генетическим тестам сделать просто нельзя.
Вообще, нужно четко понимать: чем дальше от медицины (с ее давно и тщательно собираемыми клиническими данными), и чем больше генов участвует в регуляции процесса, тем труднее по результатам генетического тестирования сказать пациенту что-то определенное. И тут, когда мы вручаем человеку листок с результатами, он недоуменно смотрит на него, а потом поднимает глаза и говорит: «Ну и что?» К сожалению, ответить на этот вопрос чаще всего нечего.
Часть 2. Какие генетические услуги предлагаются клиентам
Традиционно врачи-генетики направляют пациентов с подозрением на наследственное заболевание на молекулярно-генетическое подтверждение. Такой анализ может называться, например, «поиск частых мутаций в гене wingless». Потом направившие врачи объясняют пациентам смысл результатов, полученных в лаборатории.
Менее распространено, но уже вполне возможно секвенирование полной нуклеотидной последовательности гена, «подозреваемого» в качестве причины болезни. Это тоже хорошо налаженный, отработанный метод [3], [4]. Им пользуются, когда в гене неизвестны частые мутации (т.е. они могут равновероятно случиться в разных местах) или среди частых ничего не нашлось. Тогда для анализа эффективнее будет знать полную последовательность гена, а не просто вариации по отдельным нуклеотидам.

Рисунок 3. Принцип генотипирования при помощи технологии APEX. После прохождения реакции свечение точек на микрочипе, соответствующих мутациям, регистрируется в четырех волновых диапазонах. Таким образом происходит определение последовательности в точке мутации или SNP. Гибридизуется как смысловая, так и антисмысловая последовательность [5].
Еще есть микрочиповые (а скоро появятся на рынке и основанные на NGS, «секвенировании нового поколения») скрининговые панели, предназначенные для здоровых людей, желающих проверить, носителями каких мутаций они являются, какие риски это несет для них самих и их детей (рис. 2, 3). Такие микрочипы ориентированы на определение большого количества мутаций в разных генах. Поскольку распространенность мутаций у разных народов может сильно отличаться (см. таблицу), то большое преимущество имеют чипы, разработанные с учетом популяционных данных для конкретной группы людей — панель для евреев-ашкенази, панель для жителей Средиземноморья и т.д. Есть и российский чип «Этноген», разработанный для жителей России и ее соседей.
| Заболевание | Частота | Ген | Народность |
|---|---|---|---|
| Общемировые наследственные заболевания | |||
| Вульгарный ихтиоз | 1 : 500 | FLG | — |
| Нейрофиброматоз I типа | 1 : 3 500 | NF1 | — |
| Синдром Шарко-Мари-Тута | 1 : 3 500 | 31 ген | — |
| Нейросенсорная тугоухость | 1 : 5 000 | GJB2 | — |
| Муковисцидоз | 1 : 10 000 | CFTR | — |
| Фенилкетонурия | 1 : 10 000 | PAH | — |
| Национальные болезни | |||
| Спиноцеребеллярная атаксия | 1 : 500 | SCA1, 2, 3 | Якуты |
| Остеопетроз | 1 : 3 500 | TCIRG1 | Чуваши, Мари |
| Аутосомно-рецессивный эритроцитоз | 1 : 5 000 | VHL | Чуваши, Мари |
| Миотоническая дистрофия | 1 : 5 000 | DM1 | Якуты |
Есть панели полиморфизмов — коммерческие наборы для тестирования на всякого рода «предрасположенностей к». На такое обследование иногда тоже направляют врачи, хотя чаще уже не врачи-генетики, поскольку репутация у таких тестов куда более сомнительная. Их результаты не часто имеют клиническое значение. Это может быть связано как с тем, что заболевание является многофакторным, так и с тем, что у клиницистов нет возможности (или желания, или опыта) менять лечение в зависимости от генетических данных. Некоторые фирмы ведут рекламу таких тестов среди широкого населения, и люди сами решают провести такое обследование, а потом долго ищут в интернете, кто бы взялся за трактовку полученных результатов.
Есть и откровенно неклинические наборы для генетического обследования — такие, как исследование геногеографии, т.е. происхождения человека, его близость к тем или иным народам из разных частей планеты. А также существуют комбинированные панели, куда входят как мутации, приводящие к болезням, так и непонятные полиморфизмы, и явно непредназначенные для медицинской трактовки тесты.
Часть 3. В чем конфликт?
Упомянутая в самом начале статьи компания 23andMe предоставляет как раз услугу по тестированию «комбинированного типа» на базе микрочиповой технологии. В состав их панели вошли «сильные» (значимые) и «слабые» мутации, полиморфизмы, аллельные варианты, данные о происхождении — всё, что можно было сделать в рамках формата микрочипового анализа. Это их первая особенность — универсальность теста. Вторая — доступность! Сейчас их услуга стоит всего $99. С точки зрения охвата населения скринингом это, разумеется, огромный плюс. И третья особенность — отсутствие «живого» генетического консультирования. Его заменяет автоматизированная онлайновая экспертная система, в которой есть функция «дать согласие на предоставление информации» в отношении определенных мутаций.
Таким образом, компания 23andMe совместила в одной услуге как «развлекательную», так и клинически ориентированную, медицинскую генетику.
Чем разозлила сразу всех.
Потому что есть несколько позиций, с разных сторон враждебных концепции 23andMe.
С одной стороны, сторонники применения генетических тестов «с пользой» очень не любят развлекательную генетику, когда она замаскирована под медицинскую услугу. В самом деле — это очень вредит репутации генетики как таковой. Для примера, замученные врачи частенько нервно реагируют на слова пациента «А вот еще мы тут тест сделали сами, он что значит?» Потому что ответ — «Да ничего он не значит, это гадание, не дающее клинически достоверной информации!» — не устраивает пациента категорически: «Как же так, это же передовой метод, мы столько денег отдали! Доктор, вы просто не понимаете!» Далее, даже в случае личной консультации разочарование пациента не меньше — он-то думал, что ему сейчас скажут, как жить дальше, а оказывается, что все рекомендации сводятся к «ну, вам курить нельзя, и алкоголь следует ограничить». (Различия между медицинской и «развлекательной» генетикой подчеркнуты на рисунке 4.)
Самое обидное, что потом и этим пациентам, и этим врачам очень трудно бывает объяснять, что есть ведь и настоящая медицинская генетика, и важные для лечения и прогноза заболевания мутации. Вот бы лучше ими занимались, а не развлекательным гаданием на полиморфизмах. Иллюстрацией к этой проблеме может быть старая врачебная шутка: «Прежде, чем назначить анализ, подумайте, что вы сделаете, если он будет А) отрицательным и Б) положительным. Если ответы одинаковы, надобность в анализе отпадает».

Рисунок 4. Принципиальное различие между медицинской (на зеленом фоне) и развлекательной генетикой заключается в необходимости активного действия после прохождения теста и получения тревожного результата
С другой стороны, другие приверженцы той же самой медицинской генетики считают, что серьезные исследования должны проводиться исключительно по назначению врача. И результаты надо не просто сообщать пациенту, но консультировать его с разъяснением рисков. И чтобы непременно это делали медики, а не генетики-исследователи. Так что клинически значимую диагностику следует оставить медицинским лабораториям со специальными сертификатами, а вот напрямую клиентам можно продавать такую как раз такую коммерческую услугу, как развлекательная генетика.
Часть 4. Чего они все опасаются и какие аргументы есть в оправдание стратегии 23andMe?
У каждой такой позиции есть свои основания. Предлагаю для простоты рассмотреть идеальную ситуацию, где есть только идеологические, или, как выше было предложено называть, мировоззренческие противоречия. Нет ни интересов Big Pharma, ни лобби страховых компаний, ни заинтересованности крупных корпораций. А есть только искреннее желание причинить пациенту пользу. Только ее все себе представляют по-разному.
Условные «медики» вполне справедливо считают, что генетическая информация может приносить не только пользу, но и вред. Во-первых, человек, которому сообщили о мутации, может попросту запаниковать. Известны случаи самоубийств при получении результатов тестирования на особенно тяжелые неизлечимые заболевания (такие, например, как хорея Гентингтона). Во-вторых, человек может неправильно понять значимость рисков и свои возможности управления ими. Он может не понимать, например, что одна копия мутации иногда вообще безвредна — болезнь вызывают только две. Но иногда одной достаточно — и тогда, наоборот, есть вероятность, что пациент недооценит угрозу. Есть и риск распада семей — когда человек, узнавший, что они с супругом являются носителями одной и той же мутации, вместо пренатальной диагностики для предотвращения болезни у потомства решит бросить супруга.

Рисунок 5. Фирма «гарантирует»!
Условные же «исследователи» считают, что информация — это сила, ее не может быть много, и она должна быть доступной (хотя они тоже страхуются, см. рисунок 5). И у этого подхода тоже есть свои аргументы. Позитивным аргументом является то, что поиск информации сейчас значительно упростился за счет появления онлайн-ресурсов. И мотивированный человек, желая понять, что означают его результаты, вполне может найти сведения в интернете, обратиться за онлайн-консультацией или, наконец, самостоятельно прийти на прием к врачу-генетику — не потому, что это обязательный этап генетического обследования, а потому, что у него нашлось что-то, о чем ему необходимо узнать больше.
А негативным аргументом является печальное понимание, что идеальная ситуация «каждому пациенту по персональному врачу-генетику, и пусть никто не уйдет непроконсультированным» пока совершенно недостижима. Врачей-генетиков очень мало, а стоимость их услуг высока. Да и гарантии, что врач-генетик выдаст более квалифицированную информацию, чем можно найти в интернете за пять минут, увы, нет. Потому что генетика развивается очень быстро, в сети сведения обновляются стремительно, а вот врачи их отслеживать успевают не всегда. Ведь они далеко не всегда владеют английским языком, посещают в сети правильные места или даже просто знают о существовании базы данных OMIM (каталога известных наследственных заболеваний). Вот и получается, что в таких реалиях пациент, читающий на иностранных языках и заглядывающий хотя бы в англоязычную википедию (хотя сейчас не редкость пациенты, которые уже пользуются и OMIM, и PubMed), оказывается уже в более выигрышном положении, чем не читающий по-английски доктор, который привык полагаться на учебники, по которым его когда-то учили, и переводную литературу, которая часто устаревает раньше, чем ее у нас издадут.
В защиту конкретно 23andMe мне бы хотелось отметить, что у них хоть и не предусмотрено «живых» консультаций, однако есть прекрасная система выдачи персонализированной информации через специальный сайт. Там подробно, грамотно и понятным языком описано, что значит та или иная «находка». Конечно, система не отслеживает обратную связь, не может оценить, понял ли клиент объяснения, не нужна ли ему дополнительная поддержка. Но там по возможности очень аккуратно объяснены «потенциально опасные» вопросы, множество раз повторяется рекомендация обратиться к врачу в реале, предусмотрена дозированная выдача информации, чтобы человек, прежде чем увидеть какую-то часть результатов, задумался, готов ли он к этому.
Часть 5. Принцип «не навреди» и патернализм в медицине — где граница?
Медиков учат, что первейшая задача врача — не нанести своими действиями дополнительного вреда пациенту.
Из-за чего у них часто формируется высокомерное отношение к пациенту, как к неразумному дитяти. Такое отношение называется патернализм.
Патерналисты в своем стремлении оградить пациента от ятрогенной (наносимой врачами) травмы смещают ответственность за здоровье человека с него самого на его врача.
Особенно неуместно потом, кстати, выглядят претензии к тому, что пациенты не соблюдают предписания и вообще ведут себя безответственно и инфантильно. Ну еще бы — у них же забрали ответственность, вот они роль детей и приняли.
А если относиться к пациентам, как ко взрослым разумным людям, то ответственность делится. Врач отвечает за то, чтобы грамотно проконсультировать, когда к нему за этой консультацией обращаются. Чтобы помочь изложить простым языком и распространить информацию в той области, где он компетентен. А пациент отвечает за свое решение пройти тестирование, и обратиться за консультацией или искать информацию самому. И тогда, придя к врачу, он ему доверяет заведомо больше, чем когда его тащат на консультацию силком.
А теперь внимание, вопрос. Не слишком ли «идеальный» ли это пациент? Встречается ли он в реальности? Или это такая же недостижимая абстракция, как и доступный-квалифицированный-уважительный врач-генетик?
И вот именно этот вопрос является мировоззренческим. Это вопрос веры в людей.
Заключение. Личная позиция, или идеальный мир, как его вижу я
Я медик по образованию, исследователь по второму образованию, и я работаю в области генетического тестирования и консультирования (заведую лабораторией «Генетико» и ПГД-консультированием в Институте Стволовых Клеток Человека — см. врезку). Я занималась генетикой как в России, так и в США, и, конечно, сравнивала разные подходы. И у меня есть свое мнение о том, «как правильно», причем я его с годами серьезно пересматривала и скорее всего, буду и дальше, с накоплением опыта, корректировать.
Мне кажется, что генетические услуги должны быть доступны. Я не люблю «развлекательную генетику», считая, что она много вреда нанесла репутации того дела, которым мы занимается. Но той же 23andMe я простила бы все эти заигрывания с полиморфизмами только за то, что их тест стоит всего $99. И благодаря такой доступной цене тысячи людей смогли вовремя узнать не только про свое происхождение и способность чувствовать разные запахи, но и про то, что у них есть значимая мутация, из-за которой может родиться больной ребенок. И они пошли к врачу, и им рассказали про ПГД (преимплантационная генетическая диагностика — проверка эмбрионов при ЭКО [6], [7]) и провели ее, и вместо больного ребенка у них родился здоровый. И, да, конечно, было бы лучше, чтобы такой тест назначали и объясняли врачи на личной консультации. Но если из-за этого цена станет не $99, а $999, то таких людей будет намного меньше, поскольку такую сумму «просто так» мало кто потратит. Вместо массового скрининга это будет услуга «для богатых». А у всех остальных будут продолжать рождаться больные дети.
Так что в реальных современных условиях самым правильным мне представляется такой подход. Есть услуга «генетическое тестирование». Это должна быть тщательно подготовленная и проверенная скрининговая панель с часто встречающимися и клинически значимыми в конкретной популяции мутациями. И эта услуга должна быть широко доступна и «вписана» в систему здравоохранения, обеспечивая действительно массовое обследование населения в режиме скрининга.
Для людей, проходящих такое обследование, должна быть создана удобная и понятная система автоматического консультирования, в которой, помимо справочной информации, специально выделялись бы случаи, когда пациенту необходимо обратиться к врачу за личной консультацией. А также, что найденные важные мутации следует прицельно проверять независимым методом. И в этой системе должны быть контекстно размещены ссылки на базы данных и клинических исследований и другие достоверные источники, куда пациент при желании сможет углубиться самостоятельно, не опасаясь нарваться на «волновой геном» и прочую лженауку в своих поисках на просторах рунета. Помимо этого, очень важно, чтобы были ссылки на группы поддержки и пациентские организации, не позволяющие человеку остаться один на один с серьезной проблемой. В России такие группы уже тоже появляются — в формате как тематических блогов и сайтов, так и больших организаций, проводящих ежегодные конференции по редким заболеваниям.
Для работы с такими пациентами понадобятся и специальные психологи, причем знающие генетику — чтобы не пытались объяснить наследственные заболевания плохой кармой или тем, что мама не любила.
И нужна система подготовки врачей-генетиков и генетических консультантов, причем совершенно не такая, как сейчас. Это отдельный сложный вопрос, и тут, кстати, есть чему поучиться у американцев.
Уже сейчас для создания такого комплексного подхода есть практически все. Методы, позволяющие уменьшить себестоимость анализа, информация для создания системы онлайн-консультирования, немногочисленные, но квалифицированные врачи-генетики для работы со сложными случаями, эксперты, готовые проводить обучение новых врачей, пациенты, готовые вникать в суть своей проблемы и поддерживать других людей с похожей ситуацией. Это все надо в первую очередь — организовать.
И мы это обязательно сделаем.
Литература
- Долотовская С. (2013). Плевок в будущее. Lenta.ru;
- Важнейшие методы молекулярной биологии и генной инженерии;
- 454-секвенирование (высокопроизводительное пиросеквенирование ДНК);
- Код жизни: прочесть не значит понять;
- Tõnisson N., Oitmaa E., Krjutskov K., Pullat J., Lind I., Leego M., Kurg A., Metspalu A. Arrayed Primer Extension Microarrays for Molecular Diagnostics. Oxford: Academic Press, 2010;
- Paul R. Brezina. (2013). Preimplantation Genetic Testing in the 21st Century: Uncharted Territory. Clin. Med. Insights. Reprod. Health. 7, 17-21;
- «За экстракорпоральное оплодотворение» — это не тост, а Нобелевская премия!.






