
Почти детективная история о том, как элемент-убийца помог возникнуть жизни
29 октября 2011
Почти детективная история о том, как элемент-убийца помог возникнуть жизни
- 2640
- 19
- 2
Озеро Моно расположено на востоке Центральной Калифорнии, восточнее Йосемитского национального парка, между горами Сьерра-Невада и калифорнийскими Уайт Маунтинз. На южном берегу озера находится небольшое поселение Ли Вининг. Единственной впадающей в Моно рекой является Оуэнс.
-
Автор
-
Редакторы
Статья на конкурс «био/мол/текст»: Год назад исследователи из американского Национального аэрокосмического агентства (NASA) сообщили об открытии уникальной способности изучаемого ими микроорганизма использовать в качестве строительного материала для своих клеток... мышьяк! И дело даже не в том, что этот химический элемент с подачи авторов детективных рассказов считается смертельным ядом — в природе существует много микроорганизмов, спокойно переносящих его токсическое воздействие, да и для многоклеточных организмов он в малых дозах бывает полезен. Загадка заключается в том, что атомы мышьяка используются микробом для строительства самого главного компонента клетки — дезоксирибонуклеиновой кислоты (ДНК), несущей важнейшую информацию, передающуюся по наследству. Но так ли это неожиданно? Возможно, другие представители земных форм жизни также смогли бы «научиться» использовать мышьяк в своих жизненных циклах (в которых обычно задействован ближайший аналог мышьяка — фосфор)? Следует ли называть находку необычных бактерий открытием альтернативных биохимических путей для живых организмов планеты Земля? Попытаемся разобраться в этих вопросах по порядку.
Конкурс «био/мол/текст»-2011
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2011 в номинации «Лучшая обзорная статья».
Анонсированный в конце октября и опубликованный 2 декабря 2010 г. пресс-релиз NASA вызвал огромный интерес и настоящий бум в средствах массовой информации, которые, в частности, поспешили сообщить об обнаружении «внеземных форм жизни». Многие из последовавших в СМИ публикаций содержали многочисленные кривотолки, основанные на неадекватном переводе, непонимании сути вопроса и желании сотворить сенсацию там, где ее нет. Материалы исследований, полученные специалистами при финансировании NASA, очень интересны — тем более важно при воспроизведении первоисточника сохранять его смысл. Ниже приводим перевод этого релиза, максимально приближенный к оригиналу.
Как все началось
Жидкая среда наиболее благоприятна для протекания большинства химических реакций. Этот факт, казалось бы, убедительно свидетельствует в пользу того, что жизнь на нашей планете зародилась в океане.
Важнейшими элементами (так называемыми макроэлементами ), без которых современная земная жизнь не возможна, являются водород, кислород, углерод, азот и фосфор . Первые четыре из них являются чрезвычайно распространенными в природе.
Термины, отмеченные курсивом, поясняются в Словарике в конце статьи.
Часто к этому списку добавляют шестой элемент — серу.
Сама океанская вода уже содержит два важнейших элемента, обязательно входящих в состав органических молекул — водород и кислород. Еще два макроэлемента — углерод и азот — также являются чрезвычайно распространенными в природе и существуют в ней в первую очередь в виде атмосферных газов, то есть они доступны практически повсеместно.
В отличие от этих макроэлементов, фосфор имеет только одну газообразную форму — чрезвычайно реакционноспособный газ фосфин (PH3), возникающий в весьма специфических условиях и при попадании в атмосферу легко окисляющийся до нелетучих соединений. Сложные комплексные минералы фосфора — например, апатиты — слаборастворимы в воде, хотя в природе они встречаются не так уж редко: в земной коре этого элемента содержится до 0,1% по массе. Поэтому, несмотря на то, что по важности для жизни фосфор располагается сразу за водородом, кислородом, углеродом и азотом, для живых организмов он намного менее доступен, чем другие макроэлементы. Зачастую именно количество биодоступного фосфора является лимитирующим фактором роста и развития микроорганизмов.
Но если в условиях недоступности одного из ключевых элементов живые организмы не могут нормально развиваться — как же они тогда в таких условиях возникли? Конечно, можно предположить, что на ранних этапах эволюции воды Мирового Океана имели высокую кислотность (что облегчало растворение фосфатов). Но есть и другой выход из этого противоречия: возможно, первые формы земной жизни базировались не на фосфоре, а на его более доступном аналоге — мышьяке!
Путь пребиотической (чисто химической, «добиологической») эволюции также пока во многом загадочен. Исследования процессов, происходящих в звездах, моделирование условий в первичной атмосфере, анализ космической пыли и структуры метеоритов скорее добавляют новые вопросы, чем дают ответы на старые. В частности, остается загадкой, сколько раз жизнь на нашей планете возникала и/или претерпевала революционные изменения. Ясно только одно: в какой-то момент в водной или неводной среде из «земных» или «космических» элементов впервые возникли мономерные органические молекулы со сравнительно небольшой молекулярной массой — спирты, карбоновые кислоты, аминокислоты, пурины, пирролы, пиримидины, сахара . Взаимодействуя между собой (а также с водой и газами первичной атмосферы), они сформировали более сложные структуры, на каком-то этапе «научившиеся» самовоспроизводиться. А от них уже оставался один шаг до живой клетки...
Об исследованиях, касающихся зарождения жизни, см.: «К вопросу о происхождении жизни» [9]. — Ред.
Один из наиболее вероятных сценариев эволюции жизни — с учетом изменения условий на нашей планете — выглядит следующим образом. Возможно, первые циклы химических реакций как прототип сегодняшних клеток (живых замкнутых систем) возникли на основе кристаллов, то есть в «неводную» эпоху пребиотической эволюции. Такие циклы должны были быть, с одной стороны, относительно замкнутыми, то есть не нуждаться в дополнительных участниках «извне», а с другой стороны — были способны к автокатализу, то есть могли сами себя стимулировать (т.е. в результате протекания химической реакции, вырабатывается продукт, который является катализатором, стимулятором этой первичной, породившей его химической реакции). Эту идею хорошо иллюстрирует так называемая гипотеза «мира РНК», согласно которой на первом этапе возникновения жизни молекулы РНК выполняли как функцию хранения информации (сейчас это делает ДНК), так и функцию катализа процессов ее «перезаписи» для других поколений (сейчас это делают белки). В этой гипотезе мир РНК, реализуя функции ДНК и белков, стал прообразом современной белково-нуклеиновой жизни, в которой молекулы РНК заняли свое «рабочее место»: информационные РНК являются посредниками между генами и их продуктами — белками, малые ядерные РНК «корректируют» работу генов, рибосомные РНК имеют «реликтовую» функцию (катализируют биосинтез), транспортные РНК стали высокоизбирательными переносчиками аминокислот.
Впоследствии, по мере остывания атмосферы, появилась вода — уникальный полярный растворитель (это значит, что в ее молекулах электрический заряд распределен несимметрично). Полярность обусловила повышенную растворимость в воде многих неорганических соединений. Возможно, жизнь претерпела изменения и стала «водной» только на этом этапе. Действительно, вода — очень удобная и эффективная среда для жизни: доступность макроэлементов в водной фазе, как уже упоминалось, резко возрастает. Полярность воды живые системы «эксплуатируют» максимально: именно она является критической в организации и формировании структуры клетки, в стабильности ДНК, при сохранении энергии, полученной во время питания. Вода принимает участие во всем, ведь современные живые системы — это комплексы макромолекул и молекул, окруженные водными оболочками.
Яд или лекарство?
В 1987 г. были представлены результаты исследований, свидетельствующие о феномене фосфора как макроэлемента, способствующего сохранению стабильности генетического материала. Мышьяк является ближайшим аналогом фосфора. Атом мышьяка имеет близкий радиус и почти идентичную электроотрицательность. Наиболее распространенное в клетке соединение фосфора — фосфат PO43− — ведет себя аналогично арсенату AsO43− . Эта физико-химическая схожесть является главным фактором токсичности мышьяка: ферменты клетки, «работающие» с фосфатом, не могут отличить его от арсената. Поэтому, попав в клетку, атом мышьяка «воспринимается» ферментами как фосфор, однако функционально он фосфор заменить не может, что приводит к множественным нарушениям протекания жизненно важных реакций. В результате клетка лишается энергии для поддержания своей жизнедеятельности. Это блокирует обмен веществ, так как продукты обмена, возникающие в ходе подобных реакций, не могут далее участвовать в других жизненно важных процессах из-за разницы в реакционной способности фосфор- и мышьяксодержащих метаболитов.
Дело в том, что соединения фосфора намного стабильнее, чем соединения мышьяка. Именно это, а также то, что сам по себе мышьяк и около 200 его соединений встречаются в природе весьма редко, и предопределяет его токсичность. В земной коре этого элемента содержится не более 1,7×10−4%, и сосредоточен он только в местах скопления тяжелых металлов, в глубинных гидротермальных источниках, а в морской воде и в верхних слоях почвы его концентрация ничтожно мала. Подавляющее большинство живых организмов с ним практически не сталкиваются, что и объясняет такую «неразборчивость» ферментов. Тем не менее, практически у всех организмов имеются механизмы смягчения эффекта токсичности микро- и ультрамикродоз мышьяка. Некоторые прокариоты способны использовать соединения мышьяка для получения необходимой энергии, то есть для питания. Эти микроорганизмы весьма разнообразны и встречаются в разных экологических нишах. У них существуют эффективные системы, обеспечивающие устойчивость к мышьяку. Наиболее эффективны они именно у организмов, «имеющих дело» с мышьяком в своей природной эконише, тем более — использующих мышьяк для питания (например, путем преобразования арсенита в арсенат с выделением энергии — т.н. «арсенатное дыхание»). Любопытно, что в случае, когда мышьяк небольшими дозами хронически попадает в организм (как одноклеточный, так и высший — многоклеточный, в то числе и человека), возможно развитие устойчивости к нему, которая, впрочем, довольно индивидуальна и носит ограниченный характер . Заметим этот факт — наличия «спящих» генетических механизмов системы детоксикации мышьяка. Механизмов на самом деле несколько, системы выведения мышьяка из клетки не оригинальны и довольно консервативны как у одно-, так и у многоклеточных организмов.
Кроме этого, препараты мышьяка используют в медицине как антипротозойное средство — для лечения инфекций, вызванных простейшими (трипаносомами, амебами, плазмодиями), а также как некротизирующее средство при местном применении. До появления антибиотиков мышьяк наряду с висмутом и ртутью применяли для лечения бактериальных инфекций.
Однако, возвращаясь к вопросу о пребиотической эволюции, следует вспомнить, что, по одной из версий, первые самокатализируемые системы «собирались» и функционировали в безводной среде. Вполне возможно, что соединения на основе мышьяка участвовали в древних метаболических системах и являлись предшественниками аналогичных процессов на основе фосфора.
Такое допущение не выглядело бы слишком смелым, если бы мышьяк использовался какими-либо современными организмами в своих жизненных циклах — как «воспоминание» о ранних стадиях эволюции. Где искать такие «чудеса природы»? Ответ очень прост: там, где много мышьяка и мало фосфора. Удивительно, но организмы, способные использовать мышьяк для своей жизни, действительно найдены — пока только среди микроорганизмов (среди представителей Архей и Бактерий). Пока не найдено ни одного представителя Эукариотов, способных к постоянному метаболизму соединений на основе мышьяка. Возможно, причина этого кроется в том, что Эукариоты являются эволюционно самыми молодыми. Все организмы, способные к такому метаболизму, найдены в экстремальных условиях (с точки зрения человека), очень напоминающих те, что царили на Земле в эпоху зарождения жизни. Они существуют в эконишах, обособленных от большинства земных экосистем, и эта обособленность (изолированность) длится порой миллионы лет, что и объясняет удивительные свойства, присущие населяющим их микроорганизмам.
Среди таких организмов, обладающих необычными свойствами, особо выделяются археи. Еще сравнительно недавно — лет двадцать назад — их относили к царству Прокариот и называли «архебактериями». Действительно, на первый взгляд у этих экзотических микроорганизмов много общего с бактериями (рис. 1). Морфологически они представляют собой микроскопические клетки, как обычной «бактериальной» формы, так и очень необычной — треугольной, кубической, «осколочной» (в виде кусочков битого стекла). Размеры их клеток такие же как и бактериальных, однако имеются археи с длиной клетки около 0,17 мкм, и более 100 мкм (при том, что длина средней бактериальной клетки — 1–1,5 мкм). Общие принципы организации и характер деления архей также соответствуют бактериальным. Приставки «архе-» возникла в связи с тем, что в данной группе микроорганизмов достаточно много «экстремалов»:
- анаэробов (нормально существующих без доступа воздуха);
- термофилов, оптимальная температура для развития которых лежит в пределах +70..90 °C;
- ацидофилов, «предпочитающих» для обитания сильнокислую среду с pH 1–3;
- галофилов, растущих в растворах с содержанием солей до 250–300 г/л.
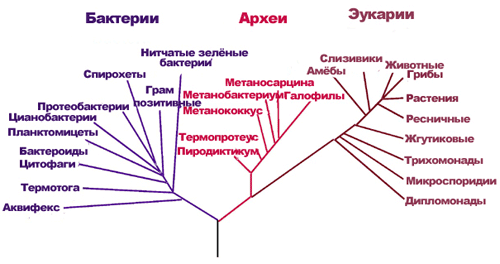
Рисунок 1. Филогенетическое «дерево родства» между живыми организмами на Земле
Наряду с прокариотами существует также царство Эукариот, к которому относятся грибы, растения, животные (в т.ч. люди).
Возьмите обычную линейку, посмотрите на миллиметровую отметку, мысленно разделите ее на 10, вы получите 0,1 мм, или 100 мкм. Клетку таких размеров, или больше, можно назвать «гигантской»! «Обычная» бактериальная клетка в 100 раз меньше.
Поэтому было высказано предположение о том, что эти микроорганизмы — достаточно древние и являются теми формами клеточной жизни (или их ближайшими родственниками), которые появились на Земле одними из первых («архе-»). Согласно данным геологии, именно на заре возникновения земной жизни условия на поверхности нашей планеты и состав ее атмосферы были очень подходящими для современных архей.
Экзотические археи
Однако при более подробном изучении выяснилось, что археи имеют некоторые уникальные характеристики, а также уникальные комбинации свойств, «принадлежащих» как бактериям, так и эукариотам.
Во-первых, у них весьма своеобразные рибосомальные и транспортные РНК. Их рибосомы по форме и размерам отличаются от бактериальных и больше похожи на эукариотные. Во-вторых, археи имеют уникальную мембрану, молекулы которой отличны от молекул бактериальных мембран и, по некоторым данным, опять же очень близки мембранам эукариот и актиномицетов. Наконец, некоторые археи способны осуществлять процессы, несвойственные другим организмам — например, генерировать метан. Для них характерны очень высокие темпы горизонтальных генных переносов — передачи молекул ДНК от одного организма другому. Археи практически неспособны к паразитизму и патогенезу. Правда, среди архей встречаются эндосимбионты эукариот (проживающие внутри их клеток). На сегодняшний день известна только одна архея (наноархея Nanoarchaeum equitans), по-видимому, являющаяся не только спутником, но и паразитом другой археи — Ignicoccus hospitalis. О том, что данная наноархея — паразит, «рассказал» ее геном (кстати, самый маленький геном среди изученных форм жизни ). Однако в ходе экспериментов с этим организмом признаков паразитизма не было обнаружено. Видимо, в этом единственном случае у архей наблюдается какой-то весьма специфический тип паразитических отношений с хозяином.
Об обладателе самого маленького генома среди свободноживущих эукариот см. «„Покороче, пожалуйста“: самый маленький ядерный геном» [10]. — Ред.
Все вышеперечисленное, как и ряд других данных, привело исследователей к выводу, что относить археи к бактериям не совсем правомерно. В связи с этим в систематике пришлось создать домены, иерархически находящиеся выше царств . «Неклассифицируемые» организмы были «вынесены» в собственный домен «Археи», наряду с доменами «Бактерии» и «Эукарии».
О том, что такое «домены жизни», почему раньше их было только два (прокариоты и эукариоты), а теперь три, а также о том, как некоторые пытаются доказать, что на самом деле их четыре, — см. «Эволюция между молотом и наковальней, или Как микробиология спасла эволюцию от поглощения молекулярной биологией» [11] и «Гигантские вирусы: 4-й домен жизни?» [12]. — Ред.
Тем не менее, происхождение архей, их возраст и степень родства с другими организмами остаются весьма дискуссионными вопросами. Большинство ученых склоняются к мысли, что археи не являются такими древними, как это представлялось еще совсем недавно. По результатам комплексного анализа были сделаны выводы о том, что грамотрицательные бактерии (например, кишечная палочка) могут быть намного старше. Предположительно археям около 900 млн. — 2 млрд. лет, в то время как грамотрицательным микроорганизмам — до 3,5 млрд. лет. Но самым любопытным оказалось их родство с эукариотами. Есть основания полагать, что, образно выражаясь, археи — не наши «предки», чудом дошедшие до нас со времен зарождения жизни, а скорее «братья», то есть формы жизни, появившиеся в результате дивергенции общего предка архей и эукариот! Так что и название «археи», по-видимому, ошибочно.
А если эти организмы не такие древние, и сами по себе они, по-видимому, стали тупиковой ветвью эволюции, не дав «потомков», — тогда чего же в них такого необычного?
Несмотря на все «разоблачения», археи являются весьма интересной и своеобразной группой. Уникальность их многих биохимических свойств, кстати, — еще один аргумент в пользу того, что археи обособились в отдельную группу и не стали родоначальниками нового эволюционного пути. Тем не менее, их нельзя назвать «неуспешными организмами». Главной движущей силой появления и развития этих микроорганизмов было заселение экологических ниш, недоступных уже имеющимся на тот момент формам жизни, то есть бактериям. Разумеется, сами археи появились не de novo, их предками были те же бактерии. Но свойства, которые им удалось приобрести, были уникальны, и именно они позволили археям поселиться там, где их предшественники не выживали. В настоящий момент археи найдены практически везде — от глубоководных вулканов, всех видов водных источников и зон вечной мерзлоты до кишечников животных и человека. По общим оценкам, они представляют до 20% биомассы нашей планеты! Будучи столь многочисленными, археи принимают очень важное участие в круговороте азота, серы и углерода.
Как уже было отмечено, главным «механизмом успешности» архей является их экстремофильность. Они встречаются, например, в гидротермальных источниках и гейзерах, где температура воды достигает 110 °C. В богатых молекулярной серой зонах возле подводных вулканов — «черных курильщиков» — найдена архея Pyrodictium occultum, или «огненная сеточка», состоящая из шаровидных клеток, соединенных тяжами. Оптимальная температура для ее существования — 105 °C. Питается архея частицами серы — она использует энергию, выделяющуюся при ее восстановлении водородом до сероводорода. Самый теплостойкий живой организм — архея Methanopyrus kandleri — способна жить при 122 °C!
Среди экстремальных термофилов много метанобразующих архей. Несмотря на то, что способность к образованию метана (CH4) свойственна только археям, микробный синтез этого газа несет ответственность за значительную часть — до 1,5% — круговорота углерода. Археи, выделяющие метан, встречаются практически повсеместно, в том числе они заселяют кишечник термитов и млекопитающих, где попутно синтезирует цианкобаламин (витамин B12).
Только археи способны жить в очень кислых условиях. К таким организмам (ацидофилам) относятся, например, термоплазмы, развивающиеся в кислых горячих вулканических источниках. Еще более «кислотолюбив» Picrophilus, живущий при pH 1, а Picrophilus torridus способен расти и развиваться при pH 0 (такой водородный показатель имеет 35%-ная соляная кислота).
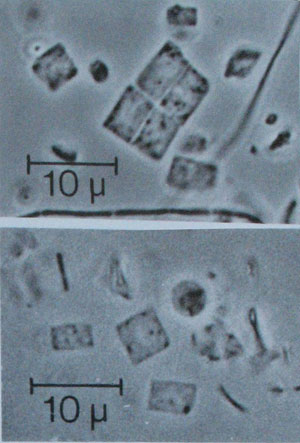
Рисунок 2. Плоские археи квадратной формы Haloquadratum walsbyi
Археи, предпочитающие обитать в водах очень соленых источников, объединяют в экологическую группу галофилов. Его представители — такие, как Natronobacterium и Natronococcus — способны развиваться не только в крайне соленых, но и в чрезвычайно щелочных условиях. Археи-галофилы — единственные «жители» Мертвого моря, расположенного на границе Израиля и Иордании. Их аналоги «населяют» практически все соленые источники. К этой уникальной и своеобразной группе относятся единственные среди архей виды, способные к использованию для жизни энергии солнечного света. Однако процесс, происходящий в их клетках, не похож на фотосинтез растений и является как бы вспомогательным — археи-фотосинтетики не могут питаться исключительно световой энергией. Тем не менее, любопытна группа пигментов, помогающих осуществлять такой фотосинтез. Эти пигменты — бактериородопсин, а также сенсорный родопсин I и II, аналогичные пигменту сетчатки человеческого глаза! Они возникают в клетках архей-фотосинтетиков лишь при отсутствии доступа молекулярного кислорода. Наконец, только среди архей найдены микроорганизмы с плоскими клетками (!) квадратной формы (!) (рис. 2).
Метаболизм мышьяка, т.е. жизнеобеспечивающие химические реакции (обмен веществ) на основе соединений мышьяка, в археях только начинают изучать. Но уже сейчас обнаружено достаточно много штаммов архей, обитающих в экстремальных экологических условиях и способных к арсенатному дыханию , при котором арсенат-ион выступает в роли окислителя в дыхательной цепи (у организмов, способных к кислородному дыханию — в том числе и людей — таким окислителем является молекулярный кислород). Так, например, в соленом кислом озере Сирлес Лейк сравнительно недавно обнаружены и изучены галофильные археи Crenarchaea, способные «дышать» пятивалентным мышьяком As (V), превращая его в трехвалентный As (III). Ряд исследователей сообщают о способности к метаболизму мышьяксодержащих соединений археями классов Methanospirillum, Methanobrevibacter, Thermoplasmata и Halobacteriales. В процессе изучения такого метаболизма в экстремальных условиях был обнаружен и описан новый класс архей Thaumarchaeota. Кроме арсенатного дыхания, у некоторых архей обнаружена чрезвычайная устойчивость к высокотоксичным формам мышьяка.
Окислительные реакции на основе соединений мышьяка. Дыхание — процесс окисления питательных веществ, поступающих в живой организм из внешней среды. В результате дыхания выделяется энергия, используемая организмом для поддержания своей жизнедеятельности. При аэробном (кислородном) дыхании питательные вещества окисляются свободным кислородом, содержащимся в воздухе или растворенным в воде. Некоторые одноклеточные используют в качестве окислителя более сложные соединения (азот в форме нитрат-иона, мышьяк в форме арсенат-иона, трехвалентное железо), причем встречаются микроорганизмы, способные в отсутствие свободного кислорода «переключаться» на анаэробное (бескислородное) дыхание.
Позже оказалось, что мышьяк-метаболизирующими микроорганизмами являются многие галофильные экстремальные бактерии, способные к арсенатному дыханию. Недавно в горячих источниках Калифорнии были обнаружены цианобактерии рода Oscillatoria и весьма древние пурпурные бактерии, также использующие соединения мышьяка в своих жизнеобеспечивающих химических процессах.
Монстры озера Моно Лейк
К группе галофильных бактерий, устойчивых к мышьяку, относится и бактерия Halomonadaceae GFAJ-1, изучаемая учеными из NASA. Эта бактерия была выделена из озера Моно Лейк в Калифорнии — очень соленого водоема с сильной щелочной реакцией (рис. 3). Около 50 лет озеро было абсолютно изолировано от других водных источников. По элементному составу оно в некотором роде уникально: концентрация мышьяка в его водах достигает 17 мг/л. Наблюдая штамм GFAJ-1 и его устойчивость к мышьяку, ученые задумались над тем, не может ли эта бактерия быть настолько «привычной» к мышьяку, что умудрилась использовать его в своей клетке как аналог фосфора, но без токсического эффекта? Надо заметить, такая мысль у ученых родилась не случайно. В принципе, в природе такие замены имеют место. Так, в ряде ферментов вольфрам аналогичен молибдену, а кадмий — аналогичен цинку. Медь является аналогом железа в гемолимфе моллюсков и членистоногих. Однако до сих пор не было известно ни одного случая аналогичной замены ни одного из шести макроэлементов.

Рисунок 3. Озеро Mono Lake в восточной Калифорнии очень соленое и с сильной щелочной реакцией. Около 50 лет оно было абсолютно изолировано от других водных источников. Концентрация мышьяка в его водах достигает 17 мг/л.
Была и еще одна предпосылка для подобных соображений. Во времена зарождения жизни не существовало растительного фотосинтеза, который, однажды возникнув, преобразил атмосферу, насытив ее кислородом. Свободная атмосферная форма этого газа, которой в наше время в воздухе содержится 20,95%, на самом деле намного токсичнее мышьяка. Атмосферный кислород («рождающий кислоту») — сильный окислитель. Он способен окислить все органические молекулы, что для «неподготовленных» организмов смертельно. Именно поэтому после появления оксигенного фотосинтеза, ставшего важнейшим шагом в развитии жизни на Земле, вторым важнейшим шагом стало приобретение живыми организмами систем защиты от окислительного действия новой атмосферы, причем эти процессы шли в глобальном масштабе — кислород проникал практически всюду, даже в океаны на достаточно большую глубину. Как указывалось выше, мышьяк является элементом весьма редким, поэтому организмы с ним сталкиваются не часто. Но те из них, которые эволюционно приспособлены к существованию в условиях высоких концентраций мышьяка и низкой концентрации фосфора, возможно, не только умеют противостоять токсичности мышьяка, но и использовать его как аналог фосфора. Эту гипотезу проверили на микроорганизме, устойчивом к соединениям мышьяка — бактерии GFAJ-1 (рис. 4).
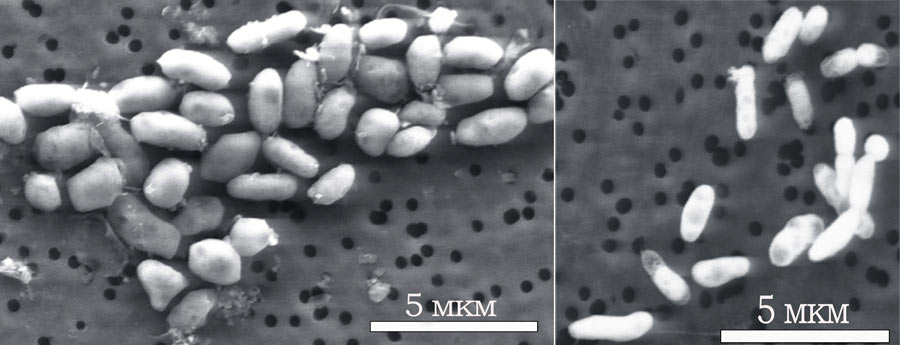
Рисунок 4. Бактерии GFAJ-1. Слева — бактерии, выросшие в питательной среде, содержащей мышьяк и не содержащей фосфора. Справа — те же бактерии, но выросшие на полноценной питательной среде (не содержащей мышьяк и содержащей фосфор).
Фосфор, как и пять других макроэлементов, входит в состав всех жизненно важных молекул — макроэргов, снабжающих живую клетку энергией, липидов мембраны и, конечно же, нуклеиновых кислот. Чтобы проверить, сможет ли подопытный микроб справиться с нестабильностью мышьяксодержащих соединений, его «поселили» в среду, полностью лишенную фосфора, но содержащую все прочие молекулы, необходимые для роста и развития, и мышьяк. Это стало ключевым моментом экспериментов: микроб должен был или «научиться» использовать мышьяк вместо фосфора (тогда в питательной среде возникло бы большое количество микробных колоний), или — если он не смог бы этого сделать — погибнуть.
Авторы эксперимента наблюдали рост микроба — то есть микроорганизм смог размножаться, строить свою ДНК и все остальные жизненно важные молекулы исключительно благодаря единственному доступному аналогу фосфора — мышьяку! Это подтвердил ряд тонких анализов. Удалось также установить локализацию мышьяка в клетках бактерий: около 80% этого элемента находилось в белках и малых метаболических молекулах (макроэргах), 6,5% содержалось в липидах мембран и ассоциированных с ними белках и около 11% — в нуклеиновых кислотах. Это полностью соответствует распределению фосфора в «нормальной» клетке. Используя дополнительные высокотехнологичные методы, ученые смогли также идентифицировать те молекулы, с которыми атомы мышьяка находятся в непосредственной связи. Все это бесспорно указывает на то, что GFAJ-1 (рис. 5) успешно инкорпорировал мышьякосодержащие соединения и может эффективно использовать мышьяк как структурно-функциональный аналог фосфора — в том числе и для построения «работоспособной» ДНК.
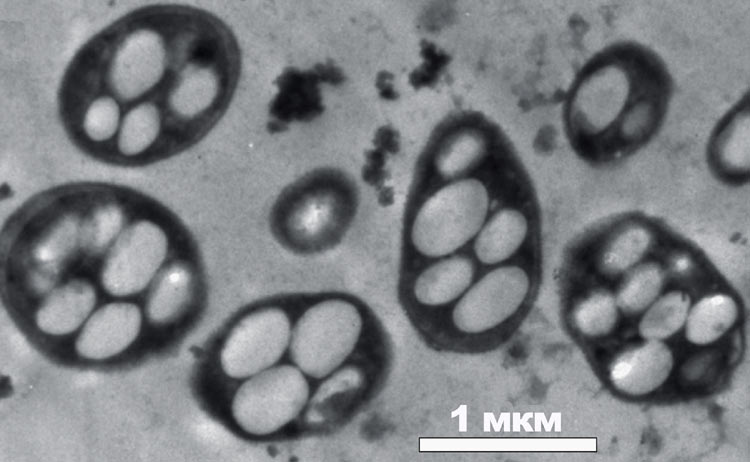
Рисунок 5. «Мышьяковые» бактерии крупнее, внутри у них образуются вакуолеподобные структуры
Таким образом, не исключено, что мышьяк, будучи токсичным элементом для большинства современных живых форм, возможно, являлся важным этапом в пребиотической эволюции. И сложные метаболические пути, неизменно использующие фосфор, вероятно, имели намного более простые прототипы, базирующиеся на мышьяке. Как упоминалось выше, изучено много примеров путей выведения мышьяка из клеток множества микро- и макроорганизмов. Большинство из них весьма сходны — при том, что в естественной среде обитания такие организмы с мышьяком не сталкиваются. Эти системы выведения, таким образом, можно «заподозрить» в реликтовости, то есть они могли возникнуть еще в те времена, когда этот элемент предположительно был неотъемлемой частью живой клетки. Но мышьяк и сегодня успешно используется некоторыми микроорганизмами, существующими в экстремальных условиях. Как свидетельствуют данные последних исследований, такие организмы могут не только противостоять токсическому эффекту мышьяка и внедрять его в свои метаболические циклы, но и строить на его основе свою ДНК! Эти открытия лишний раз подтверждают, что экология микроорганизмов-экстремофилов таит еще много загадок, а наши познания в области биологической эволюции еще требуют множества уточнений...
Литература
- NASA-funded research discovers life built with toxic chemical. (2010). Пресс-релиз NASA;
- Элементы: «Мышьяк вместо фосфора — это реально!»;
- F. Wolfe-Simon, J. S. Blum, T. R. Kulp, G. W. Gordon, S. E. Hoeft, et. al.. (2011). A Bacterium That Can Grow by Using Arsenic Instead of Phosphorus. Science. 332, 1163-1166;
- Ronald S Oremland, John F Stolz, James T Hollibaugh. (2004). The microbial arsenic cycle in Mono Lake, California. FEMS Microbiology Ecology. 48, 15-27;
- R. S. Oremland. (2003). The Ecology of Arsenic. Science. 300, 939-944;
- Thomas Cavalier-Smith. (2006). Cell evolution and Earth history: stasis and revolution. Philosophical Transactions of the Royal Society B: Biological Sciences. 361, 969-1006;
- Harald Huber, Michael J Hohn, Karl O Stetter, Reinhard Rachel. (2003). The phylum Nanoarchaeota: Present knowledge and future perspectives of a unique form of life. Research in Microbiology. 154, 165-171;
- Громов Б.В. (1997). Удивительный мир архей. «Соросовский образовательный журнал». 4, 23–26;
- К вопросу о происхождении жизни;
- «Покороче, пожалуйста»: самый маленький ядерный геном;
- Эволюция между молотом и наковальней, или Как микробиология спасла эволюцию от поглощения молекулярной биологией;
- Гигантские вирусы: 4-й домен жизни?.







