
Эпигенетика поведения: как бабушкин опыт отражается на ваших генах?
18 ноября 2014
Эпигенетика поведения: как бабушкин опыт отражается на ваших генах?
- 18857
- 0
- 7
Материнская забота влияет на поведение детенышей.
сайт fineartamerica.com
-
Автор
-
Редакторы
Статья на конкурс «био/мол/текст»: Одна из самых интересных областей современной молекулярной биологии — регуляция экспрессии генов с помощью эпигенетических механизмов. Молодая, но быстро развивающаяся ветвь науки под названием «эпигенетика» уже сейчас предоставляет в распоряжение ученых множество интересных сведений, которые меняют наше представление об индивидуальном развитии живых организмов. Процесс формирования особи, ее взросление, приобретение собственного жизненного опыта зависит не только от воспроизведения генетического материала, полученного ею от родителей, но и от изменений, которые могут происходить с этим генетическим материалом в течение жизни. Экспрессия генов зачастую управляется сложными молекулярными процессами, которые приводят к неоднозначным результатам в фенотипе. Можно объяснить это так: если генетическую информацию представить в виде текста, а затем некоторые слова выделить курсивом, некоторые — зачеркнуть, часть — подчеркнуть и выделить жирным шрифтом, то текст обретет другой смысл: многотомный роман превратится в коротенький рассказ, а диссертация — в фельетон. Бывает и такое, что эпигенетические изменения, произошедшие с индивидуумом в течение жизни и отражающие его собственный опыт, передаются потомкам и влияют на множество аспектов их развития.
Конкурс «био/мол/текст»-2014
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2014 в номинации «Лучший обзор».
Главный спонсор конкурса — дальновидная компания Генотек.
Конкурс поддержан ОАО «РВК».
Спонсором номинации «Биоинформатика» является Институт биоинформатики.
Спонсором приза зрительских симпатий выступила фирма Helicon.
Свой приз также вручает Фонд поддержки передовых биотехнологий.
Дарвин и Фрейд заходят в бар. Там на двух барных стульчиках сидят двое мышей-алкоголиков — мама и сын — и хлещут джин из двух наперстков.
Мама-мышь подымает глаза и говорит:
— Эй, гении, расскажите мне, как мой сын дошел до такого жалкого состояния?
— Плохая наследственность, — отвечает Дарвин.
— Плохая материнская забота, — говорит Фрейд.
Из журнала Discover
Материнская забота улучшает стрессоустойчивость
Есть много научных тематик, призвавших на помощь эпигенетику для объяснения тех или иных механизмов. Об этом подробно написано на «Биомолекуле» [1–3]. Здесь же пойдет речь об эпигенетике поведения. Интерес к этой области возник десять лет назад, когда было показано, как забота о потомстве у крыс влияет на стрессоустойчивось этого потомства [4].
Забота о детях начинается у крыс сразу после родов — они уделяют своему потомству много времени, кормят, чистят и вылизывают малышей. Однако в популяции крыс существуют индивидуальные различия в материнском поведении — некоторые матери не уделяют достаточно внимания уходу за детенышами. Было замечено, что у заботливых матерей потомство вырастает значительно менее боязливым и лучше обучается, в то время как дети равнодушных мамаш оказываются тревожными и труднее поддаются обучению. Оказалось, что материнское поведение в самом начале жизни детенышей (а именно в первую неделю после рождения, когда детеныши наиболее уязвимы) оказывает влияние на силу ответа гипоталамо-гипофизарной-надпочечниковой системы на стресс.
Гипоталамо-гипофизарно-надпочечниковая система управляет реакциями на стресс
Способность млекопитающих вырабатывать сложные поведенческие ответы на окружающие факторы обусловлена слаженной работой нервной и эндокринной систем. Важную роль в реакции организма на психоэмоциональный стресс играет активация гипоталамо-гипофизарно-надпочечникового механизма образования глюкокортикоидных гормонов: у человека это кортизол, у крысы — кортикостерон [5]. Гипоталамус и гипофиз — две небольшие, но чрезвычайно важные области мозга (рис. 1). Гипофиз в этой паре можно назвать генералом, а на роль генералиссимуса претендует гипоталамус. Нейросекреторные клетки гипоталамуса выделяют специальные гормоны — рилизинг-факторы, — которые переносятся с током крови в заднюю долю гипофиза. Здесь они стимулируют синтез гипофизарных гормонов, которые, в свою очередь, дирижируют работой других желез, в том числе работой надпочечников по производству глюкокортикоидных гормонов.
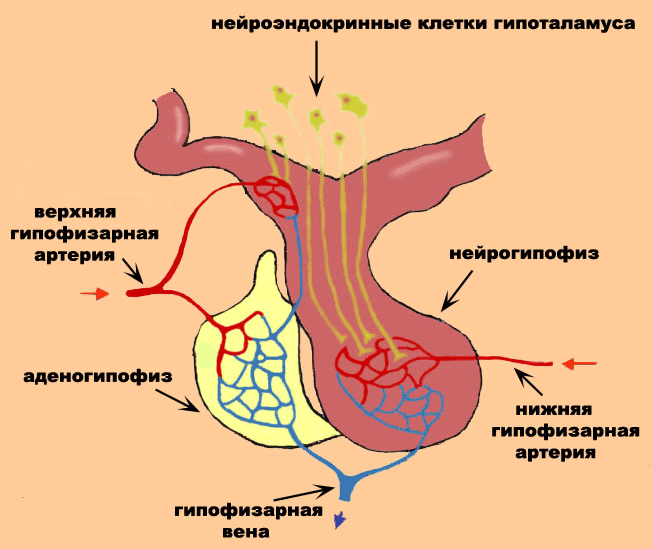
Рисунок 1. Устройство гипоталамо-гипофизарной системы
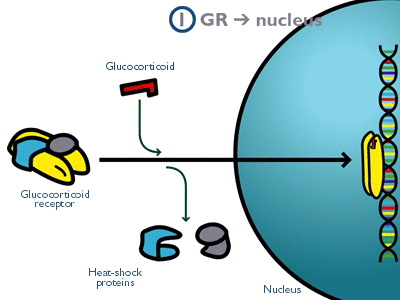
Рисунок 2. Механизм действия рецептора глюкокортикоидов. Гетеродимер глюкокортикоидного рецептора связывается с гормоном и белком теплового шока, после чего переносится через ядерную мембрану и связывается с регулируемой областью ДНК. Комплекс глюкокортикоидного рецептора с белками теплового шока обеспечивает его более высокое сродство к гормону.
Однако и активность самого гипоталамуса по выделению рилизинг-факторов регулируют некоторые другие структуры головного мозга. В их числе гиппокамп — самая древняя в эволюционном отношении и, наверное, самая загадочная область мозга [6]. Считается, что гиппокамп играет важную роль в обеспечении эмоциональной фиксации индивидуального опыта, процессе формирования ранней памяти [7] и обучения [8]. Нужно отметить, что именно гиппокамп занимает одно из первых мест среди различных отделов головного мозга по плотности глюкокортикоидных рецепторов, и поэтому он очень чувствителен к действию глюкокортикоидов — гормонов стресса. Глюкокортикоидные рецепторы относятся к так называемым ядерным рецепторам (рис. 2). Это означает, что взаимодействие гормона с рецептором приводит к активации последнего и позволяет ему связаться напрямую с участками ДНК в регуляторных районах подконтрольных генов [9], [10].
Если вырабатывается слишком много гормонов, это свидетельствует о стрессовом ответе чудовищной силы, который необходимо остановить, чтобы не нарушить сбалансированную работу всех систем организма. Поэтому, чем больше глюкокортикоидных рецепторов имеет клетка, тем «чувствительнее» она к повышению уровня глюкокортикоидных гормонов в крови и тем быстрее дает сигнал к торможению стрессового ответа [11]. Известно, что выборочный нокдаун гена глюкокортикоидного рецептора у грызунов приводит к увеличению активности гипоталамо-гипофизарно-надпочечникового механизма, что приводит к снижению эффективности борьбы со стрессом [12], [13]. Наоборот, усиленная экспрессия гена глюкокортикоидного рецептора приводит к повышенной чувствительности клеток мозга в ответ на выработку глюкокортикоидов, что заставляет гипоталамо-гипофизарную систему уменьшать силу ответа на стресс [14].
Активность генов зависит от материнской заботы
Разберем некоторые особенно важные эпигенетические модификации (рис. 3). Пожалуй, главная из них — это метилирование ДНК, то есть, присоединение метильной групп к нуклеотиду цитозину в определенных регионах ДНК, так называемых CpG-островках. Метилирование заставляет ген «замолчать», то есть, запрещает его транскрипцию.
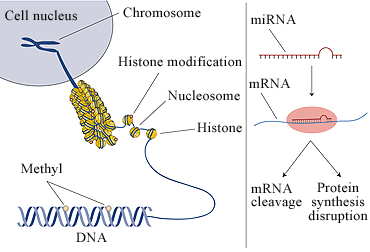
Рисунок 3. Варианты эпигенетических модификаций хроматина: ацетилирование гистонов, метилирование ДНК и регуляция транскрипции за счет РНК-интерференции.
Еще один тип эпигенетической регуляции — модификации гистонов, особых белков, необходимых для поддержания ДНК в порядке. ДНК — это очень длинная нить, которая неизбежно запутается, если ее на что-нибудь аккуратно не намотать. Роль таких «катушек для наматывания» и выполняют гистоны. Чтобы ДНК могла транскрибироваться, ей нужно на время размотаться с гистона. Модифицируя гистоны тем или иным способом, можно облегчить или затруднить разматывание ДНК и таким образом повлиять на транскрипцию гена. Одна из самых распространенных модификаций гистонов — ацетилирование (присоединение ацетильных групп к остаткам лизина); гены, гистоны которых ацетилированы, транскрибируются лучше. О других видах эпигенетической регуляции можно прочитать в статье «Развитие и эпигенетика, или история о минотавре» [1].
В поисках механизма, объясняющего разницу в ответе на стресс среди крыс, имеющих счастливое детство, и других, лишенных необходимой заботы, исследователи обратили внимание на регуляторную область глюкокортикоидного рецептора — экзон 17. С помощью бисульфитного секвенирования — методики, позволяющей определить метилирование ДНК, — ученые обнаружили разницу в метилировании нескольких цитозинов в составе экзона 17 в нейронах гиппокампа животных с разным эмоциональным опытом, полученным в детстве. У животных, окруженных заботой в детстве, цитозиновые остатки оказываются неметилированными — а значит, ген глюкокортикоидного рецептора активно транскрибируется. И действительно, у таких животных наблюдается повышенное количество соответствующей мРНК. Отсутствие метилирования коррелирует с высоким уровнем ацетилирования некоторых форм гистонов, которое, как известно, является маркером активного хроматина (см. выше). У животных, не получивших нужного ухода в детстве, напротив, наблюдалось метилирование цитозиновых остатков в экзоне 17 и сниженное количество экспрессируемой мРНК.
Может ли мачеха быть лучше родной мамы?
В доказательство того факта, что именно материнское поведение влияет на эпигенетические изменения в экзоне 17, был проведен следующий эксперимент: в период 12 часов после рождения потомство от заботливых матерей отдавали на воспитание менее заботливым и наоборот. Оказалось, что у детенышей, воспитанных заботливыми приемными матерями, отсутствие метилирования цитозинов в составе экзона 17 неотличимо от такового у детенышей, рожденных от заботливых матерей. В случае, если детеныш от заботливой матери попадал к равнодушной мачехе, наблюдались все те же изменения в метилировании, как если бы он был рожден и воспитан недобросовестной родной мамой.
Как заставить гены забыть прошлое
Если детенышу так уж не повезло в детстве, есть ли возможность изменить его стрессоустойчивость? Можно ли изменить молекулярные механизмы, происходящие в экзоне глюкокортикоидного рецептора? Исследователи утверждают, что ингибитор деацетилаз TSA приводит к повышению уровня ацетилирования гистонов в экзоне 17 глюкокортикоидного рецептора у потомства незаботливых матерей и, тем самым, увеличивает количество молекул фактора транскрипции NGFI-A, которые привлекаются к этому экзону и способствуют активации транскрипции гена. Наряду с этим, при обработке TSA происходит гипометилирование CpG-островков в этой же области, что также приводит к активации транскрипции. Однако нужно отметить, что при повышении уровня мРНК количество белка, субъединицы которого образуют глюкокортикоидный рецептор, не увеличивалось. Этот факт говорит о том, что влияние материнской заботы на формирование стрессоустойчивости значительно сложнее, чем просто влияние на метилирование нескольких цитозинов в экзоне. Тем не менее, исследования в этой области могут привести к изобретению лекарственных препаратов, с помощью которых можно корректировать негативный опыт, полученный в детстве.
Как эпигенетические изменения передаются из поколения в поколение
В дальнейших исследованиях (теперь уже проведенных на мышах) было показано, что тревожные расстройства и сниженную способность к ориентации на новых пространствах проявляли в основном самцы незаботливых матерей [15]. В то же время самки мышей лучше справлялись с заданиями и не демонстрировали депрессивного поведения [16]. Полагают, что это может быть связано с различным действием половых гормонов на организм, однако этот факт требует дальнейших проверок.
Отсутствие материнской заботы можно заменить, в экспериментальных целях, неожиданным отлучением детенышей от матери на ранних сроках вскармливания. В этом случае, вырастая во взрослых животных, они (в основном, самцы) будут проявлять все симптомы тревожного поведения. Исходя из этих фактов, ученые скрещивали самцов, подвергавшихся раннему стрессу из-за отсутствия материнской заботы (F1), с нерожавшими самками (считается, что первородящие самки — самые заботливые матери) и убеждались, что детеныши получают нормальный уход, растут и набирают вес в соответствии с нормами. Удивительно, что самки F2 проявляли все признаки тревожного поведения, которое корректировалось получением антидепрессантов. Самцы поколения F2, напротив, были активны и не демонстрировали повышенной тревожности. А вот потомки самцов F2 вновь демонстрировали поведенческое отчаяние и другие признаки депрессии (рис. 4). Почему именно самки F2, а не самцы, оказываются настолько уязвимыми для этого типа депрессии, пока не понятно, но видно, что такая депрессия наследуется в ряду поколений.
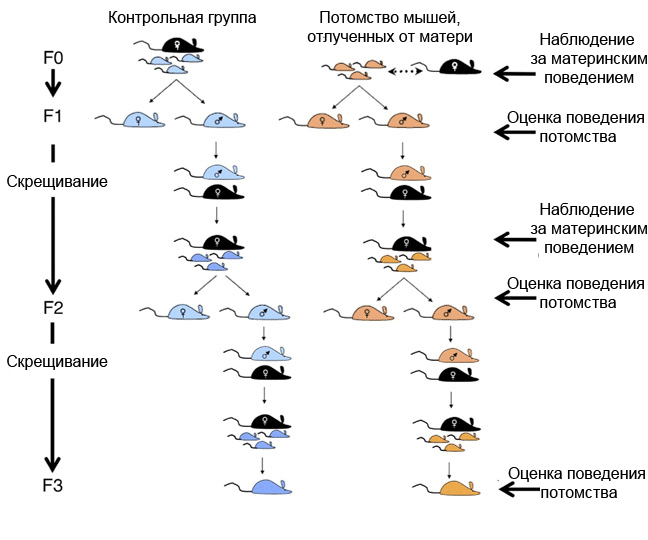
Рисунок 4. Изучение возможности передачи эпигенетических маркеров из поколения в поколение. Голубым цветом обозначены самцы (и их потомки) из группы животных, которых никогда не подвергали стрессу (контрольная группа). Коричневым показаны самцы из группы, самый старший дедушка которых был отлучен от матери в детском возрасте (экспериментальная группа). Черным показаны самки первородящих мышей, которых скрещивали с самцами контрольной и экспериментальной групп. Подробное описание эксперимента приводится в тексте.
В качестве молекулярного механизма, объясняющего влияние стресса, полученного в раннем детстве, на отсутствие стрессоустойчивости у взрослых животных, ученые вновь предлагают рассматривать эпигенетические изменения, в частности, изменение уровня метилирования некоторых генов как в половых клетках самцов, так и в клетках мозга их потомков.
Гиперметилирование CpG-островков в регуляторных регионах генов MeCP2, CB1 и гипометилирование регуляторной области гена CRFR2 приводили к уменьшению экспрессии мРНК этих генов. При этом не наблюдалось изменений в метилировании регуляторных областей генов серотонинового рецептора (играющего значительную роль в развитии депрессии) и моноамиоксидазы (катализирующей расщепление серотонина). Изменения уровней метилирования, происходящие одновременно в разных генах, позволяют полагать, что множество генов оказывает влияние на поведение особей.
Результаты этого исследования свидетельствуют о том, что постнатальный стресс оказывает влияние не только на детей, но и на более отдаленных потомков.
Эпигенетические механизмы у людей
Механизм нейрогормонального ответа на стресс у людей имеет много общего с реакцией на стрессовую ситуацию у животных. К настоящему моменту существуют исследования о взаимосвязи депрессивного поведения с негативным опытом раннего возраста не только для грызунов и нечеловекоподобных приматов, но и для человека. Существуют свидетельства того, что люди, подвергавшиеся стрессу в раннем возрасте , чаще страдают депрессией. Это связывают с усилением активности гипоталамо-гипофизарной системы в ответ на повышенную частоту стрессовых ситуаций в детстве [18].
Конечно, у людей все тоньше и сложнее поддается интерпретации. Возможно, на эпигенетику оказывает влияние не только сам стресс, но и воспоминания о нем; возможно, у разных людей эти воспоминания будут преуменьшены или преувеличены. В этом случае желательно исследовать людей, которые испытали стресс в столь раннем возрасте, что совершенно точно не могут о нем помнить. — Ред.
Для исследования этого вопроса использовали мозг людей, покончивших жизнь самоубийством [19]. Здесь нужно отметить, что авторы исследования вовсе не зашли так далеко, чтобы напрямую связывать стресс, полученный в детском возрасте, со склонностью к суициду (хотя существуют исследования, свидетельствующие в пользу этой гипотезы [20–22]). Отдавая должное роли психологического склада личности в совершении суицида, нужно понимать, что множество других факторов играет значительную роль в принятии решения покончить жизнь самоубийством. Однако базисом для этого решения может быть сниженная устойчивость к стрессовым ситуациям.
Среди покончивших жизнь самоубийством выделили две группы: людей, подвергавшихся неправильному обращению в детстве, и людей, у которых было нормальное полноценное детство. Предметом исследования вновь был экзон 1F гена глюкокортикоидного рецептора NR3C1, гомологичный экзону 17 регуляторной области гена глюкокортикоидного гена крыс. Интересно, что в клетках мозга у людей, подвергавшихся стрессу в раннем возрасте, наблюдалось увеличение уровня метилирования экзона 1F и уменьшение количества соответствующей мРНК . Кроме того, в этих случаях, наблюдалось снижение уровня связывания транскрипционного фактора NGFI-A, который считается ответственным за регуляцию экспрессии гена глюкокортикоидного рецептора. У людей, в детстве которых не было отмечено значительного негативного опыта, изменений в метилировании экзона 1F не наблюдалось. Этот факт говорит о том, что изменение уровня экспрессии генов глюкокортикоидного рецептора зависит именно от получения достаточной заботы в раннем возрасте, а не связан напрямую со склонностью к суициду .
К результатам по уровню мРНК, возможно, стоит отнестись скептически. Все, кто работают с мРНК, знают, что эти молекулы столь же нестабильны и склонны к деградации, сколь и важны для исследования. О сохранности мРНК в мозге человека через разное время после смерти существуют противоречивые сведения [23], [24]. Это заставляет с осторожностью интерпретировать вышеуказанные данные. — Ред.
Интересная закономерность касается связи между родительством и интеллектом. В недавней работе, являющейся результатом многолетних исследований, такой связи не выявлено вовсе. Судя по ней, интеллект зависит почти исключительно от генетики, а то, насколько много занимались с ребенком в детстве, оказывает на итоговый уровень интеллекта довольно слабое влияние [25]. — Ред.
Сейчас появляется все больше исследований, которые демонстрируют взаимосвязь между употреблением разных видов пищи, образом жизни и эпигенетическими изменениями ДНК не только в одном организме, но и у его потомства. Склонность к диабету и ожирению передается внучкам (именно девочкам) от дедушек-крыс, потреблявших пищу с высоким содержанием жиров. Причиной этого являются нарушение толерантности к глюкозе и нарушения в секреции инсулина, имеющие эпигенетический характер [26].
Существуют также данные о том, что кратковременное или даже однократное употребление алкоголя, никотина, кокаина, амфетамина или опиатов грызунами приводит к изменению экспрессии некоторых генов. Результатом таких изменений становится появление пристрастия к различным веществам [27]. Кроме того, известно, что потомки животных с измененной под влиянием кокаина экспрессией генов плохо обучаются, характеризуются снижением внимания и памяти, плохо ориентируются в пространстве [28].
Подводя итог вышесказанному, нужно отметить, что на данный момент обнаружены лишь единичные закономерности, которые указывают на связь между поведением и эпигенетическими изменениями в клетках живых организмов. Некоторые ученые скептически относятся к исследованиям в этой области еще и потому, что трудно грамотно поставить эксперимент, чтобы продемонстрировать, что никакие неожиданные факторы, кроме заявленных форм поведения, не влияют на изменения на молекулярном уровне. Не говоря о том, как непросто изучать поведение животных и человека. Сейчас большие надежды возлагаются на активно развивающиеся полногеномные методы, которые предоставляют огромные массивы данных об эпигенетических изменениях всех генов в геноме. Возможно, грамотный анализ этих данных поможет установить взаимосвязь между эпигенетическими изменениями и разнообразием поведенческих ответов.
Литература
- Развитие и эпигенетика, или История о Минотавре;
- Разнообразия много не бывает: чем занимаются мобильные элементы генома в мозге;
- Пилюли для эпигенома;
- Ian C G Weaver, Nadia Cervoni, Frances A Champagne, Ana C D'Alessio, Shakti Sharma, et. al.. (2004). Epigenetic programming by maternal behavior. Nat Neurosci. 7, 847-854;
- Dick F. Swaab, Ai-Min Bao, Paul J. Lucassen. (2005). The stress system in the human brain in depression and neurodegeneration. Ageing Research Reviews. 4, 141-194;
- James P. Herman, Michelle M. Ostrander, Nancy K. Mueller, Helmer Figueiredo. (2005). Limbic system mechanisms of stress regulation: Hypothalamo-pituitary-adrenocortical axis. Progress in Neuro-Psychopharmacology and Biological Psychiatry. 29, 1201-1213;
- Jinzhao Ji, Stephen Maren. (2007). Hippocampal involvement in contextual modulation of fear extinction. Hippocampus. 17, 749-758;
- La Bar and Disterhoft JF. (1998). Conditioning, awareness, and the hippocampus. Hippocampus 8, 620–606;
- David J. Mangelsdorf, Carl Thummel, Miguel Beato, Peter Herrlich, Günther Schütz, et. al.. (1995). The nuclear receptor superfamily: The second decade. Cell. 83, 835-839;
- ALLAN MUNCK, ROSEMARY FOLEY. (1979). Activation of steroid hormone–receptor complexes in intact target cells in physiological conditions. Nature. 278, 752-754;
- E. Ronald de Kloet, Erno Vreugdenhil, Melly S. Oitzl, Marian Joëls. (1998). Brain Corticosteroid Receptor Balance in Health and Disease1. Endocrine Reviews. 19, 269-301;
- M. P. Boyle, J. A. Brewer, M. Funatsu, D. F. Wozniak, J. Z. Tsien, et. al.. (2005). Acquired deficit of forebrain glucocorticoid receptor produces depression-like changes in adrenal axis regulation and behavior. Proceedings of the National Academy of Sciences. 102, 473-478;
- S. Ridder. (2005). Mice with Genetically Altered Glucocorticoid Receptor Expression Show Altered Sensitivity for Stress-Induced Depressive Reactions. Journal of Neuroscience. 25, 6243-6250;
- Holger M. Reichardt, François Tronche, Anton Bauer, Günther Schütz. (2000). Molecular Genetic Analysis of Glucocorticoid Signaling Using the Cre/loxP System. Biological Chemistry. 381;
- Tamara B. Franklin, Holger Russig, Isabelle C. Weiss, Johannes Gräff, Natacha Linder, et. al.. (2010). Epigenetic Transmission of the Impact of Early Stress Across Generations. Biological Psychiatry. 68, 408-415;
- Andrew Holmes, Anne Marie le Guisquet, Elise Vogel, Rachel A. Millstein, Samuel Leman, Catherine Belzung. (2005). Early life genetic, epigenetic and environmental factors shaping emotionality in rodents. Neuroscience & Biobehavioral Reviews. 29, 1335-1346;
- Raphaël Métivier, Rozenn Gallais, Christophe Tiffoche, Christine Le Péron, Renata Z. Jurkowska, et. al.. (2008). Cyclical DNA methylation of a transcriptionally active promoter. Nature. 452, 45-50;
- Christine Heim, Charles B Nemeroff. (2001). The role of childhood trauma in the neurobiology of mood and anxiety disorders: preclinical and clinical studies. Biological Psychiatry. 49, 1023-1039;
- Patrick O McGowan, Aya Sasaki, Ana C D'Alessio, Sergiy Dymov, Benoit Labonté, et. al.. (2009). Epigenetic regulation of the glucocorticoid receptor in human brain associates with childhood abuse. Nat Neurosci. 12, 342-348;
- M J Webster, M B Knable, J O'Grady, J Orthmann, C S Weickert. (2002). Regional specificity of brain glucocorticoid receptor mRNA alterations in subjects with schizophrenia and mood disorders. Mol Psychiatry. 7, 985-994;
- Alan F. Schatzberg, Anthony J. Rothschild, Philip J. Langlais, Edward D. Bird, Jonathan O. Cole. (1985). A corticosteroid/dopamine hypothesis for psychotic depression and related states. Journal of Psychiatric Research. 19, 57-64;
- Isometsä E.T., Henriksson M.M., Aro H.M., Heikkinen M.E., Kuoppasalmi K.I., Lönnqvist J.K. (1994). Suicide in major depression. Am. J. Psychiatry 151, 530–536;
- Barbara K. Lipska, Amy Deep-Soboslay, Cynthia Shannon Weickert, Thomas M. Hyde, Catherine E. Martin, et. al.. (2006). Critical Factors in Gene Expression in Postmortem Human Brain: Focus on Studies in Schizophrenia. Biological Psychiatry. 60, 650-658;
- Marielle Heinrich, Katja Matt, Sabine Lutz-Bonengel, Ulrike Schmidt. (2007). Successful RNA extraction from various human postmortem tissues. Int J Legal Med. 121, 136-142;
- Kevin M. Beaver, Joseph A. Schwartz, Mohammed Said Al-Ghamdi, Ahmed Nezar Kobeisy, Curtis S. Dunkel, Dimitri van der Linden. (2014). A closer look at the role of parenting-related influences on verbal intelligence over the life course: Results from an adoption-based research design. Intelligence. 46, 179-187;
- Sheau-Fang Ng, Ruby C. Y. Lin, D. Ross Laybutt, Romain Barres, Julie A. Owens, Margaret J. Morris. (2010). Chronic high-fat diet in fathers programs β-cell dysfunction in female rat offspring. Nature. 467, 963-966;
- Chloe C. Y. Wong, Jonathan Mill, Cathy Fernandes. (2011). Drugs and addiction: an introduction to epigenetics. Addiction. 106, 480-489;
- Fang He, Irina A. Lidow, Michael S. Lidow. (2006). Consequences of paternal cocaine exposure in mice. Neurotoxicology and Teratology. 28, 198-209.








