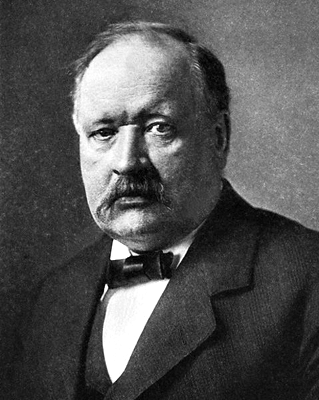Тот, кто придумал ионы
24 мая 2015
Тот, кто придумал ионы
- 845
- 0
- 0
-
Автор
-
Редактор
Нашего героя принято считать соперником и ненавистником Менделеева. Однако в этой истории не всё до конца ясно. Что точно можно сказать — это был один из разностороннейших химиков мира. Он «придумал» ионы и получил «нобеля» за свою диссертацию, которую с трудом пропустил диссертационный совет. Он применил законы физики и химии к биологии, он занимался парниковым эффектом и шаровыми молниями... В общем, встречайте — Сванте Аррениус, третий нобелевский лауреат по химии. Формулировка Нобелевского комитета: «в знак признания особого значения его теории электролитической диссоциации для развития химии».

Рисунок 1. Эрик Эдлунд (1819–1888). Шведский физик, известный трудами по теории электричества. Иностранный член-корреспондент Петербургской академии наук. Занимался индукцией, телеграфией, дуговыми лампами; разработал теорию атмосферного электричества для объяснения феномена полярного сияния.

Рисунок 2. Вильгельм Фридрих Оствальд (1853–1932). Немецкий химик и философ, лауреат Нобелевской премии по химии 1909 года — за изучение природы катализа и основополагающие исследования скоростей химических реакций. Его имя носит закон разбавления. Основал первый в мире физико-химический институт (при Лейпцигском университете), активно содействовал международному обмену научной информацией. Считал материю формой проявления энергии.
Герой нашего сегодняшнего рассказа, судя по всему, был очень непростым человеком. Впрочем, кто из нобелевских лауреатов прост? С другой стороны, этот человек не просто получил Нобелевскую премию по химии 1903 года за свою докторскую (по-нашему — кандидатскую) диссертацию; без ссылок на него не обходится ни один школьный или университетский курс химии. Он — один из основоположников химической науки ХХ века, даже несмотря на конфликты с великим Менделеевым. Считается, что впоследствии именно он помешал Дмитрию Ивановичу получить Нобелевскую премию. Хотя с точки зрения современной химии они оба были неправы и правы одновременно. Речь сегодня пойдет о первом в истории нобелиате — земляке Нобеля, Сванте Августе Аррениусе.
Будущий лауреат родился в достаточно богатой и образованной семье. Его дядя, Иоанн (Юхан) Аррениус, — известный ботаник, деятель сельского хозяйства и агроном. Отец был управляющим имением и вскорости стал членом совета инспекторов Уппсальского университета. Так что ребенку было в кого рано развиваться: пишут, что он уже в младенчестве любил складывать циферки из папиных отчетов (правда, не сообщается, делал ли он что-либо с самими листами: я как отец не по годам развитой девочки подозреваю, что за интерес к цифрам Сванте иногда влетало). Достаточно легко Сванте окончил Уппсальский университет (физика и химия), в 1878 году получил степень бакалавра, а в 1881 уехал в столицу, в Шведскую королевскую академию наук, заниматься изучением электричества под руководством Эрика Эдлунда (который, кроме того, организовал систему метеорологических наблюдений в Швеции).
Своему докторанту Эдлунд (рис. 1) предложил заняться изучением электролитов. К тому времени сам по себе электрический ток был, конечно, хорошо известен, хотя электрон еще не открыли, и природа этого явления была до конца не ясна. С другой стороны, физики и химики уже прекрасно знали, что, к примеру, кристаллы поваренной соли ток не проводят, дистиллированная вода — тоже. А вот раствор NaCl — прекрасный проводник. В чем тут дело? По мнению Аррениуса, изложенному в его докторской диссертации (увидевшей свет в 1884 году), в растворе некоторые вещества, нейтральные сами по себе, распадаются, взаимодействуя с растворителем, на положительно и отрицательно заряженные ионы. Та же соль NaСl распадается на ион Na+ и ион Cl−.
Мнение оказалось настолько революционным, что диссертация, к которой формально придраться было нельзя, была защищена с самой низкой оценкой — она прошла по четвертому классу, без права преподавания в университете [1]. Кстати, именно поэтому существовал вариант, при котором Аррениус мог бы стать первым российским нобелевским лауреатом по химии: его старший коллега, которому Аррениус прислал свою статью, пригласил его работать к себе, в Лифляндскую губернию Российской империи, в Рижское политехническое училище. Аррениус отказал (да и потом, в 1909 году, уже будучи нобелиатом и работая в Нобелевском комитете, сомневался, принимать ли номинацию своего тогдашнего «благодетеля»). Правда, в 1909 году Вильгельм Фридрих Оствальд (рис. 2) уже давно жил и работал в Лейпциге.
Кстати, сам Оствальд вначале не мог принять теорию электролитической диссоциации. «Я провел лихорадочную ночь со скверными снами», — писал он про лето 1884 года. — «У меня одновременно появились жестокая зубная боль, новорожденная дочка и статья Аррениуса “Исследования по проводимости электролитов”. То, что было написано в работе, настолько отличалось от привычного и известного, что я сначала был склонен всё в целом принять за бессмыслицу».
Но останься Аррениус в России, ему бы тоже пришлось несладко: яростным противником его теории электролитической диссоциации оказался сам Дмитрий Иванович Менделеев (рис. 3).

Рисунок 3. Дмитрий Иванович Менделеев (1834 1927). Семнадцатый (!) ребёнок в семье директора Тобольской гимназии. Русский «универсальный мозг»: химик, физик, экономист, геолог и ещё много кто. Самое известное открытие — периодический закон химических элементов. На вопрос журналиста о «кухне» открытия периодической системы Менделеев ответил: «...Не пятак за строчку! Не так, как вы! Я над ней, может, двадцать пять лет думал...». Создал точную теорию весов, впервые обобщил информацию по неорганической химии в труде «Основы химии». Ярый борец с модным в то время спиритизмом. Педагог, который старался экспериментировать во всём, вплоть до совершения самостоятельного полета на воздушном шаре — с научными целями. Считал, что «профессор, который только читает курс, а сам не работает в науке и не двигается вперед, — не только бесполезен, но прямо вреден». Менделеев подвел итог своей научной жизни так: «Всего более четыре предмета составили моё имя: периодический закон, исследование упругости газов, понимание растворов как ассоциации и „Основы химии“. Тут моё богатство. Оно не отнято у кого-нибудь, а произведено мною...» Иностранные (а не отечественные!) ученые выдвигали Менделеева на Нобелевскую премию три раза. Считается, что в 1906-м Нобелевский комитет уже присудил ее Менделееву, но Шведская королевская Академия наук не утвердила решение под влиянием С. Аррениуса. В следующем году ½ премии русскому гению всё же готовились отдать, но до сего события он не дожил...

Рисунок 4. Якоб Хенрик Вант-Гофф (1852–1911). Голландский химик, один из основателей стереохимии и физической химии. Удостоился первой «химической» Нобелевской премии — за открытие законов химической динамики и осмотического давления в растворах.

Рисунок 5. Анри Муассан (1852–1907). Лауреат Нобелевской премии по химии 1906 года — в основном за исследование и выделение фтора. Получил свободный фтор и различные его соединения, обнаружил в аризонском метеорите и описал новый минерал (муассанит), состоящий из карбида кремния.
Создатель периодической системы был автором собственной теории растворов и протестовал против того, что Аррениус не учитывал ни сольватации — взаимодействия ионов с молекулами растворителя, — ни электростатического взаимодействия между ионами в случае концентрированных растворов. Любопытнее всего, что созданная после смерти и Менделеева, и Аррениуса протонная теория кислот и оснований в итоге примирила «врагов», вобрав в себя положения как Аррениуса, так и Менделеева. Нобелевская премия Аррениуса, кстати, оказалась «чистой победой»: из 23 номинаций на премию 1903 года Аррениус занял чистое первое место 11 раз. Другими претендентами были: англичанин сэр Уильям Рамзай (премия 1904 года), француз Анри Муассан (1906), немец Адольф фон Байер (1905), американский химик Хармон Морзе и француз Марселен Бертло (тоже получил бы своего «нобеля», если бы не умер в 1907 году — Бертло номинировали общим количеством 11 раз).
Нужно обязательно отметить и еще два момента, связанные с Аррениусом и Нобелевскими премиями. Начнем в хронологическом порядке, с 1901 года. А точнее, еще раньше. В конце XIX века Аррениус, наряду с доработками своей теории, занимается и осмотическим давлением. «Классиком» работ по осмосу был голландец Якоб Вант-Гофф (рис. 4) с его классической формулой PV=iRT. (Тут P — осмотическое давление вещества в растворе, Т — температура, R — универсальная газовая постоянная, а i — эмпирический коэффициент, сейчас называемый коэффициентом Вант-Гоффа, или изотоническим коэффициентом.) Однако Вант-Гофф никак не мог объяснить, почему для растворенных газов, к примеру, i равен единице, а вот для солей коэффициент становится больше. Работы Аррениуса помогли Вант-Гоффу понять, что i связан с количеством частиц в растворе, а поскольку соли распадаются (диссоциируют) на ионы, коэффициент возрастает. В итоге Вант-Гофф стал самым первым нобелевским лауреатом в истории (1901 год).
Второй момент относится к 1906 году. К тому времени Аррениус уже вышел в отставку с поста ректора Стокгольмского университета и стал директором физико-химического Нобелевского института. Пишут, что в 1906 году Нобелевский комитет предварительно вынес решение в пользу Менделеева, однако ненавидевший соперника Аррениус запротестовал и заставил поменять решение в пользу молодого Анри Муассана (рис. 5).
Справедливости ради отметим, что я слышал и другое объяснение этой истории: комитет решил, что Менделееву можно дать премию и в следующем году, а Муассан — парень «молодой», изувеченный фтором, и ему премия нужнее. Что я могу утверждать совершенно точно, так это то, что Менделеев и Аррениус друг друга действительно не любили, а счет по номинациям в 1906 году у нашего соотечественника и Анри Муассана был 4:8, а также то, что в 1907 году не стало и Менделеева, и Муассана. И еще одно могу сказать точно: на первом конгрессе памяти Менделеева в 1907 году в Петербурге Аррениус был почетным гостем (рис. 6).

Рисунок 6. Аррениус на I Менделеевском съезде (первый ряд, третий слева). Съезд проходил с 20 по 30 декабря 1907 г. в Санкт-Петербурге. Работали отделения химии (рассматривались вопросы общей и прикладной науки), агрохимии, физики, биологии и гигиены.
Как бы то ни было, нельзя не отметить энциклопедичность и прозорливость Аррениуса. Ведь именно он впервые увязал рост температуры на планете с содержанием углекислого газа в атмосфере (к этому выводу он пришел, изучая ледниковые периоды) [2]. Аррениус оформил в стройную научную гипотезу и дополнил расчетами предположения других ученых о панспермии — переносе зародышей живых организмов через космос. Он пытался объяснить природу полярных сияний, солнечной короны и шаровой молнии, изучить вулканы методами физической химии. И давайте уже ответим на вопрос, что делает кондовый физхимик на биомолекуле?
Даже если опустить тот факт, что именно Аррениусом были введены такие замечательные понятия, как ионы — а какую роль играют ионы в нашей с вами биохимии, мне объяснять не надо — и энергетический барьер реакции, если забыть о роли осмоса в биологических процессах, останется тот факт, что Аррениус был одним из пионеров иммунохимии и посвятил этой теме целую монографию, затронув в ней и физико-химию токсинов и антитоксинов [3]. Именно Аррениус показал, что нет никакой принципиальной разницы между реакциями, над которыми химики работают в своих колбах, и теми, которые идут внутри живых организмов. И в предисловии к книге «Quantitative laws in biological chemistry» он написал: «Физики и химики пришли к заключению, что те биологические теории, которые еще пользуются признанием в медицинских кругах, основаны на совершенно неправильных взглядах и должны быть заменены другими представлениями, согласующимися с основными законами общей химии» [4].
А вот со здоровьем Сванте Аррениусу не повезло. Он рано начал набирать вес, страдал одышкой; однажды на входе на какую-то конференцию или конгресс швейцар сказал ему, что мясники заседают в соседнем здании. Как итог — 67 лет жизни (большинство нобелиатов прожили намного дольше), короткая болезнь и смерть. Печально, но тем не менее успел Аррениус очень много. В конце концов, не каждый химик и даже не каждый нобелевский лауреат может похвастаться тем, что его открытия изучают в школе — даже сейчас, когда прошло более века с того дня, когда они были сделаны.
Первый вариант статьи был опубликован в блоге автора на сайте Политехнического музея [5].
Литература
- Arrhenius S. Recherches sur la conductivité galvanique des électrolytes. Doctoral dissertation. Royal publishing house, P.A. Norstedt & söner, Stockholm, 1884;
- Arrhenius S. (1896). On the influence of carbonic acid in the air upon the temperature of the ground. Philos. Mag. J. Sci. 41, 237–276;
- Arrhenius S. Immunochemistry. New York: Macmillan, 1907;
- Arrhenius S. Quantitative laws in biological chemistry. London: G. Bell, 1915;
- Паевский А. «Соперник Менделеева». Сайт политехнического музея..