Победа над диабетом? Разбор нового гибридного пластыря с микроиглами
25 февраля 2021
Победа над диабетом? Разбор нового гибридного пластыря с микроиглами
- 1690
- 0
- 2
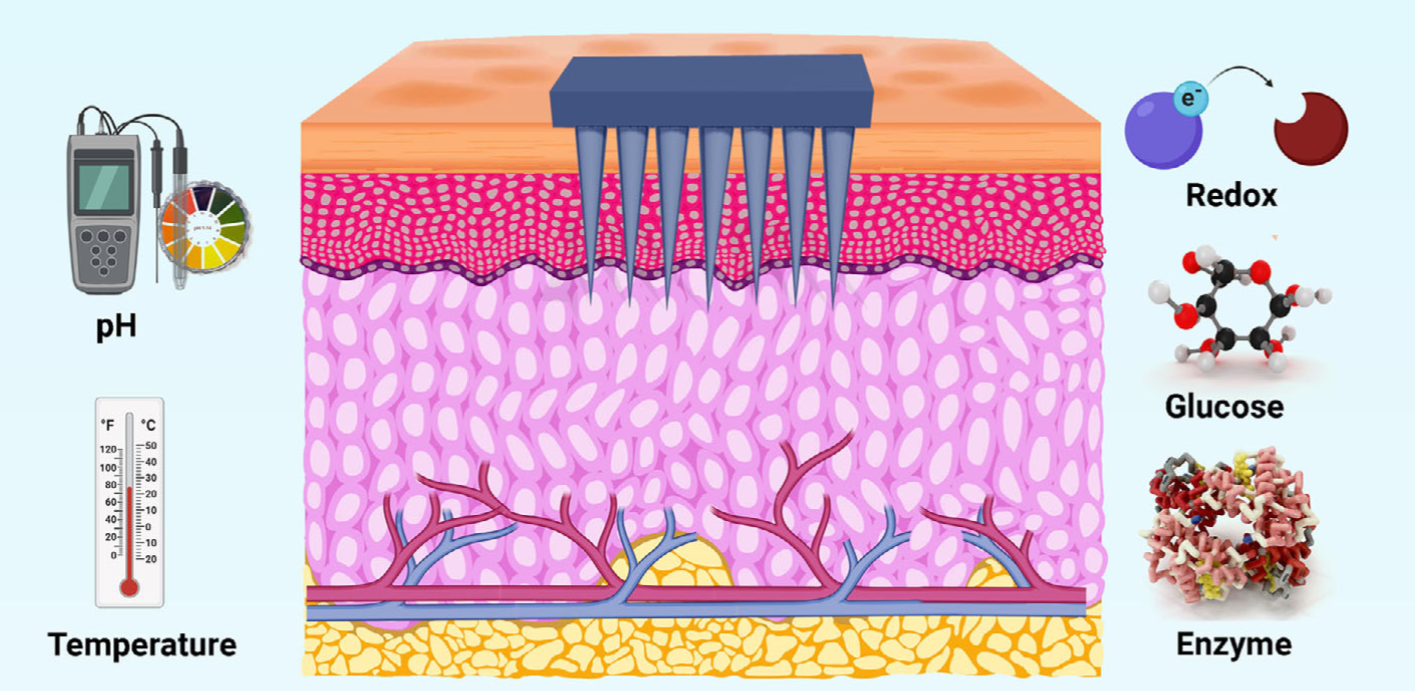
Так выглядит пластинка безболезненного пластыря с микроиглами, через которые вводятся нужные биоактивные вещества.
Рисунок в полном размере.
-
Авторы
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: В 2020 году биоинженеры разработали гибридный пластырь, который уравновешивает действие инсулина и глюкагона, не требует контроля человека и не причиняет боли при использовании. Как он работает и есть ли у пластыря недостатки?
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2020/2021.

Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.

Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
По данным ВОЗ, в 2014 году насчитывалось 422 млн пациентов с диагнозом «сахарный диабет». В течение последних 34 лет рост числа пациентов был непрерывен, поэтому сегодня число заболевших может приближаться к полумиллиарду (рис. 1). До сих пор у нас нет не только методов лечения самых распространённых типов сахарного диабета, но и эффективных способов борьбы с его симптомами — последствиями избытка глюкозы в крови (гипергликемией) . Проявления частой гипергликемии начинаются с упадка сил и нарушений сна, а заканчиваются утратой остроты зрения у 90% диабетиков, омертвением тканей ног, нарушениями работы почек, сердца и мозга. Чтобы миллионы людей могли оставаться активными как можно дольше, важно разрабатывать новые способы регулировать уровень глюкозы в крови.
О разных типах диабета, причинах их возникновения и возможных способах лечения рассказано в некоторых статьях на «Биомолекуле»: «Сахарный диабет I типа, или Охота на поджелудочную железу», «Кровавая драма на островке Лангерганса, или Как новооткрытая химера T- и В-клеток подстрекает аутоиммунный ответ при диабете I типа», «Кардиопротекция при сахарном диабете» [1–3].
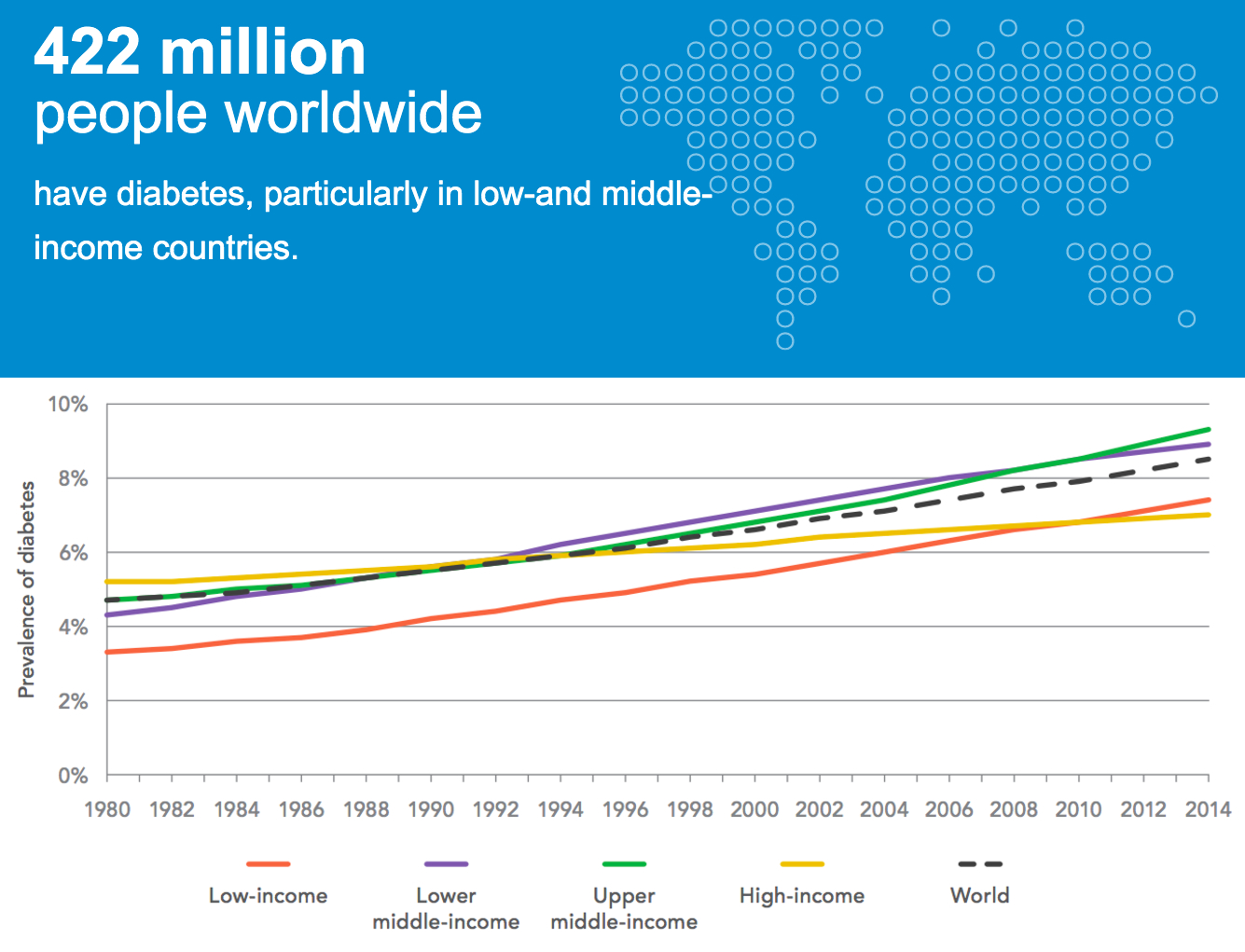
Рисунок 1. По данным ВОЗ, в 2014 году людей с сахарным диабетом было около 422 миллионов. Ускоряется рост их числа в странах с бедным и небогатым населением, как свидетельствует график в нижней части рисунка. Судя по тому, что рост не прекращается, сегодня людей с диабетом в мире может быть уже около 500 миллионов.
Что не учитывают, пытаясь помочь человеку с диабетом?
У каждого из нас при переваривании пищи большие порции глюкозы всасываются в кровь: возникает кратковременная гипергликемия, но в ответ на неё почти моментально секретируется инсулин. К тому времени он уже синтезирован бета-клетками островков Лангерганса (особых групп клеток внутри поджелудочной железы, секретирующих гормоны). Из-за увеличения концентрации глюкозы возникает последовательность сигналов внутри бета-клеток, что запускает секрецию готового к подвигам инсулина. Он снижает уровень глюкозы, стимулируя ее поглощение из крови. У больных диабетом обычно выделяется недостаточное для нормальной регуляции сахара в крови количество инсулина.
Но даже грамотная диета и постоянные инъекции инсулина не спасают от осложнений сахарного диабета и их последствий — смертей. Проблема в том, что назначаемые дозы инсулина часто несоразмерны ситуации. И если инсулина становится слишком много, наступает гипогликемия. В норме уровень глюкозы повышается глюкагоном, но часто при нарушении работы бета-клеток островков Лангерганса, секретирующих инсулин, ломаются и соседние альфа-клетки, производящие глюкагон [4–6]. Если выделяется недостаточно глюкагона, то во время резкого падения концентрации глюкозы (после щедрой инъекции инсулина, например) первым отключается остро зависимый от нее мозг. Так начинается гипогликемическая кома. Если же глюкагона секретируется избыточное количество, то гипергликемия будет только тяжелее, чем без его вмешательства — печень, стимулируемая глюкагоном, будет дополнительно вбрасывать глюкозу в кровь. Первая рекомендация человеку с диабетом — соблюдение специальной диеты и регулярное питание, чтобы сгладить колебания уровня сахара и других веществ путем контроля за их поступлением извне. Однако при нарушениях секреции глюкагона одной диеты недостаточно. Это связано с тем, что печень будет выделять глюкозу в кровь в ответ на выброс глюкагона независимо от поступления веществ из пищеварительной системы, а значит, наши возможности внешнего контроля здесь ограничены.
Если противодействовать сахарному диабету инъекциями инсулина догадались век назад, то о катастрофическом эффекте связи соседних клеток островков Лангерганса между собой сообщили только в 1970-е годы; активно изучать инсулин начали на рубеже веков, однако многое до сих пор остается неизвестным. Сейчас инсулин готовы прописать каждому пациенту с диабетом, но этого часто недостаточно. Необходимы саморегулирующиеся системы, которые выделяют в организм гормоны с противоположным друг другу действием в ответ на изменения концентрации глюкозы. Идеально, если такие системы будут удобными в использовании и безболезненными, вроде пластыря: прилепил и пошел (рис. 2) [7].

Рисунок 2. Фотография пластинки чувствительного к глюкозе пластыря с инсулином в микроиглах высотой 700 мкм
Реализовать идею гибридного пластыря решили ученые из Лос-Анджелеса: они создали пластырь, который искусно противодействует проявлениям диабета [8]. Коллеги Зэцзюнь Ван и Цзиньцян Ван, работающие в Калифорнийском университете, уже патентуют свою разработку. Ради будущего, в котором человеку с диабетом для полноценной жизни взамен постоянных проверок крови на сахар и уколов или автоматических дозаторов инсулина нужен лишь пластырь, хочется жить. В статье мы расскажем о принципах работы нового пластыря и его преимуществах по сравнению с другими способами регулирования уровня глюкозы.
Изготовление и работа гибридного пластыря
Регуляция высвобождения гормонов невозможна без постоянного контакта с внутренней жидкой средой организма. На поверхности пластыря, прилегающего к коже, расположены сотни так называемых микроигл — под микроскопом они выглядят как вытянутые вверх пирамидки высотой меньше миллиметра (рис. 3) [7].

Рисунок 3. Так микроиглы выглядят под сканирующим электронным микроскопом. Длина черной линии соответствует масштабу в 500 мкм
Ширина оснований игл — 300 микрометров — приблизительно равна диаметру самых тонких, безболезненных игл, которыми делают микроинъекции при контурной пластике. На фоне же обычных игл шприцов микроиглы выглядят как пассажиры Боинга 747 на фоне самолета (рис. 4А). Однако размеры (их длина 700 мкм) позволяют микроиглам проникать в живую ткань кожи — дерму (рис. 4Б) [9]. Находясь в контакте с межклеточной жидкостью дермы, они воспринимают изменения концентрации глюкозы, которые соответствуют изменениям в плазме крови. При этом микроиглы не раздражают болевые рецепторы, залегающие глубже, что делает применение пластыря безболезненным.
В форме микроигл застыл полимеризованный матрикс — сеть молекул, в которой скрыты гормоны. Тесная связь всех компонентов способствует взаимодействиям между содержимым пластыря и глюкозой, чтобы постоянно регулировать постепенное высвобождение гормонов, а не выделять все активные вещества за один раз. С переходом воды из дермы компоненты начинают взаимодействовать между собой: они притягивают молекулы гормона или, наоборот, позволяют им активно растворяться, удерживая их слабее. Инсулин активно высвобождается в ответ на повышение уровня глюкозы в межклеточной жидкости; глюкагон выходит из своих игл при снижении сахара (рис. 5).
Критика
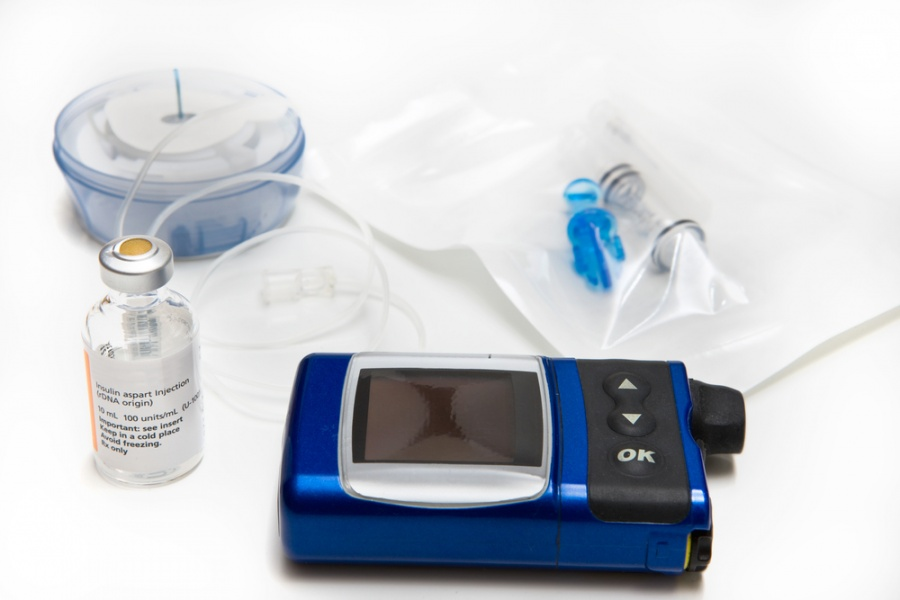
Идея нового гибридного пластыря хороша, однако ей далеко до практического применения: пока все результаты были получены на мышах; впереди — совершенствование технологии и клинические испытания. Нужно ли это, если уже сейчас широко применяются довольно продвинутые автоматические дозаторы инсулина — так называемые инсулиновые помпы? Дозаторы сообщаются с подкожной клетчаткой человека с помощью гибких катетеров, которые постоянно измеряют уровень сахара и при его повышении впрыскивают инсулин в растворенной форме (рис. 6). Мы решили сравнить действие пластыря и помпы, чтобы понять, насколько эффективна новая система на фоне уже существующих, и вообще критически оценить ее.
Прежде всего, помпы регулируют только уровень инсулина, никак не компенсируя частые нарушения секреции глюкагона. И лучшее, что хорошая помпа может сделать, когда нужен глюкагон — просто отключиться и не вмешиваться. (Это запрограммировано на случай резкой гипогликемии во сне — когда человек не может отреагировать, съев «рафаэлку»). Конечно, регуляция уровня глюкозы в крови с помощью пластыря, который выделяет гормоны для уравновешивания резкости действий друг друга, оказывается более сбалансированной, чем действие системы, которая выделяет лишь один из гормонов (рис. 7). К слову, исследователи экспериментировали с пластырями, в которых микроиглы содержали только один гормон — результат каждый раз выходил менее удачным, чем у гибридного варианта [8]. Кроме того, дозатор помпы может сломаться и тем самым навредить здоровью человека. Пластырь же настолько прост по своему устройству, что лишен таких рисков.
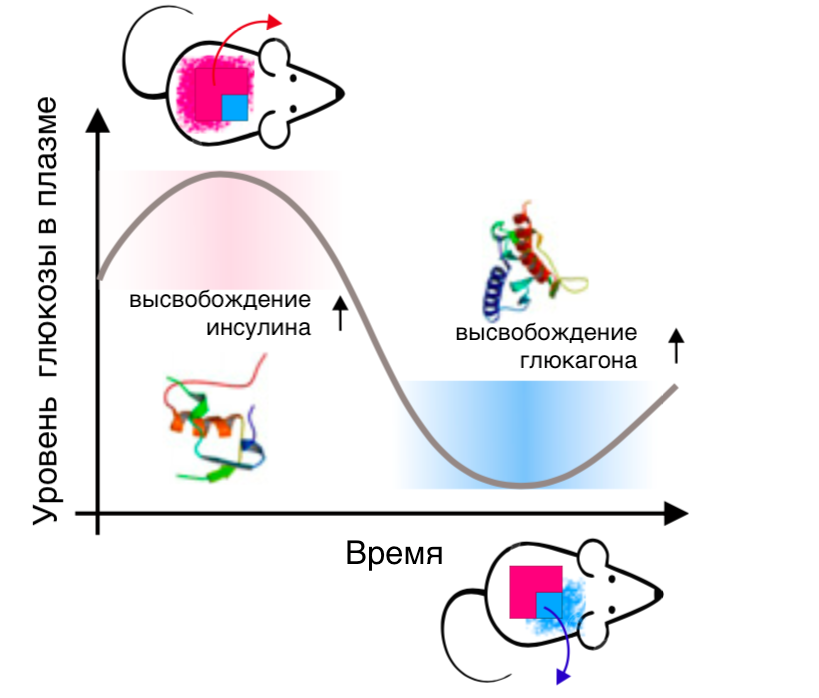
Рисунок 7. Высвобождение гормона из микроигл уравновешивает эффекты антагониста при избытке в крови последнего. При повышении уровня глюкозы высвобождается инсулин, при понижении — глюкагон.
Не будем забывать и о качестве жизни людей с диабетом. Даже помпа — передовая технология — снижает качество жизни: постоянно введенный катетер ограничивает возможности передвижений. О пластыре человеку гораздо легче забыть на весь день. Для полного комфорта осталось только защитить пластырь от поступления воды извне, чтобы пациент мог принимать душ или плавать, не боясь того, что контакт пластыря с водой может привести к сбоям в выделении гормонов из микроигл.
Однако радость от новой технологии не помешает рассмотреть ее недостатки. И главным из них кажется кратковременность эффективного действия пластыря в экспериментах. Ученые тестировали систему, чередуя экстремально высокие и низкие уровни сахара, и сообщили, что пластырь нормально работает в течение трех таких циклов-чередований. Однако, как видно из графиков, уже после полутора циклов (т.е. после трех перемен условия), высвобождается значительно меньше гормонов, чем в начале (рис. 8). Условно можно приравнять такой цикл ко времени между приемами пищи. Таким образом, из экспериментов следует, что пластырь эффективно работает не более половины дня, а дальше его эффективность может уменьшаться из-за снижения объема выделяемых гормонов. Однако в экспериментах концентрация глюкозы менялась в 8 раз — в действительности у пациентов с диабетом колебание уровня сахара в крови значительно меньше, поэтому одного пластыря вполне может быть достаточно на весь день.
Помпа же уступает пластырю тем, что использует растворенный инсулин, и его срок хранения относительно короткий. В микроиглах пластыря до его применения гормоны находятся в сухом состоянии: в таком виде они хранятся достаточно долго и без особых условий.
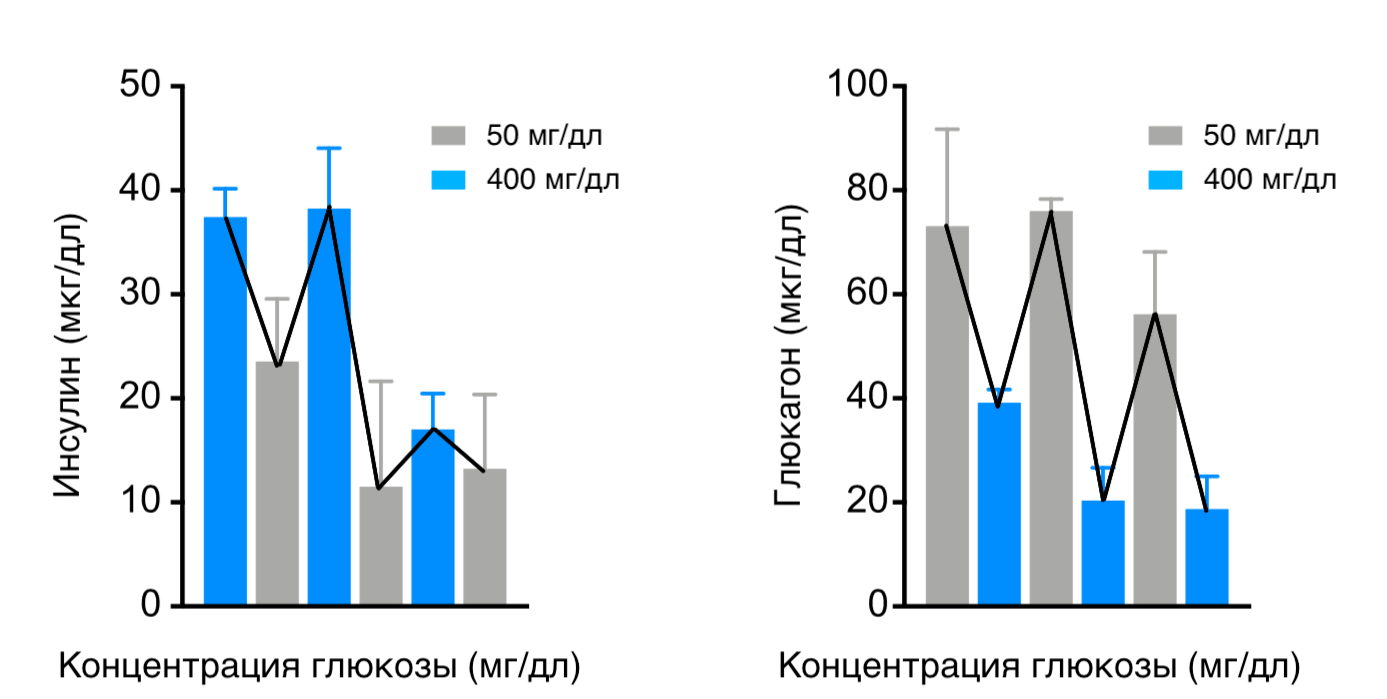
Рисунок 8. Изменение количества выделяемого микроиглами гормона в зависимости от частоты перепадов концентрации глюкозы. Инсулин — слева, глюкагон — справа. Голубым цветом обозначено количество выделенных гормонов при повышении сахара, серым цветом — при понижении. Каждый раз при повышении уровня глюкозы выделяется больше инсулина и меньше глюкагона; при понижении уровня глюкозы — больше глюкагона и меньше инсулина. Первые три столбика на каждой диаграмме значительно отличаются по высоте от других схожих с ними по цвету, то есть количество гормонов, высвобождаемое в одних и тех же условиях, в процессе использования быстро снижается. Возможно, это значит, что пластыря будет хватать ненадолго: если принять цикл повышения-снижения сахара (два соседних столбика) к циклу, который наш организм проходит между приёмами пищи, окажется, что пластыря будет хватать всего на половину дня.
Огорчает и то, что все же коже необходимо время на восстановление после такого пластыря с микроиглами (рис. 9). Предварительная рекомендация: применять пластырь стоит не чаще раза в неделю на одном месте. Правда, основана она на том, что после использования одного пластыря за неделю воспаление, заметное в первый и третий день после применения, сходит на нет (в другие дни исследователи наблюдений не делали). Однако не сообщается, что будет спустя несколько повторений.
Похожие на новую разработку пластыри с микроиглами уже применялись для безболезненной вакцинации, но это воздействие было однократным (рис. 10). Впрочем, радует проверенная безвредность веществ, составляющих бесследно растворяющийся матрикс микроигл. А менять участки тела в любом случае приходится всем пациентам: и тем, кто пользуется инъекциями, и тем, кто пользуется дозаторами.

Рисунок 10. Вакцинация с помощью пластыря с микроиглами. Так может выглядеть и применение гибридного пластыря.
сайт Horizons
Подводя итоги, хочется сказать, что гибридный пластырь с микроиглами кажется потенциально куда более простым в использовании, чем все прежние способы регулирования уровня глюкозы в крови у людей с диабетом. Однако надеемся, что это просто очередная остановка, на которой мы пережидаем время для появления доступных лекарственных препаратов, воздействующих на саму причину диабета: нарушения работы или гибель бета-клеток, секретирующих инсулин.
Литература
- Сахарный диабет I типа, или Охота на поджелудочную железу;
- Кровавая драма на островке Лангерганса, или Как новооткрытая химера T- и В-клеток подстрекает аутоиммунный ответ при диабете I типа;
- Кардиопротекция при сахарном диабете;
- Jesper Gromada, Pauline Chabosseau, Guy A. Rutter. (2018). The α-cell in diabetes mellitus. Nat Rev Endocrinol. 14, 694-704;
- Gina L.C. Yosten. (2018). Alpha cell dysfunction in type 1 diabetes. Peptides. 100, 54-60;
- Walter A. Müller, Gerald R. Faloona, Eugenio Aguilar-Parada, Roger H. Unger. (1970). Abnormal Alpha-Cell Function in Diabetes. N Engl J Med. 283, 109-115;
- Jicheng Yu, Jinqiang Wang, Yuqi Zhang, Guojun Chen, Weiwei Mao, et. al.. (2020). Glucose-responsive insulin patch for the regulation of blood glucose in mice and minipigs. Nat Biomed Eng. 4, 499-506;
- Zejun Wang, Jinqiang Wang, Hongjun Li, Jicheng Yu, Guojun Chen, et. al.. (2020). Dual self-regulated delivery of insulin and glucagon by a hybrid patch. Proc Natl Acad Sci USA. 117, 29512-29517;
- Rezvan Jamaledin, Pooyan Makvandi, Cynthia K. Y. Yiu, Tarun Agarwal, Raffaele Vecchione, et. al.. (2020). Engineered Microneedle Patches for Controlled Release of Active Compounds: Recent Advances in Release Profile Tuning. Adv. Therap.. 3, 2000171;
- Mina Rajabi, Niclas Roxhed, Reza Zandi Shafagh, Tommy Haraldson, Andreas Christin Fischer, et. al.. (2016). Flexible and Stretchable Microneedle Patches with Integrated Rigid Stainless Steel Microneedles for Transdermal Biointerfacing. PLoS ONE. 11, e0166330.