
По карте интерактома можно найти неожиданные связи между болезнями
12 марта 2015
По карте интерактома можно найти неожиданные связи между болезнями
- 421
- 0
- 0
Опасные связи в пляске смерти: болезнь, как и беда, не приходит одна. Но теперь есть возможность выявить сцепки в хороводе патологий и подумать, как избавиться от нескольких «танцоров» разом.
Рисунок в полном размере.
-
Автор
-
Редактор
Даже из неполной карты интерактома (схемы молекулярных взаимодействий в клетке), доступной на данный момент, можно извлечь полезную информацию о связях между болезнями. Кластеры белков, участвующих в патогенезе различных заболеваний, на карте интерактома могут располагаться на разном удалении друг от друга и даже перекрываться. Расстояние между кластерами отражает сходство симптомов болезней, а также вероятность того, что обе болезни разовьются у одного человека.
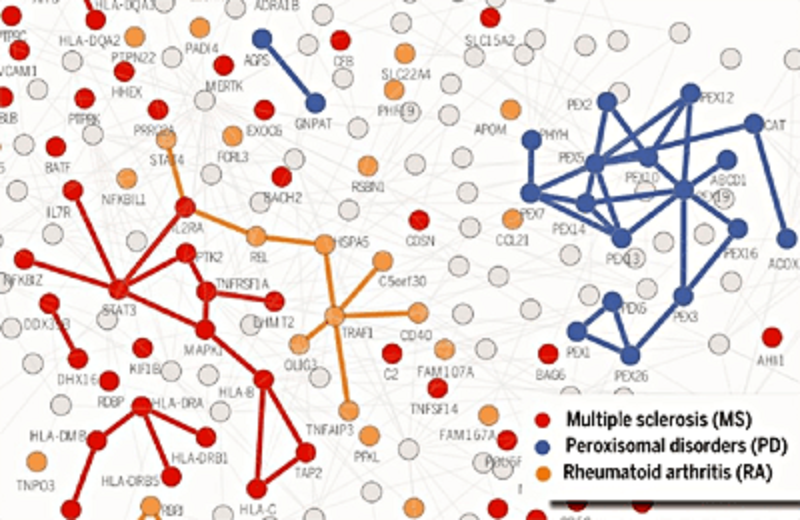
Рисунок 1. Патологические кластеры на карте интерактома. Белки, связанные с патогенезом конкретного заболевания, образуют кластеры: красный — рассеянный склероз, желтый — ревматоидный артрит, синий — пероксисомные болезни. Для заболеваний с перекрывающимися кластерами (рассеянный склероз и ревматоидный артрит) обнаруживаются общие патобиологические механизмы и симптомы.
{3]
Возможно, когда-нибудь мы узнаем о молекулярных взаимодействиях в клетках человека всё. Построив полный интерактом — схему взаимодействия всех молекул (но чаще в поле зрения оказываются белки), мы сможем предсказывать, на что повлияет поломка каждого из белков или генов. На данный момент, по оценкам ученых, нам известно около 20% интерактома человека, и исследован он неравномерно: какие-то его фрагменты известны в бóльших подробностях, чем другие. Можем ли мы уже на этой стадии начать поиск каких-то закономерностей устройства сети молекулярных взаимодействий?
Целая плеяда биологических терминов с суффиксом «-ом» описана в статье «“Омики” — эпоха большой биологии» [1]. Любители порыться в «омиках» совершают научные прорывы, не прикасаясь к реактивам, не вскрывая тел, но... не отходя от компьютера: «Вычислительное будущее биологии» [2]. — Ред.
Известно не так много заболеваний, обусловленных «поломкой» лишь одного вида генов. Чаще всего болезнь вызывается взаимодействием нескольких типов молекул: давно замечено, что мутантные белки, провоцирующие заболевание (например, определенный вид рака), часто взаимодействуют между собой. В таком случае на карте интерактома должен быть различим кластер (модуль) дефектных белков, характерных для каждой болезни (рис. 1). Но можно ли увидеть такие кластеры на неполной карте, на которой, как предполагают ученые, отмечено пока лишь около одной пятой всех связей между белками?
Американские ученые подобрали математические условия, при которых кластеры связанных с болезнью белков были различимы на карте интерактома [3]. Оказывается, при нынешнем качестве карты мы можем увидеть только кластеры, в которых участвует не менее 25 белков (рис. 2). На самом деле, эта ситуация не такая уж редкая: известно несколько сотен заболеваний, связанных с изменениями большого количества белков.
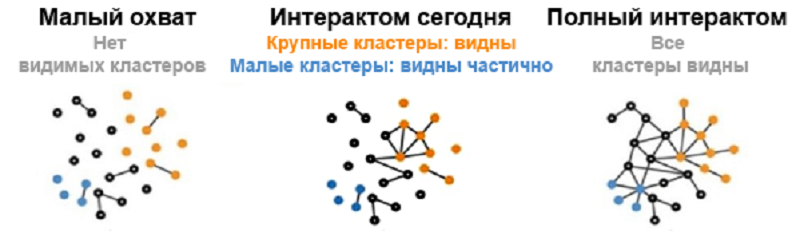
Рисунок 2. Постепенная фрагментация (увеличение разрешения) интерактома. На неполной карте интерактома, доступной сейчас, видны только крупные кластеры — для тех болезней, в патогенезе которых участвует много белков. Со временем, когда карта молекулярных взаимодействий станет более подробной, ученые рассчитывают увидеть на ней гораздо больше связанных кластеров.
{3]
Ученым удалось обнаружить на нынешней карте интерактома кластеры для 226 заболеваний (из 299 отобранных для анализа). При этом некоторые из связанных с болезнью белков всё же оказывались вне кластера: к примеру, с рассеянным склерозом ассоциировано 69 белков, но лишь 11 из них были связаны между собой и образовывали кластер на карте интерактома. Тем не менее связанных белков во всех случаях было больше, чем можно было ожидать при случайном распределении связанных с болезнью белков по карте интерактома. Интересно, что в кластеры объединяются в среднем около 20% связанных с болезнью белков — а именно такая доля всех взаимодействий нам на данный момент известна. Недостающие связи, возможно, будут открыты со временем.
Расположение кластеров на карте интерактома может дать нам новую информацию о связях между заболеваниями. Между кластерами двух болезней можно рассчитать дистанцию, исходя из наименьших расстояний между белками, относящимися к каждой из болезней, а также из расстояний между белками, относящимися к разным болезням. Иногда кластеры перекрываются, если в патогенезе нескольких болезней задействованы одни и те же белки. К примеру, в патогенезе астмы (болезни дыхательных путей) и целиакии (связанном с непереносимостью глютена нарушении всасывания в тонкой кишке) неожиданным образом задействован определенный набор общих белков. Оказалось, что для этих непохожих болезней также характерен общий однонуклеотидный полиморфизм — единичная замена нуклеотида в ДНК [4]. По-видимому, между этими болезнями есть много общего.
Таким образом, расположение патогенных белков на карте интерактома помогает искать связи между теми данными, которые у нас уже есть. Но ученые обнаружили и другие случаи перекрывания кластеров, в которых совпадающих белков не было.
Эти случаи особенно интересны, поскольку у болезней с перекрывающимися кластерами, даже если у них нет общих патогенных белков, все равно обнаруживалось определенное сходство. Например, чем больше перекрывались кластеры на карте интерактома, тем больше одинаковых симптомов обнаруживалось у соответствующих болезней. Кроме того, с возрастанием степени перекрывания кластеров росла и вероятность возникновения этих заболеваний одновременно. Как уже говорилось, у таких сходных по проявлениям болезней могло и не быть общих белков, участвующих в патогенезе, поэтому обнаружить связь между ними просто по спискам задействованных в развитии болезни молекул невозможно.
Одним из неожиданных результатов стало перекрывание кластеров лимфомы и инфаркта миокарда, в патогенезе которых одинаковых молекул замечено не было. Однако, как оказалось, эти состояния достаточно часто встречаются вместе. Кроме того, ранее было показано, что при внутрисосудистой B-крупноклеточной лимфоме опухолевые клетки могут забивать просвет сосудов, в том числе и в сердце, вызывая острую ишемию [5].
Пересечения кластеров для разных болезней на карте интерактома могут показать, что даже между на первый взгляд не связанными болезнями есть что-то общее. Такие связи в перспективе помогут установить механизмы развития менее изученных заболеваний на основе данных о более изученных. Со временем карта интерактома человека будет уточняться, и мы сможем использовать ее для предсказания эффектов тех или иных мутаций и раскрытия новых терапевтических возможностей уже используемых препаратов.
Литература
- «Омики» — эпоха большой биологии;
- Вычислительное будущее биологии;
- Jörg Menche, Amitabh Sharma, Maksim Kitsak, Susan Dina Ghiassian, Marc Vidal, et. al.. (2015). Uncovering disease-disease relationships through the incomplete interactome. Science. 347;
- Karen A Hunt, Alexandra Zhernakova, Graham Turner, Graham A R Heap, Lude Franke, et. al.. (2008). Newly identified genetic risk variants for celiac disease related to the immune response. Nat Genet. 40, 395-402;
- Alexander BAUER, Boris PERRAS, Sven SÜFKE, Hans-Peter HORNY, Burkhard KREFT. (2005). Myocardial infarction as an uncommon clinical manifestation of intravascular large cell lymphoma. Acta Cardiologica. 60, 551-555.






