
Особая диета: молекулярный водород три раза в день, ионы сульфата перед едой
25 января 2021
Особая диета: молекулярный водород три раза в день, ионы сульфата перед едой
- 1059
- 0
- 2
Всё именно так и выглядит под микроскопом! Верьте мне, я эксперт!
рисунок автора статьи
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: На дне водоемов и в их толще, в глубине земли, на скалах, в горячих гейзерах и холодных болотах можно найти удивительных микроорганизмов. Мы не можем рассмотреть их глазом, но поверьте, они там есть. И многие из них сильно отличаются от нас. Если мы едим мясо, овощи, крупы, фрукты, то они едят аммоний, сероводород, сульфит, пирит, молекулярный водород. Если мы дышим кислородом, то некоторые из них могут дышать нитритом и нитратом, сульфатом и даже железом. Кто они? Хемолитотрофные бактерии.
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Вирусы и микроорганизмы» конкурса «Био/Мол/Текст»-2020/2021.

Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.

Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
В глубинах ночных океана,
Куда не дотянемся мы,
Из черного дна неустанно
Крутые восходят дымы.
Среди закипающей черни,
Рождающей множество руд,
Огромные плоские черви
В горячих рассолах живут.
Едят они серу на ужин,
Вкушая от этих щедрот.
Здоровью их даром не нужен
Полезный для нас кислород.
И в час, когда вспыхнет пожаром
Земная недолгая плоть,
И ядерным смертным ударом
Людей покарает Господь,
И солнце погаснет, и реки
Покроются пепельным льдом,
Они лишь освоят навеки
В наследство доставшийся дом.
И ступят на цепкую лапу,
Что станет позднее ногой, —
Начало другого этапа,
И будущей жизни другой.
Александр Городницкий
Без чего невозможно существование жизни? Без воды? Разумеется. Без тепла? Верно. Без кислорода? Частично верно. Без других живых существ? Правильно. Без еды? Абсолютно точно. И именно о таком важном аспекте, как «покушать», мы и узнаем сегодня. Но зайдем с совершенно другой, можно сказать, экзотической стороны.
В повседневной жизни мы наблюдаем типичное явление: живые существа едят друг друга. Травоядное ест растения, хищник ест травоядное, хищника может съесть следующий хищник. Все поглощают органические вещества для получения энергии и строительного материала для своего тела. И все дышат кислородом: человек, хищники, травоядные, насекомые, моллюски, черви, инфузории, коловратки, тихоходки и т.д. Из этой стройной и простой картины уже начинают выбиваться растения: они сами синтезируют себе органические вещества из углекислого газа для строительства тела за счет энергии света (так называемого фотосинтеза [2]); и то хорошо — типично, как все нормальные существа, растения дышат кислородом. А давайте представим, что есть необычные микроорганизмы — бактерии и археи — которые используют для получения энергии соединения азота и серы, железо и, страшно сказать, водород. Причем некоторые из них умудряются «дышать» той же серой или азотом. И при этом они еще и сами себе синтезируют органику. Невероятно, но такие организмы действительно существуют, и называют их хемолитоавтотрофами.
И бактерии, и археи — микроорганизмы, причем прокариоты (то есть лишенные ядра). Однако различия между ними очень существенны, на что впервые указал Карл Вёзе [3], введший в обиход трехдоменную классификацию жизни на Земле [4]. Что интересно, объединение этих форм жизни воедино во времена, практически столь же древние, что и LUCA [5], [6], породило третий домен жизни — эукариот (организмов с клеточным ядром, к которым относятся простейшие, грибы, растения и животные [7]). — Ред.
Типы питания
Сначала, выясним, что скрыто за таким пугающим словом — «хемолитоавтотрофы». Все варианты типов питания всех живых организмов описываются шестью терминами с прибавлением окончания -трофия (от греч. τροφή — «пища»). Они распределены на три категории, которые являются тремя главными аспектами метаболизма:
- Источник энергии:
- Донор электронов (объяснения, что это такое, в следующем параграфе):
- Литотрофы — донор электронов неорганической природы (растения используют воду как донора);
- Органотрофы — донор электронов органической природы (человек);
- Источник углерода:
- Гетеротрофы — источником являются другие органические вещества, которые расщепляются и используются для роста;
- Автотрофы сами создают себе органические вещества из углекислого газа (CO2), формиата (HCOO–), бикарбоната (HCO3−), угарного газа (CO), формальдегида, метанола, метана и веществ с «неорганической» метильной группой.
Используя эту информацию, мы можем сказать, что хемолитоавтотрофы — это организмы, которые используют энергию химических связей и неорганические вещества для получения внутренней (собственной) энергии, которую, в том числе, они расходуют на создание органики из неорганических соединений углерода. Чисто для справки: человек является типичным хемоорганогетеротрофом.
Секреты метаболизма
Для понимания, почему некоторые микроорганизмы могут «есть» серу и «дышать» азотом, необходимо обсудить, как происходит метаболизм на молекулярном, самом изначальном, уровне. Готовьтесь, будет нелегко.
Главная молекула здесь — АТФ, или аденозинтрифосфат [8]. Ради ее получения всё и происходит. Она — батарейка, запасающая энергию, которая потом используется для жизни. «Батарейка-АТФ» производится особым ферментом — АТФ-синтазой, который является по своей сути молекулярным мотором: он, в прямом смысле, крутится за счет прохождения через него протонов (H+) и создает «батарейку». «Так, — думаете вы, — появились протоны, и они каким-то образом проходят через фермент». Их никто не толкает и не переносит — протоны сами стремятся по градиенту концентрации из области, где их много, в область, где их мало. Для разграничения этих областей используется мембрана — это может быть обычная мембрана клетки (если другой нет), периплазматическая мембрана, мембрана митохондрии (как у нас с вами) или мембрана хлоропласта (при фотосинтезе у растений). Но это всё тонкости, главное — есть мембрана , которая разграничивает две области с разной концентрацией протонов. В этой мембране сидит белок-фермент; он открывает канал через себя, и протоны с визгом и хохотом устремляются в область, где их меньше, ведь они любят личное пространство. И эта энергия активного движения протонов обрабатывается и аккумулируется в АТФ.
Пожалуй, это и правда главное: все известные нам формы жизни строятся на наличии мембраны, непроницаемой для воды и растворимых веществ из-за своего липидного состава: «Липидный фундамент жизни» [9]. — Ред.
Остался вопрос: а как так получилось, что концентрации протонов по обе стороны мембраны разные? И вот для этого нам необходимы источник энергии и донор электронов. Из названия «донор электронов» понятно, что он дает нам электрон, движение которого и обеспечивает разницу концентраций. Только вот электроны ленивы и куда-либо двигать со своих насиженных мест просто так не будут. Им нужен «пинок», которым выступает источник энергии; электрон, которому «придали ускорение», начинает двигаться, но не просто свободно лететь, а передаваться, как горячая картошка, по цепочке веществ (в основном белков). Это приводит к перебросу протона из одной области в другую через мембрану, а так как протоны не появляются из воздуха и не исчезают неожиданно, то на одной стороне их становится больше, а на другой меньше — разница концентраций обеспечена, можно делать «батарейку-АТФ»!
Но «активный» электрон остался в цепи, и с ним надо что-то делать, иначе он может выйти из-под контроля и начать барагозить в клетке (например, производить активные формы кислорода [10], что способно привести к разрушению белков и других молекул). Один вариант — передать этот электрон на специальные вещества (например, НАДН и НАДФН), которые используют его в метаболических путях как для получения энергии, так и, например, при создании углеводов из неорганического углерода в растениях (фотосинтез). Второй путь — сбросить его на молекулу, называемую акцептором электронов, которая «успокоит» электрон. Проще всего привести пример: у человека это кислород. Да, можно сказать, что то, чем мы дышим, является некой сточной канавой для «использованных» электронов. И кислород в этом плане самый лучший! Теперь мы понимаем, как можно «дышать» соединениями азота или серы: на них сбрасываются электроны после использования. У бактерий множество разнообразных акцепторов электронов, не только неорганических. А есть даже уникальные случаи, когда микроорганизм сам себе производит акцептор электронов, а не берет из среды — например, некоторые метаногенные археи из отдела Euryarchaeota.
Для наглядного примера используем электрон-транспортную цепь митохондрии (она работает в человеке) (рис. 1). Оранжевым показан путь электрона; конкретно в митохондрии он приходит из цикла Кребса, но изначально его отдает донор электронов.
Чуть больше всяких интересностей и подробностей про митохондрии и метаболизм в клетках человека можно прочитать в спецпроекте «Биомолекулы» «Биоэнергетика».
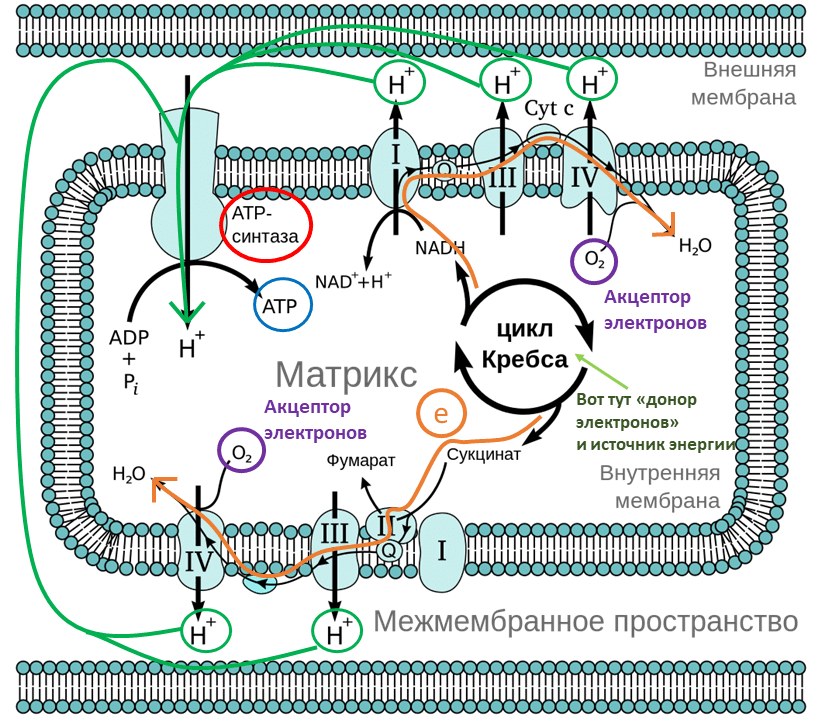
Рисунок 1. Митохондриальная электрон-транспортная цепь. ATP = АТФ.
Вот теперь мы рассмотрели необходимую информацию для понимания, как хемолитоавтотрофы могут жить, расти и размножаться. Хочу уточнить, что это описание энергетического метаболизма клетки очень упрощено и утрировано с использованием, возможно, не совсем корректных сравнений. Но для нашей текущей задачи этого достаточно. Собираем всё вместе (идем по картинке!): донор электронов дает электрон (или электроны), который «заряжается» источником энергии; электрон бежит по цепи и дает энергию клетке, а после сливается на акцептора электронов.
Поедающие азот
Основная еда — аммиак (NH3) или нитрит (NO2−). Стоит сказать, что подобное встречается только у бактерий, и их называют нитрифицирующими. В зависимости от того, чем они выбрали питаться (аммиаком или нитритом), их делят на нитрозобактерий (класс Betaproteobacteria) и нитробактерий (род Nitrobacter, род Nitrococcus, род Nitrospina) соответственно. Дышат они кислородом.
Нитрозобактерии «перерабатывают» аммиак в нитрит и выбрасывают его в окружающую среду. Нитробактерии подбирают за нитрозобактериями то, что они не доели, «перерабатывают» это в нитрат (NO3−) и также выбрасывают как отход метаболизма. По этой причине две группы этих бактерий часто образуют сообщества, где азот проходит следующий путь:
NH3 → NO2− → NO3−
И если нитробактерии нуждаются в соседстве с нитрозобактериями, то последние могут жить отдельно, так как аммиак поступает из множества источников (рис. 2). Неравноценные отношения, не так ли? Жить они могут как в воде, так и в почве, был бы источник энергии.
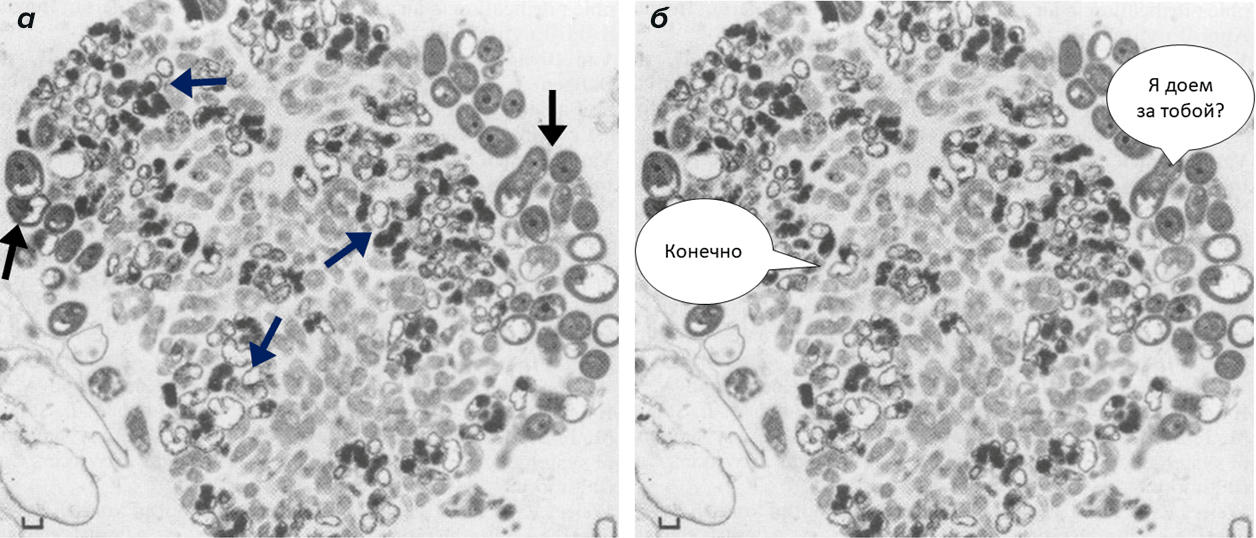
Рисунок 2. Поедающие азот. а — Смешанная культура Nitrosospira штамм AHB1 (нитрозобактерия) и Nitrobacter штамм NHB1 (нитробактерия). Черные стрелки — нитробактерии, синие стрелки — нитрозобактерии. Просвечивающая электронная микроскопия. б — То, как я вижу эту микрофотографию.
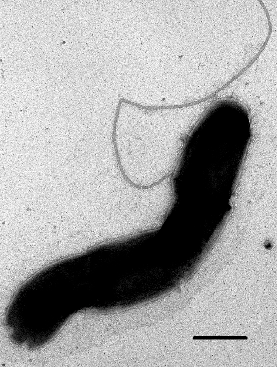
Рисунок 3. Клетка Nitrospira inopinata со жгутиком. Просвечивающая электронная микроскопия, масштабная линейка 0,2 мкм. На вид обычная, а такая уникальная.
После открытия нитрифицирующих ассоциаций бактерий ученые задумались: а есть ли такой уникальный микроорганизм, который бы осуществлял полный цикл от аммиака до нитрата в одно лицо? И, в конце концов, его нашли. Обнаружили его в воде из нефтяной скважины на глубине 1000 м и назвали Nitrospira inopinata (рис. 3) [11]. Такую полную нитрификацию назвали комамоксом.
Не то чтобы и давно (первые сообщения появились в 1995 году) открыли питание аммиаком без использования кислорода. Подобный процесс назвали аннамоксом [12]. Чем дышат такие микроорганизмы? Нитритом. Да, одни его едят, другие им дышат — нормальное явление у бактерий. Отходами жизнедеятельности у них является чистый азот (N2). Еще один интересный факт: промежуточный продукт метаболизма — гидразин (H2N—NH2), применяемый как ракетное топливо, — токсичен, поэтому накапливается в отдельной органелле — анаммоксосоме — и там же перерабатывается (рис 4). Это как если бы у человека в процессе метаболизма накапливался метанол в отдельном органе в больших количествах и потом перерабатывался в воду и углекислый газ. Эти бактерии вообще странные (даже по меркам описанных в этой статье примеров): и состав белков в клетке странный, и липиды в мембране странные. У них даже есть очень чувствительный «орган», который «вынюхивает» аммоний в среде [12]. Но аннамокс-бактерии живут со всем этим спокойно. Все они принадлежат отделу Planctomycetes, например, род Brocadia и род Kuenenia.
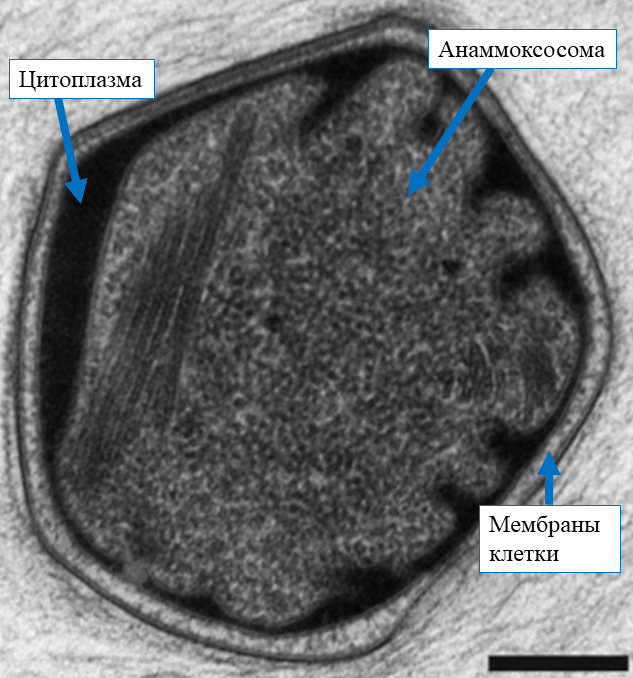
Рисунок 4. Некоторые подробности строения клетки аннамокс-бактерии. Масштабная линейка 0,2 мкм.
Нитрифицирующие, комамокс- и аннамокс-бактерии — обязательные участники глобального круговорота азота (рис. 5) [13]. Поступающий в почву аммоний от азотфиксаторов и редуцентов они переводят в нитрат, необходимый для растений, или молекулярный азот, возвращающийся в атмосферу.
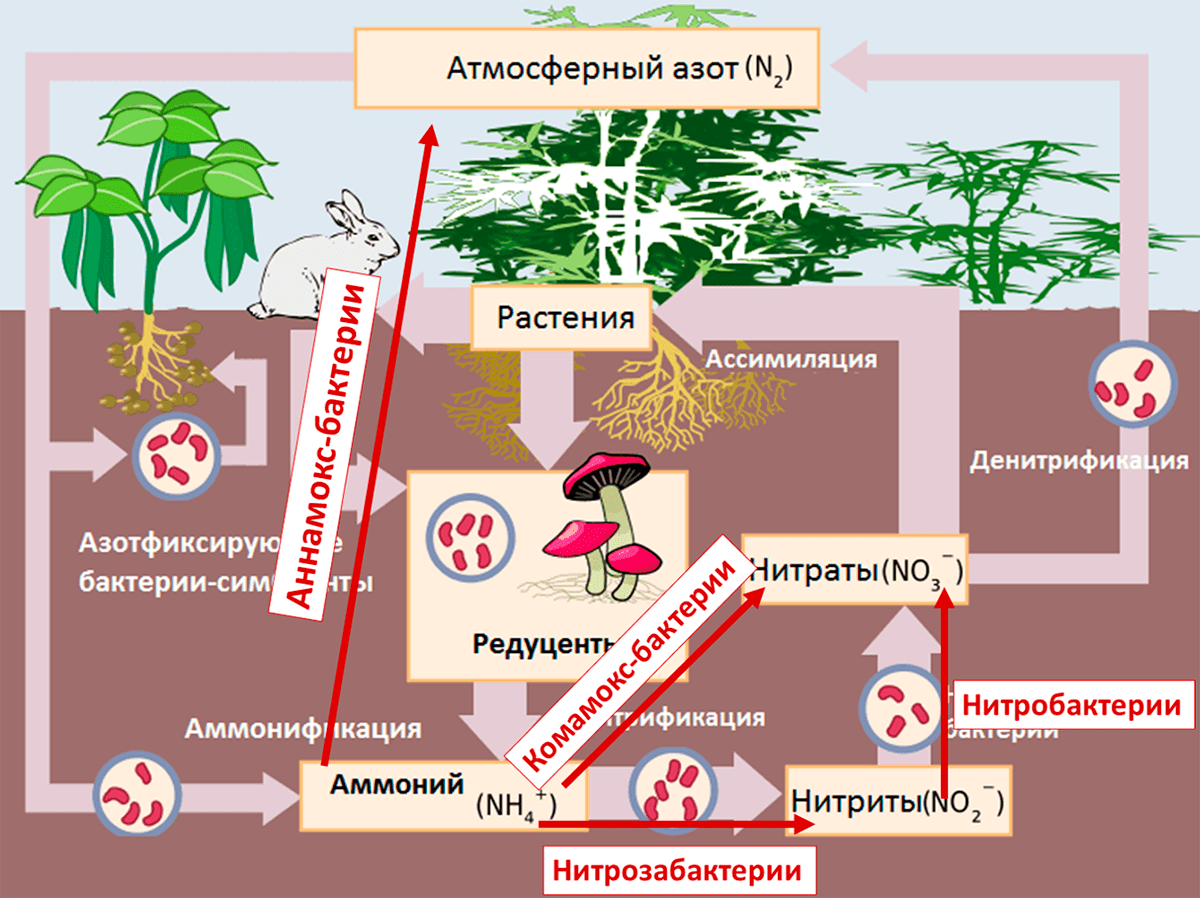
Рисунок 5. Схема цикла азота
[13], рисунок с изменениями
Поедающие серу
Здесь основным источником энергии выступают элементная сера (S0) и так называемые восстановленные неорганические соединения серы. Это такие вещества как политионаты (SO3—(S)n—SO3), сульфид (S2−, в том числе сероводород H2S), сульфит (SO32−) и тиосульфат ([S—SO3]2−). Такое обилие субстратов (а это еще и не совсем полный список) подразумевает разнообразные метаболические пути, но конечным продуктом всегда остается серная кислота или, что примерно то же самое, ион сульфата (H2SO4/SO42−).
Всех серных бактерий очень условно и с оговорками можно разделить на две группы: бесцветные серные бактерии и тионовые бактерии. Бесцветные делают запасы элементной серы в виде серных глобул (а то вдруг голод), которая образуется после использования сероводорода как источника энергии (рис. 6 и рис. 7). Впоследствии они могут подъедать ее с образованием сульфита. А тионовые сразу извлекают максимум из еды, что они смогли найти, осуществляя полный цикл с выделением серной кислоты.
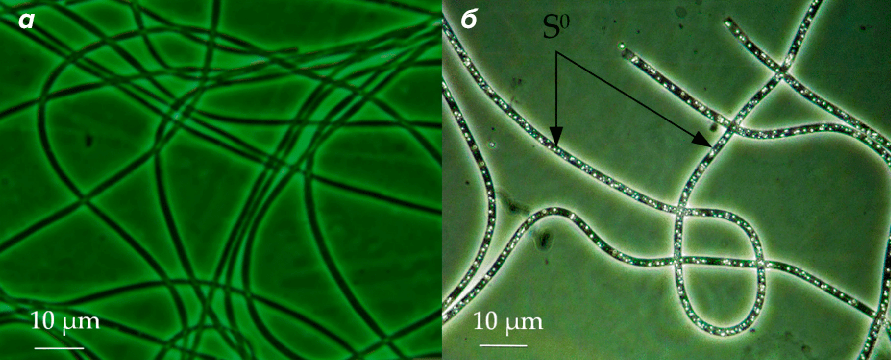
Рисунок 6. Поедающие серу. Трихомы штаммов Beggiatoa leptomitoformis D-401 (а) и D-402 (б) (бесцветная серная бактерия). Фазовый контраст. Стрелочки указывают на серные глобулы. Именно на бактериях рода Beggiatoa С.Н. Виноградский открыл явление литотрофии.

Рисунок 7. Мат белых трихомных серных бактерий между корнями мангрового дерева на глубине примерно 1 м — необычное можно встретить намного ближе, чем вы думаете. Красной стрелкой указан мат.
В основном для дыхания эти бактерии используют кислород, но есть исключения. Некоторые представители родов Thioploca (рис. 8) и Thiomargarita имеют вакуоль, где запасают нитрат. Этот нитрат может быть заменой кислороду, когда последнего не оказывается в среде, — нитратное дыхание! Есть специфические ситуации, когда используется ион трехвалентного железа, но об этом далее.

Рисунок 8. Жизнь серных бактерий.< а — Бактерии р. Thioploca не живут поодиночке: множество трихомов выходят из общего чехла (более темный). б — Водная колония бактерий р. Thioploca, одна нить — один чехол. в — Колония серных бактерий различных родов в подводной пещере Grotta sulfurea, Италия. Нити очень нежные и ломаются от малейших колебаний воды.
Commuting to Work, [22] и Wikimedia
Одним из промежуточных продуктов подобных метаболических путей является сульфит (SO32−). Он токсичен и имеет антимикробные свойства, но некоторые серные бактерии используют его как единственный источник энергии — настоящие экстремалы среди бактерий (рис. 9). Понятное дело, его нужно убрать из клетки, преобразовав в сульфат. Можно просто использовать кислород для этого, но тогда мы не получим энергию и электроны, а можно делать это с помощью ферментов. И вот в одном из вариантов с ферментами одним из возможных акцепторов электронов служит Fe3+ — железное дыхание (рис. 10).

Рисунок 9. Серные бактерии действительно могут выбирать экстремальные местообитания. Например — Канареечный родник (Canary Spring) в Йеллоустонском национальном парке. Температура воды там «всего лишь» 80 °C — это вполне приемлемо для развития оранжевых колоний серных бактерий.

Рисунок 10. Примеры уравнений ассимиляции соединений серы
Помимо вышеназванных соединений серы, некоторые представители серных бактерий могут использовать для питания сульфидные минералы: пирит (FeS2), сфалерит (ZnS), галенит (PbS), халькопирит (CuFeS2) и другие. Подробно описывать усвоение этих минералов незачем, важно, что при этом отделяется катион металла. Это привело к созданию бактериального выщелачивания — процесса получения из бедных руд и заброшенных выработок меди, железа, свинца, цинка и других металлов (рис. 14). Это достаточно дешевый, экологичный и быстрый способ, так как в некоторых случаях достаточно полить гору отработанной руды водой и добавить бактерий, подождать, снова полить, собрать «металлическую» воду и, наконец, выделить из нее необходимые ценные ископаемые (любым понравившимся способом) — вуаля, вы прекрасны!
Обитают серные бактерии там, где есть постоянный приток соединений серы, особенно сероводорода, и кислорода. Это могут быть донные отложения: снизу в результате процессов разложения поступает сероводород, сверху потоками воды приносит кислород; зоны морского вулканизма, гидротермальные источники («черные курильщики») (рис. 11). В гидротермальных источниках они занимают место, где не очень жарко, есть приток кислорода и соединений серы. При этом вместе с ними там развивается обилие жизни в виде беспозвоночных, рыб и других бактерий. В черных курильщиках также был обнаружен уникальный симбиоз: серная бактерия Candidatus «Endoriftia persephone» живет внутри червей из класса Vestimentifera (рис. 11). У червей нет рта и ануса, а пищеварительная система сильно редуцирована, вместо этого у червя есть орган «трофосома», который набит серными бактериями. Фактически, червь питается за счет того, что нашли бактерии, а бактерии получают более-менее комфортную и безопасную нишу для жизни.

Рисунок 11. «Черные курильщики» — глубоководные гидротермальные источники. Из них извергается высокоминерализованная горячая (до 400 °C) вода под давлением в сотни атмосфер. Здесь жизнь существует только за счет хемолитоавтотрофных бактерий: не было бы их, не было бы такого уникального сообщества.
Возможность питания серой распространена по многим отделам и практикуется очень разными и далекими в плане родства бактериями. Судя по всему, это очень древний биохимический процесс, который мог быть унаследован от общего предка.
Поедающие железо
Процесс питания железом имеет намного больше проблем, чем все ранее описанное. Во-первых, железо «низкокалорийное», поэтому в основном выступает в роли «дополнительного питания». Часто в метаболизме соседствует с питанием серой, причем серная хемолитотрофия является основной. Есть представители классов Betaproteobacteria и Gammaproteobacteria, которые используют исключительно соединения Fe2+ (двухвалентное железо) как источник энергии. Но для этого они должны жить в среде с высокой концентрацией пищи и постоянно перерабатывать ее для получения энергии, достаточной для роста и размножения. Их колонии имеют охристый цвет за счет накопления оксидов и гидроксидов трехвалентного железа (Fe3+) (рис. 12).

Рисунок 12. Это не последствия экологической катастрофы, это бурное развитие железных бактерий. На первой фотографии — ручей Гессенбах, Германия (Maria Fabisch, 2009); на второй — отложения трехвалентного железа на почве вокруг ручья (Felix Beulig, 2011).
Во-вторых, возникает проблема с добычей субстрата. Железо имеет валентности 2+ и 3+. Fe2+ растворимо в воде, и его легко использовать, но также легко оно окисляется кислородом воздуха и выпадает в нерастворимый осадок Fe3+. Его, понятно, не получится использовать в пищу. У бактерий есть два пути: либо жить, где Fe2+ много, а кислорода мало (тогда точно удастся отхватить свой кусочек) (рис. 12), либо жить в кислых местообитаниях, где не так активно идет образование осадка. Поэтому такой классический представитель железных хемолитотрофов как Acidithiobacillus ferrooxidans (рис. 13) живет в кислых водах (pH 4–5). Идеальные условия образуются для него в затопленных отработанных шахтах или кислых водоемах, где в результате действия подобных бактерий вода приобретает рыжий или охристый цвет (рис. 14).

Рисунок 13. Acidithiobacillus ferrooxidan; сканирующая электронная микроскопия

Рисунок 14. «Кислотные» шахты. а — Заброшенная железорудная шахта, участок, затопленный грунтовыми водами. Рыжий цвет воды указывает на высокую вероятность проживания там железных бактерий. б–г — Затопленный Дегтярский рудник, кислые воды. Тут тоже вполне комфортно для проживания железных бактерий; приятный бонус — человек редко тревожит, так как из-за высокой кислотности вода разъедает обувь и одежду.
У железных бактерий дыхание может быть кислородным, тогда все достаточно типично:
4Fe2+ + O2 + 4H+ → 4Fe3+ + 2H2O
Наряду с этим есть бескислородные железные бактерии. И если в современности «железное питание» имеет малый вес, то в далеком еще бескислородным прошлом Земли использование железа без участия кислорода (откуда ему было тогда взяться?) имело намного большее значение. Акцептором электронов в этой реакции является нитрат, который преобразуется в молекулярный азот (N2):
10FeCO3 + 2NO3− + 24H2O → 10Fe(OH)3 + N2 + 10HCO3− + 8H+
Железные бактерии питаются разными соединениями железа, не только водорастворимыми, но и железными минералами, в частности, уже упомянутым пиритом FeS2, причем некоторые могут использовать в этом соединении и серу, и железо. Эта способность наряду с возможностью жить в кислых водах идеально подходит для бактериального выщелачивания металлов. Бактерии переводят нерастворимые сульфиды в растворимые сульфаты, позволяя добывать цинк, медь, ванадий, уран и т.д. (рис. 15).
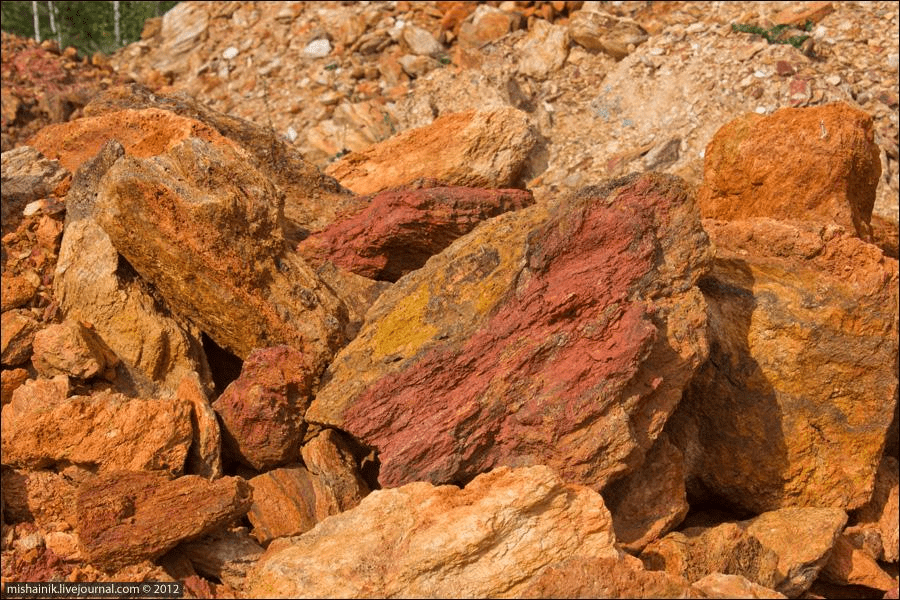
Рисунок 15. Медьсодержащая порода на отвалах Дегтярского рудника. Ценные ископаемые просто лежат никому не нужные. А с помощью бактериального выщелачивания из этой породы вполне возможно добыть медь.
Поедающие водород
Пора переходить к последнему в этой статье и, по моему мнению, одному из самых интересных типов питания. Водородная хемолитотрофия является самой распространенной среди бактерий. Как и железо, водород редко является единственным источником энергии — скорее, одним из возможных вариантов питания, и то дополнительных. Хотя у таких бактерий, как Aquifex pyrophilus (рис. 16), Hydrogenobacter thermophilus и Calderobacterium hydrogenophilum он если не единственный, то главный.
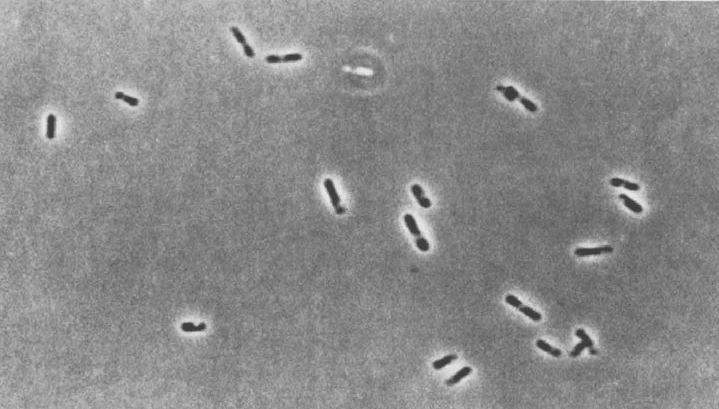
Рисунок 16. Клетки Aquifex pyrophilus ; фазовый контраст
Классические представители водородных бактерий — отдел Aquificae. В эволюционном плане этот отдел один из самых древних, и метаболизм с использованием водорода как субстрата — также достаточно старый способ. И если в эволюции появляется что-то хорошее (а молекулярный водород достаточно распространенный субстрат, хотя и концентрация его в отдельных точках мала), то это подхватывается, поэтому водородных микроорганизмов можно найти в отделах Proteobacteria, Firmicutes и среди архей.
Акцептором электронов может быть как кислород, что дает нам «классический вариант», так и, например, сульфат. Что мне показалось интересным в свое время: классический вариант является экологически чистым, так как для него берут распространенные на планете материалы — кислород и водород, — а в результате получается вода. Идеальное безотходное производство! :-)
H2 + 1/2O2 → H2O
4H2 + SO42− → 4H2O + S2−
Водородные бактерии и археи стоят в самом начале цепей питания в экстремальных нишах с повышенной геохимической активностью (наземных и водных): среди них есть те, кто может выдерживать высокую температуру (70 °C и выше, максимум 95 °C) (рис. 17), изменение pH и токсичные неорганические вещества. Играют большую роль в разрушении органики без участия кислорода. Входят в сообщества с другими бактериями и различные симбиозы.

Рисунок 17. Водородных бактерий можно найти, например, в геотермальных источниках Камчатки. а — Долина гейзеров. б — Кальдера вулкана Узон.
На самом деле есть микроорганизмы, выделяющие чистый водород, а не поглощающие его. Выделяется он как побочный продукт очень важной для биосферы реакции — азотфиксации (рис. 5). Благодаря ей, цианобактерии и клубеньковые бактерии возвращают атмосферный азот обратно в круговорот, делая его доступным для растений и рядом живущих организмов. Как можно заметить — ничто в природе не бесполезно, даже побочные продукты. Для человечества выделяющие водород бактерии также могут принести пользу: молекулярный водород — это экологически чистое топливо в практически неограниченных количествах [14]. Проблема только в разработки технологий его получения и использования.
Значение для планеты
Вы могли заметить, что я ничего не сказала про автотрофию этих бактерий. В этой статье я не ставила задачу подробное описание различных циклов ассимиляции неорганического углерода, а простое перечисление названий циклов не скажет ничего. Я обсуждала хемолитоавтотрофных бактерий (а практически все приведенные в этой статье бактерии — хемолитоавтотрофы) с той точки зрения, что конкретно они являются первым (а значит одним из главных) звеном в пищевых цепочках своих местообитаний. В места их жизни может не проникать свет, либо условия очень экстремальные для развития растений или других фотосинтетиков — высокая температура, очень кислый или очень щелочной водоем, высокая концентрация сероводорода, сульфита, токсичных металлов и т.д.
Именно они производят органику в этих нишах из неорганического углерода, которую используют другие существа: бактерии, микроорганизмы, беспозвоночные и позвоночные животные, и так может дойти даже до человека (хотя и не во всех случаях). Подобные сообщества могут называть «второй» или «третьей» биосферой, противопоставляя «первой» биосфере с растениями-создателями органики. Уже упомянутые «черные курильщики» могут быть примером: за счет наличия хемолитоавтотрофов там развивается бурная жизнь с беспозвоночными животными и рыбами, хоть и разнообразие там меньше по сравнению с менее экстремальными нишами.
Земле около 4,5 млрд лет, а первая жизнь, по разным подсчетам, появилась около 4,1–3,7 млрд лет назад. Существовало две гипотезы, что было первичным: элементарный метаболизм [15] или «мир РНК» [16] (я склоняюсь ко второй). В то время планета была не самым райским местом для жизни: постоянные извержения, везде кислоты, токсические вещества, дым, высокая температура, грозовые бури и т.д. Цианобактерии появились только 2,5 млрд лет назад, а значит, даже кислорода в нормальной концентрации не было! Поэтому, скорее всего, подобные хемолитоавтотрофные сообщества были основой жизни в детстве нашей планеты, около 3–3,2 млрд лет назад. И они сохранились до нашего времени, мы можем посмотреть на них, изучить их. Они могут остаться на Земле и после исчезновения растений или многоклеточных животных, так как «вторая» и «третья» биосферы практически независимы от «первой». Можно, с некой долей пафоса, сказать: они пришли первыми и уйдут последними.
Такие бактерии участвуют в больших биогеохимических циклах азота, серы, железа, углерода, фосфора и т.д. Они связаны с азотфиксацией, переводом нерастворимых веществ в растворимые (доступные), возвращением элементов из глубин Земли (некоторая часть веществ уходит из круговорота и надолго запасается в толще — например, нефть, залежи железной руды, сероводорода). Причем хемолитотрофы — необходимый участник, без которого многие циклы просто остановились бы.
Человечество тоже научилось использовать их уникальность. Ранее уже упоминалось бактериальное выщелачивание металлов, которое позволяет по максимуму выработать породу. Рассуждают об использовании хемолитотрофов для добычи полезных ископаемых на других планетах. Некоторые из них используются в промышленности для производства лекарств и иных вещей.

Рисунок 18. Дай хоть небольшое послабление, и жизнь тут же расплодится. На фотографии знаменитое озеро Утренней Славы (Morning Glory Pool) в Йеллоустонском национальном парке, и его изменение с течением времени. До активного туризма озеро самоочищалось и поддерживало слишком высокую температуру для роста бактерий. Но многочисленные посетители стали кидать туда монетки на удачу, чем забили желоб настолько, что самоочищение стало невозможным. Температура упала до 70 °C, и начался бурный рост микроорганизмов (цветная каемка).
Заключение
В этой статье при рассказе о бактериях специально упущены некоторые подробности и мелкие детали, а описание процессов порой не совсем корректно упрощено для лучшего восприятия информации. Я прошу прощения за это, особенно у разбирающихся людей, кто будет читать эту статью. Все приведенные варианты метаболизма здесь и примеры микроорганизмов — лишь малая доля разнообразия бактерий и архей, поэтому моей главной целью скорее было заинтересовать тебя, читатель, и рассказать что-то новое о многообразии жизни на Земле, чем написать подробную лекцию. Я надеюсь, у меня это получилось. В основном, я базировалась на учебнике А.В. Пиневича «Микробиология. Биология прокариот» [1], и, если у вас появилось желание немного углубиться в тему, я вам его советую.
Литература
- Пиневич А.В. Микробиология. Биология прокариотов: учебник (т. 2). СПб.: Изд-во С.-Петерб. ун-та, 2007. — 331 с.;
- Фотосинтез в образах;
- Карл Вёзе (1928–2012);
- Эволюция между молотом и наковальней, или Как микробиология спасла эволюцию от поглощения молекулярной биологией;
- В диких условиях: как жил последний всеобщий предок LUCA;
- От Бульона до Эукариот. Первый организм и наш древнейший предок;
- Опасные связи. Новый взгляд на происхождение эукариотических химер, подмявших под себя весь мир;
- Вторая жизнь АТФ: от главной батарейки до нейромедиатора;
- Липидный фундамент жизни;
- Активный кислород: друг или враг, или О пользе и вреде антиоксидантов;
- Maartje A. H. J. van Kessel, Daan R. Speth, Mads Albertsen, Per H. Nielsen, Huub J. M. Op den Camp, et. al.. (2015). Complete nitrification by a single microorganism. Nature. 528, 555-559;
- Аммонийный датчик анаммокс-бактерии;
- Одиссея азота;
- Бактерии для водородной энергетики;
- К вопросу о происхождении жизни;
- РНК: начало (мир РНК);
- W. De Boer, P. J. A. Klein Gunnewiek, M. Veenhuis, E. Bock, H. J. Laanbroek. (1991). Nitrification at Low pH by Aggregated Chemolithotrophic Bacteria. Applied and Environmental Microbiology. 57, 3600-3604;
- Holger Daims, Elena V. Lebedeva, Petra Pjevac, Ping Han, Craig Herbold, et. al.. (2015). Complete nitrification by Nitrospira bacteria. Nature. 528, 504-509;
- J. Gijs Kuenen. (2020). Anammox and beyond. Environ Microbiol. 22, 525-536;
- Tatyana S. Rudenko, Sergey V. Tarlachkov, Nikolay D. Shatskiy, Margarita Yu. Grabovich. (2020). Comparative Genomics of Beggiatoa leptomitoformis Strains D-401 and D-402T with Contrasting Physiology But Extremely High Level of Genomic Identity. Microorganisms. 8, 928;
- PY Pascal, S Dubois, HTS Boschker, O Gros. (2014). Trophic role of large benthic sulfur bacteria in mangrove sediment. Mar. Ecol. Prog. Ser.. 516, 127-138;
- M Huettel, S Forster, S Kloser, H Fossing. (1996). Vertical Migration in the Sediment-Dwelling Sulfur Bacteria Thioploca spp. in Overcoming Diffusion Limitations.. Applied and environmental microbiology. 62, 1863-1872;
- Yu Zhang, Shuang Zhang, Dan Zhao, Yongqing Ni, Weidong Wang, Lei Yan. (2019). Complete Genome Sequence of Acidithiobacillus ferrooxidans YNTRS-40, a Strain of the Ferrous Iron- and Sulfur-Oxidizing Acidophile. Microorganisms. 8, 2;
- Robert Huber, Thomas Wilharm, Dagmar Huber, Antonio Trincone, Siegfried Burggraf, et. al.. (1992). Aquifex pyrophilus gen. nov. sp. nov., Represents a Novel Group of Marine Hyperthermophilic Hydrogen-Oxidizing Bacteria. Systematic and Applied Microbiology. 15, 340-351.








