Обоняние: от носа к мозгу, спотыкаясь и падая
05 февраля 2021
Обоняние: от носа к мозгу, спотыкаясь и падая
- 17651
- 0
- 10
Карикатурно представленные обонятельные нейроны заблудились в лабиринте ароматов. На карту нанесены маршруты из запахов, которые используют в одном из стандартных тестов, проверяющих обоняние: испытуемого просят назвать, на что похожи предъявляемые запахи [1].
Рисунок в полном размере.
иллюстрация Глеба Русина
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Как вы думаете, от какого из чувств люди скорее готовы отказаться? Увы, чаще всего говорят: «обоняние». Но это непопулярное чувство намного важнее и загадочнее, чем мы считаем. И в то же время оно очень уязвимо: все мы ждем, что можно будет перестать волноваться о внезапной потере обоняния. Что же таинственного прячут молекулярные и клеточные механизмы обоняния? И почему именно его теряют полностью или частично? Об этом и многих других неожиданных поворотах исследований обоняния читайте в статье.
Конкурс «Био/Мол/Текст»-2020/2021
 Эта работа заняла второе место в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2020/2021.
Эта работа заняла второе место в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2020/2021.

Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.

Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
В мае 2019 года из университета Канберры, опасаясь возможной утечки газа, эвакуируют полтысячи человек; в июле 2019 года самолёт, направлявшийся из Филадельфии в Лондон, совершает экстренную посадку в Бостоне; в июне 2020 года шесть сотрудников почтового отделения отправлены в больницу, — десятки похожих историй появляются в прессе с завидной регулярностью. Что же их объединяет? Провокатор этих происшествий — запахи и наша способность их воспринимать. Мы, как читатели, сочтём эти ситуации курьёзом. Но пострадавшие от отправленного кем-то дуриана или невыносимого запаха в салоне вряд ли захотят повторять такой опыт. Но не стоит завидовать тем, кто, находясь в месте непосредственных событий, остаётся только зрителем, не понимая, в чем причина для паники. За это право приходится дорого платить — обоняние довольно легко потерять, а вот вернуть иногда невозможно.
«Добро пожаловать в мир без вкуса и запаха», — лирично сообщают знакомые в соцсетях. Наверное, самый выделяющийся симптом этой пандемии. Мы стали внимательнее к аромату утреннего кофе и небеспричинно начинаем беспокоиться, если все блюда обеда будут одинаково никакими по вкусу. Потеря обоняния, известная как аносмия, привлекла в 2020 году беспрецедентное научное и общественное внимание (рис. 1).
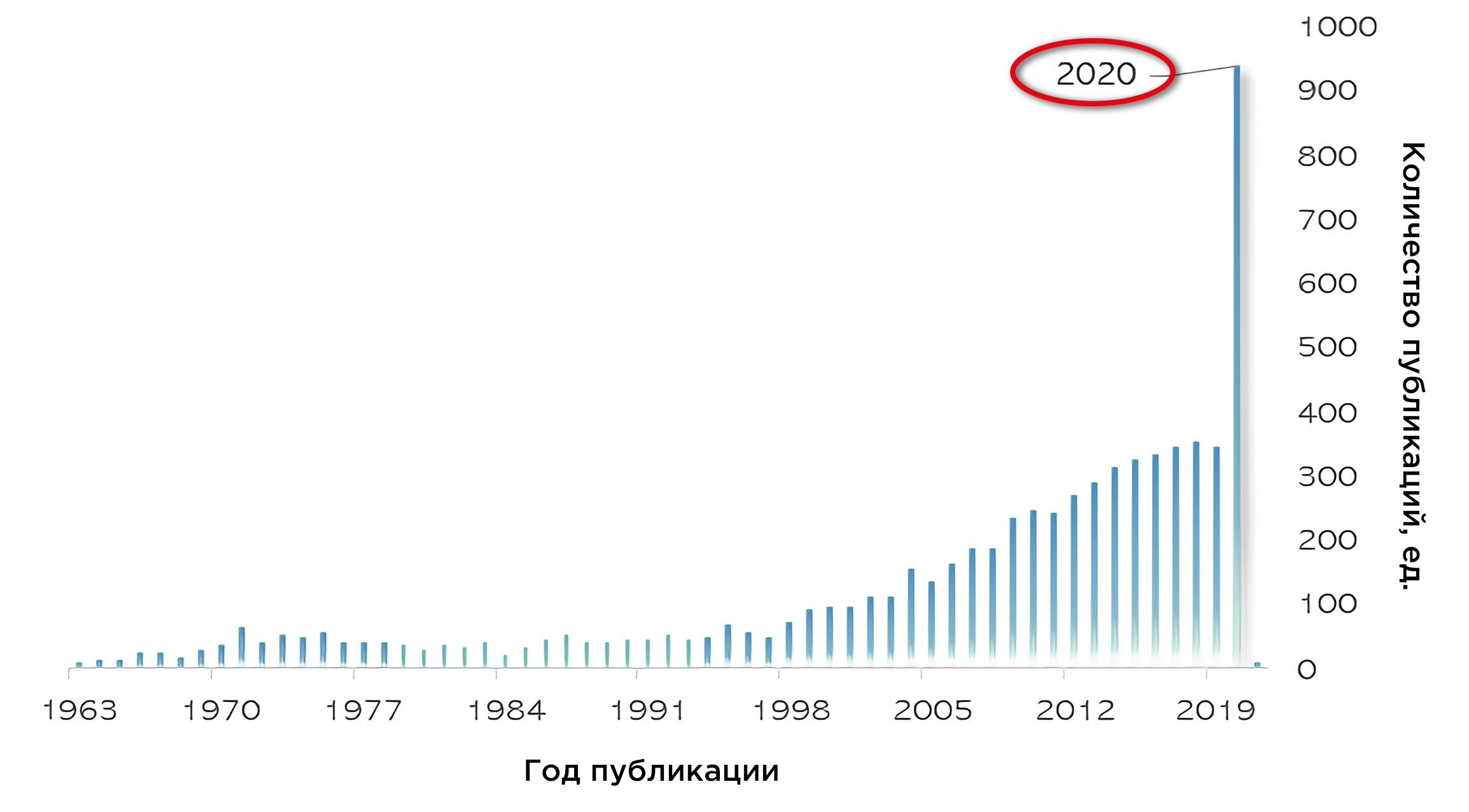
Рисунок 1. Количество публикаций в PubMed по запросу «аносмия». (По данным на 10 декабря 2020 года).
Устранять последствия пандемии мы будем долго, но среди безрадостных цифр найдутся и положительные влияния на здоровье людей — помимо привычки регулярно мыть руки. Например, аносмия и гипосмия (снижение обоняния) — больше не малоизвестные термины. И есть надежда, что исследования последнего года откроют дорогу к созданию новых методов терапии. Знаем об обонянии мы теперь точно немного больше.
По разным докоронавирусным данным эта патология затрагивает от 5% до 20% процентов людей. Предпосылки аносмии разнообразны — это респираторные инфекции, травмы головы, токсические действия лекарств, аллергии и многое другое. В самых крайних случаях — например, при недоразвитии обонятельных долей мозга или генетических дефектах — люди так и узнают мир: практически без вкуса и запаха. Болезнь Паркинсона, Альцгеймера, рассеянный склероз — только некоторые заболевания масштаба эпидемий, о наступлении которых за много лет может сообщить потеря или резкое снижение обоняния [2]. Диагноз «идиопатическая аносмия» получит около четверти людей, так и не узнав, почему они лишились нюха. «Обонятельные» чрезвычайные ситуации тоже бывают — истории шеф-поваров, оставшихся после аварий без работы, можно легко найти в интернете.
Будь то результат пренебрежения или других заблуждений, но обоняние, тип хеморецепции, — самое древнее и самое неразгаданное чувство. На школьных медосмотрах не проверяют наш нюх, в кино пока не пришли ароматы, а говорить о запахах нам часто становится неловко. Как следствие, и в нарушениях мы пока не разбираемся до конца. В феврале благотворительные и научные организации отмечают День осведомлённости об аносмии. Они справедливо считают, что нарушения обонятельной системы заслуживают более серьезного внимания. Как же возникает аносмия? На этот вопрос мы и попытаемся ответить.
Обозначим маршрут
Чтобы понять природу нарушений, мы проследим, как формируется обонятельное измерение. А точнее, обозначим клеточные и молекулярные основы превращения одоранта в нервный сигнал. Для знакомства с обонятельным анализатором (в терминах И.П. Павлова) разберём его на три части (рис 2). Обонятельные нейроны в составе эпителия (это продолжение мозга у нас в носу) улавливают молекулы одорантов (летучих веществ) и отвечают на них сигналом — потенциалом действия. Сигнал уходит по аксонам в обонятельную луковицу, где они переключаются на митральные или пучковые клетки в гломерулах. А дальше по проводам обонятельного тракта информация о запахах отправляется в центральную часть мозга — пириформную кору, миндалину, обонятельный бугорок, энторинальную кору. Уже оттуда сигналы расходятся дальше — в гипоталамус, таламус, гиппокамп, орбитофронтальную кору и др.
Основное внимание мы сосредоточим на периферии анализатора — обонятельных нейронах. По этой причине, к сожалению, за пределами рассказа останутся объяснения многих таинственных аспектов: расшифровка, узнавание и классификация запахов, их связь с эмоциями и воспоминаниями, физиология (например, как похудеть, если отказаться от запахов). Однако попутно представится возможность узнать о некоторых интригующих секретах обоняния, многообещающих клинических испытаниях, Нобелевских лауреатах и новой нейромедиаторной системе, ещё не успевшей попасть во многие учебники.
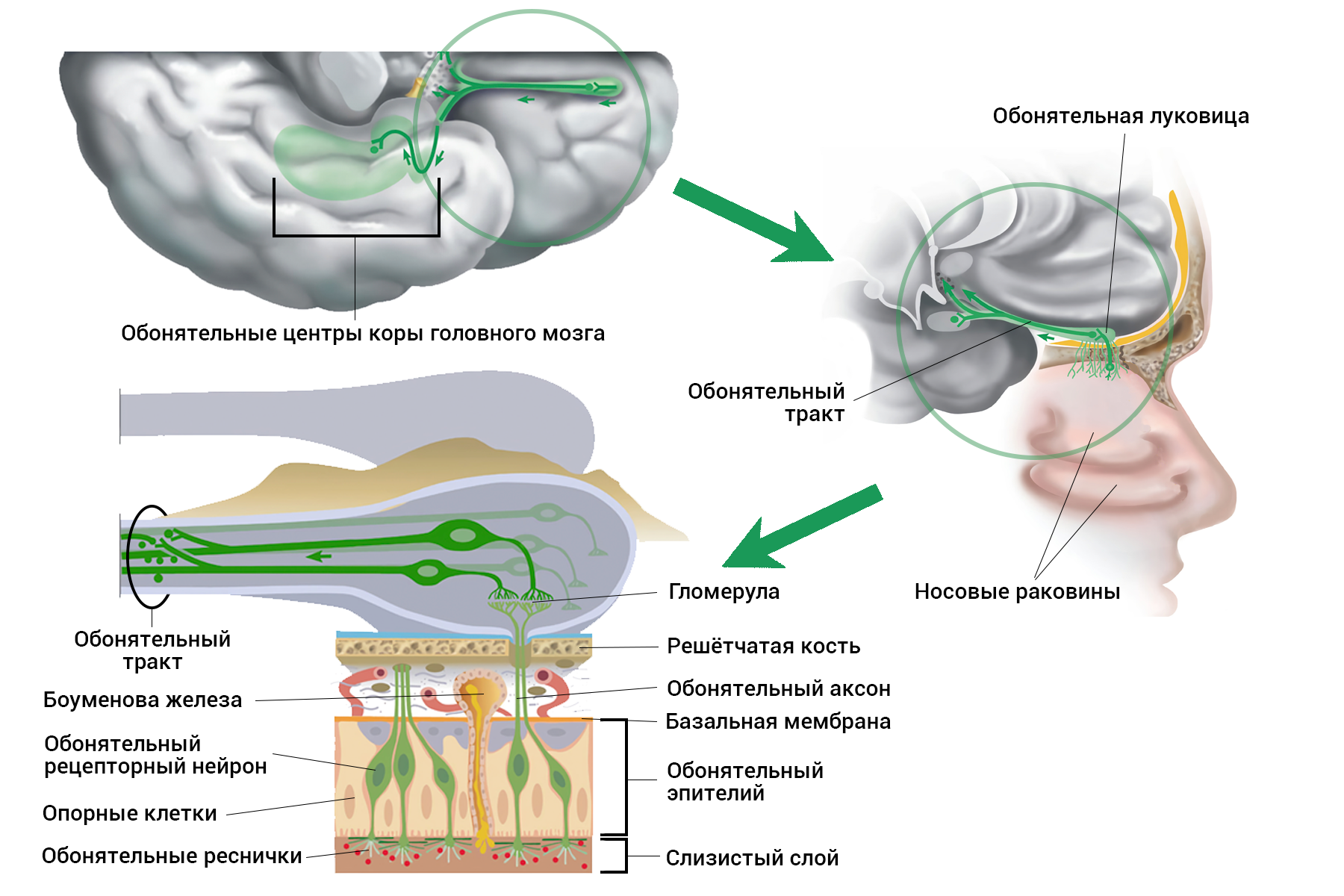
Рисунок 2. Строение обонятельной системы. Показаны основные структуры: окончания аксонов митральных и пучковых клеток в головном мозге — центральные проекции обонятельного тракта (обонятельные центры); обонятельная луковица с гломерулами, обонятельный тракт, строение обонятельного эпителия.
адаптировано из [61]
Глава I. С чего всё действительно начинается?
Начинается всё до рецептора
Итак, на периферии анализатора работают обонятельные биполярные нейроны. Это они известны уникальной для нервной системы способностью к обновлению. Укрывает их слой назального мукуса, в который с поверхности эпителия выглядывают реснички нейронов, которые делают их похожими на актиний (рис. 5). На ресничках расположены комплексы обонятельных рецепторов — самого многочисленного семейства среди рецепторов, связанных с G-белком (им посвящена одна из рубрик «Биомолекулы»). Когда молекула одоранта преодолеет слой мукуса, произойдёт ведущее событие трансдукции — она свяжется с рецептором. Однако обоняние может прерваться, даже не успев начаться.
Трансдукция — преобразование внешнего воздействия в код нервных сигналов.
Дело в том, что слизь в носовой полости совершенно не заслуживает негативных коннотаций. Помимо очевидной защитной функции, она обеспечивает удержание, транспорт и удаление молекул одоранта. При воспалении усиленная продукция слизи становится физически непреодолимым барьером для молекул. Что же входит в состав слизи кроме воды и ответственных за вязкость мукогликопротеинов? Это иммуноглобулины, цитокины, лизоцим и лактоферрин, кальций-связывающие белки псориазин и кальпротектин, различные пептидазы, калликреин, глутатион-S-трансфераза, карбоксилэстераза, дегидрогеназы, цитохром P450, пероксиредоксины, пероксидазы, Plunc — белок небно-легочно-назального эпителиального клона, ионы металлов, и главным образом одорант-связывающие белки [3] — список неполный, но внушительный. Более 400 молекул с различными свойствами, включая антимикробные и обезвреживающие ксенобиотики, защищают уязвимый сенсорный эпителий от внешнего воздействия.
Особого внимания заслуживают одорант-связывающие белки, далее OBPs (от англ. odorant binding proteins). Они принадлежат семейству транспортных липокалинов и помогают гидрофобным молекулам добираться до рецепторов. Вдобавок они помогают рецепторам расставаться с одорантами [4]. У человека пока известен единственный вид ОВРs, кодируемый геном OBP2A. И если не повезло с генетическим полиморфизмом, то молекулам не стоит ожидать комфортной дороги к рецептору: один из аллельных вариантов отличается низкой чувствительностью транспортного белка. Как следствие, развивается гипосмия [5].
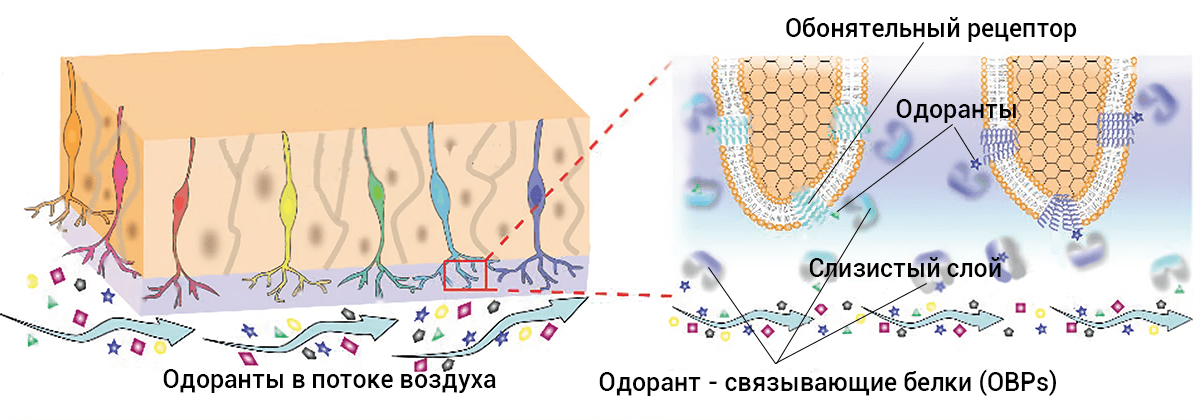
Рисунок 3. Одорант-связывающие белки в мукусе захватывают одоранты для их транспортировки к рецепторам на ресничках обонятельных нейронов.
адаптировано из [4]
С большим энтузиазмом к ОВРs относятся биоинженеры. Чем они ещё могли привлечь учёных? В мукусе ОВРs успешно функционируют в коктейле протеолитиков, а также они устойчивы к температурам и органическом растворителям. Остаётся научиться настраивать специфичность ОВРs или использовать уже имеющуюся — и в руках оказываются неплохие составляющие для создания искусственных сенсорных систем.
Часть ферментов из списка активна по отношению к самим одорантам [6]! Можно ли быть уверенным, что для рецептора, лишённого своего мукусного окружения, в эксперименте найдут правильный лиганд? Это ещё предстоит уточнить. Про связь состава слизи и возрастного ухудшения обоняния пока тоже непонятно. Не исключено, что в долгосрочной перспективе для дифференциальной диагностики синуситов и ринитов к цитологическим исследования мукуса, риноцитограммам, добавят и протеомный анализ [7], [8].
Помощь со стороны
Также в мукусе комфортно живут бактерии со своими разнообразными ферментами и метаболитами (часть из которых будут одорантами). Кто особенно интересуется микробной флорой носа? К сожалению, таких мало. Но если хочется привлечь к исследованию безмикробных мышей, то это стоит учитывать [9]. Обоняние у животных занимает не последнее место, и действительно, поведение мышей с бактериально осиротевшим обонятельным эпителием может отличаться. А влияют ли сами бактерии на остроту нашего нюха? Пока знание об этом в зачаточном состоянии. Подозревают, что есть бактерии, потеря которых будет критической [10]. Но всё же основной принцип скорее «больше — не значит лучше». Причём как количественно — усиленное заселение бактериями блокирует доступ для молекул, — так и качественно. Шведские учёные обнаружили, что у людей, чей балл TDI был меньше нормы, в мукусе носа есть характерные для кишечника и полости рта виды фекалибактерий, энтеробактерий, порфиромонад [11].
К слову об оценках. Для объективного исследования обоняния вычисляют TDI-индекс (общий индекс обоняния). Он рассчитывается по данным тестов, оценивающих: threshold — порог восприятия (например, бутанола-1), discrimination — показатель дискриминации запахов (в тройке просят найти отличающийся от двух запах), identification — показатель идентификации запахов.
Исследователи предполагают, что, в отличие от кишечника, увеличенная продукция бутирата этими видами оказывается в носу не к месту. Порфиромонаду, кстати, можно было заметить на страницах ноябрьского Nature [12]. В специальном материале вновь обсуждали статус инфекционной гипотезы Альцгеймера. У этого вопроса тернистый путь длиной в десятилетия, и, чтобы разрешить все сомнения, знаний пока недостаточно. Однако, кажется, уместно размышлять, что обонятельный эпителий как минимум упрощает микробам доступ в ЦНС.
А вот об участии бактерий в том, как мы пахнем, известно однозначно. В неприятном для большинства запахе пота можно обвинять, например, колонии коринебактерий и стафилококков. Они превращают аминокислоты в характерно пахнущие изовалериановую кислоту и серосодержащие вещества. В исследовательском отделе швейцарской фирмы Живодан активно исследуют, как мы приобретаем свойственный нам запах и как воспринимаем чужие. Оказалось, что основной вклад в подмышечный аромат вносят продукты специального фермента коринебактерий — Nα—ацил-глутамин-аминоацилазы и производимых ею карболовых кислот. Ещё исследователи смогли установить, как распространённый в Восточной Азии полиморфизм гена ABCC11 (кодирует АТФ-связанные кассетный транспортер) связан с почти полной потерей привычных для нас компонентов запаха [13]. Многие читатели наверняка знакомы с историей, заманчиво намекающей нам его важность. В 1995 году впервые сообщили о связи HLA-генотипа (от англ. Human Leukocyte Antigens — человеческий лейкоцитарный антиген) и индивидуальной привлекательности запаха. Речь шла о соединениях, не являющихся феромонами. Естественный вопрос — что же могло пахнуть? Вы могли слышать, что HLA принимает участие в диалоге бактерий и иммунной системы, а значит способен влиять на состав микробиома и производимые запахи. Следовательно, оценка чужого запаха как приятного или нет может зависеть от бактериальных метаболитов? Но не стоит поддаваться соблазну — подобное объяснение приводит в тупик. Исследования ассоциированного с HLA запахового паттерна пока не дают результатов, а к известному эксперименту с футболками тоже есть вопросы , [14]. Но думаю, никто не будет спорить, что неприятный запах тела приводит к социальному изгнанию. Ещё, как показала Джой Милн, они могут предупреждать о болезни Паркинсона.
В 1995 году профессор Клаус Ведекинд собрал почти 50 мужчин, которые согласились на два дня отказаться от любой парфюмированной химии и не менять футболку. Примерно столько же женщин согласились оценить, насколько привлекательным им кажется запах этих футболок. Он обнаружил, что чем больше генотип HLA у женщины отличался от мужчины, носившего футболку, тем положительнее была оценка его запаха. Этот эксперимент запомнился как «опыт с пахнущими майками».
Диагностика болезней по запаху — вполне перспективное занятие. Джой Милн потеряла мужа из-за болезни Паркинсона. Она заметила изменения — странный запах — ещё за несколько лет до постановки диагноза. Познакомившись с другими больными, она поняла, что так пахнет эта болезнь. В прошлом году сообщили, что наконец удалось выяснить, какие пахучие молекулы ответственны за этот аромат. Полагаться только на людей с «супер-нюхом» нельзя, поэтому для диагностики активно разрабатывают электронные устройства. Кстати, «Биомолекула» уже писала о них [15].
Другими словами, запахи важны для нашей повседневной жизни. Пусть даже вам неинтересны детали химического общения людей. Но, может, вы всегда мечтали к просмотру любимого кулинарного шоу добавить еще и запахи. Не стоит ошибочно полагать что исследования мукуса недостойны научного изыскания. Мукус — это не просто 95% воды, это — биологически активная система. Ферментативные превращения веществ в мукусе и участие микробного сообщества — возможный источник несоответствия между нашим восприятием и ответами рецепторов в чашке Петри. Если мы хотим достойно воспроизводить воспринимаемые запахи, то нужно иметь в виду перирецепторные события (так называют события, предшествующие активации рецептора) [16].
Второстепенных ролей не существует
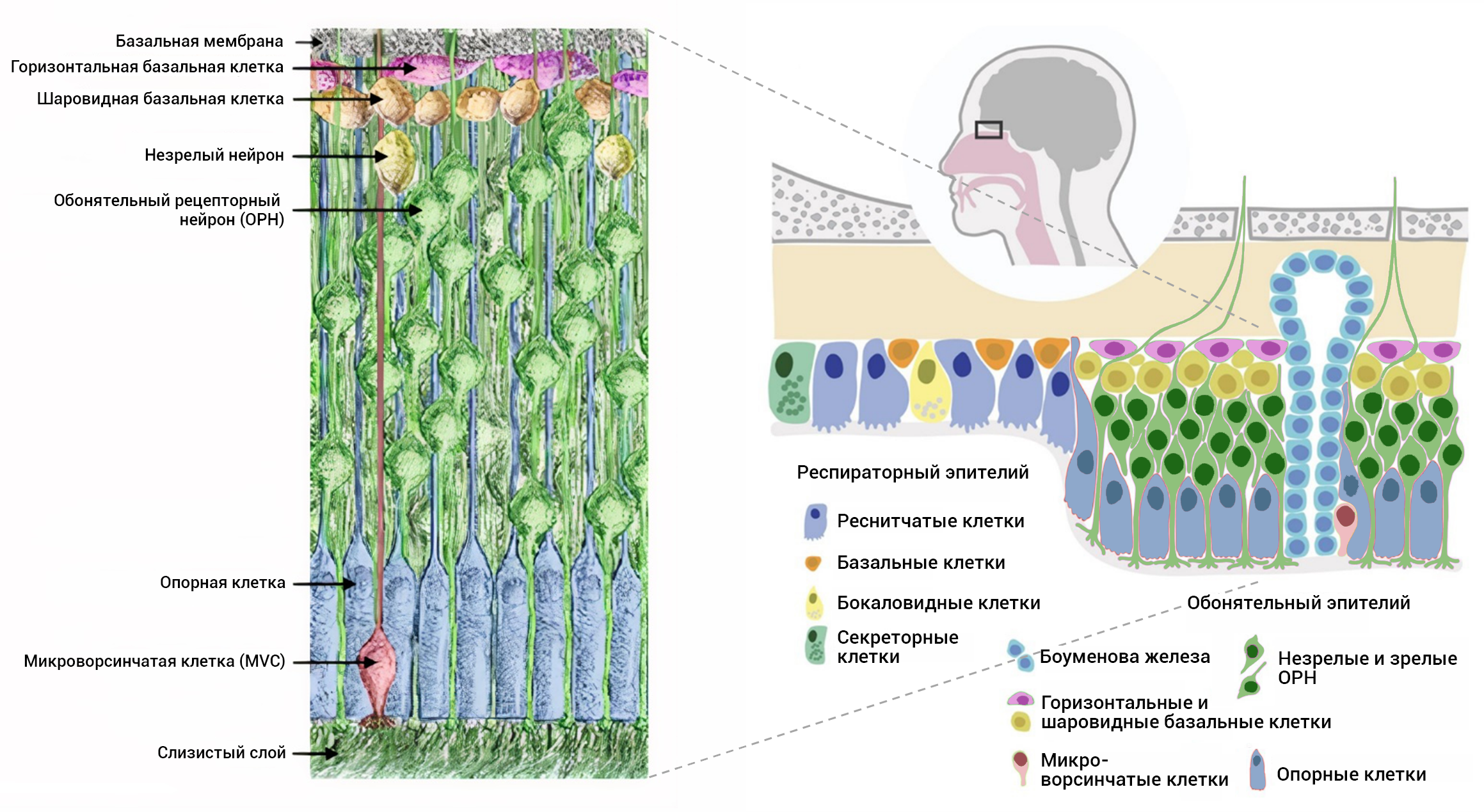
Под слоем мукуса мы найдём обонятельный эпителий (рис. 4). В его составе традиционно выделяли три группы клеток — собственно обонятельные нейроны, окружающие их опорные клетки и базальные стволовые клетки. И в дополнение — железы Боумена. Впрочем, об обонятельных нейронах и их ресничках (цилиях) речь пойдет чуть позже.
Трава под ресничками нейрона (рис. 4) — это микроворсинки клеток с одноимённым названием — микроворсинчатые клетки (англ. microvillar cells, MVS), а также опорные клетки (англ. sustentacular cells). Опорные клетки производят компоненты мукуса, окисляющие ксенобиотики, а также механически поддерживают и разделяют нейроны. Истинные взаимоотношения клеток эпителия намного сложнее, чем принято считать. Например, зачем микроворсинчатым клеткам экспрессировать канал TRPM5, больше известный как рецептор горького вкуса? Оказывается, это тоже инструмент защиты эпителия, он связывает подозрительные метаболиты. На это клетка отвечает выделением ацетилхолина, который, в свою очередь, стимулирует опорные клетки (это проявление паракринной регуляции): сигнального кальция в опорных клетках становится больше, и клетки активнее производят защитные ферменты [17]. Увы, разнообразие мембранных белков не-нейрональных клеток эпителия иногда оборачивается проблемами. Например, обнаружили, что проникновение нового коронавируса происходит через связывание с сериновой протеазой-2 TMPRSS2 (от англ. Transmembrane protease, serine 2) и ангиотензинпревращающим ферментом 2 ACE2 (от англ. Angiotensin-converting enzyme 2) на микроворсинчатых и опорных клетках. Эти «рецепторы» также есть и на глубоко лежащих базальных клетках, и в тканях мозга. Возможно, при их повреждении и наблюдаются случаи длительной аносмии и других менее типичных симптомов [18], [19]. Различные белковые комплексы могут сходным образом открывать двери и для входа других патогенных организмов.
Есть и другие угрозы для целостности эпителия: контакт с агрессивными химическими реагентами и лекарствами может привести к гибели опорных клеток. За ней последует апоптоз обонятельных нейронов и аносмия. Потенциально на это способны многие вещества, например, известный кожный аллерген — сульфат никеля, применяемый в промышленности и, вполне возможно, до сих пор встречающийся в косметических изделиях.
Иногда отлаженная работа клеток эпителия оказывается под атакой системных заболеваний. Например, до 70% процентов больных муковисцидозом в некоторой степени утрачивают обоняние. Муковисцидоз — это тяжелое заболевание, вызванное мутациями гена хлорного канала CFTR (от англ. Cystic Fibrosis Transmembrane conductance Regulator). Такой канал есть на подтипе микроворсинчатых клеток, производящих нейропептид Y, который, к слову, провоцирует усиленную пролиферацию стволовых клеток, а сам канал CFTR координирует гомеостаз обонятельного эпителия [20]. Так, потеря канала приводит к истощению слоя мукуса, поскольку вода и натрий стремительно направляются внутрь клеток. В сочетании с увеличеной продукцией нейропептида Y и активацией иммунного ответа обонятельный эпителий функционирует хуже [21] — отсюда и ухудшение обоняния. Все связующие звенья этого процесса ещё предстоит узнать. Но, возможно, по следам этих экспериментов получится создать клеточные модели заболевания.
Сами обонятельные нейроны сменяют друг друга каждые 30–40 дней. Меняются и поддерживающие клетки. Их последователи развиваются в основном из шаровидных базальных клеток. Считается, что горизонтальные стволовые клетки — это экстренный резерв при повреждении эпителия. В грубом приближении истощение ресурсов стволовых клеток — причина наступления аносмии с возрастом (пресбиосмия).
ГЛАВА II. Удивительные обонятельные нейроны
Много миллионов антенн
На 2,5 квадратных сантиметра обонятельного эпителия (рис. 5) приходится с десяток миллионов нейронов. Каждый зрелый нейрон обслуживают 15–30 ресничек, служащих для принятия, усиления и передачи химического сигнала. Они пробиваются из обонятельной булавы нейрона — окончания единственного дендрита нейрона. Благодаря этим ресничкам нейроны, спрятанные в эпителии, увеличивают площадь контакта с внешней средой, не подвергая себя лишнему воздействию. На мембранах ресничек находятся не только рецепторы, но и все детали классического сигнального каскада. Если правильность их установки или сборка цилий нарушается, то страдает обонятельная функция. Все компоненты для сборки и содержания приходят из цитоплазмы, поскольку в цилиях нет своих митохондрий и белоксинтезирующего аппарата.
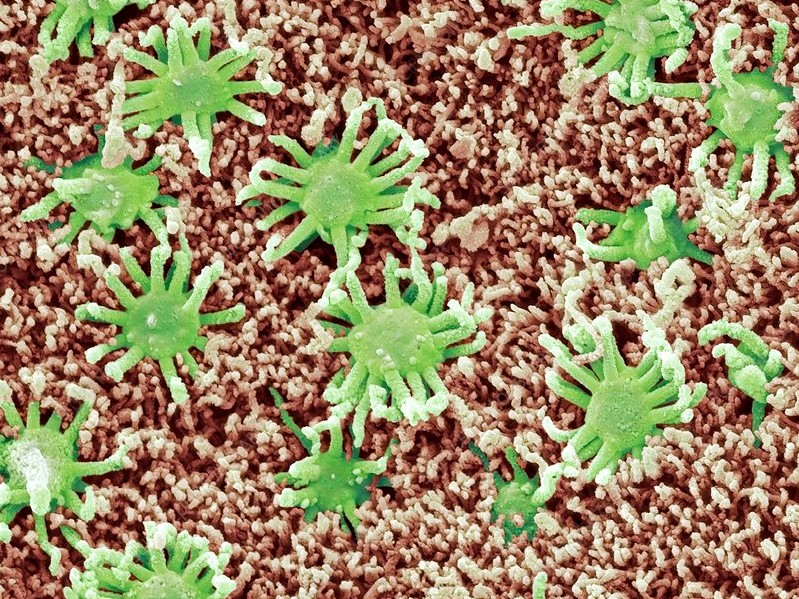
Рисунок 5. Выстилка носа (обонятельный эпителий). Изображение получено методом сканирующей электронной микроскопии. Помимо ресничек и булавы обонятельных нейронов (выделены зелёным цветом) видны мироворсинки опорных и микроворсинчатых клеток (выделены коричневым цветом).
Цитоплазму и цилии связывает система интрафлаггелярного транспорта (ИФТ) (от лат. intra — внутри и flagellum — бич, жгут). В заметке Кейта Козмински, который, будучи аспирантом 30 лет назад изучал ИФТ, можно узнать о хитросплетениях исследований и их возрождении [22]. Другая основательная статья о роли этой системы была опубликована в 2002 году [23]. Основные участники системы — ИФТ-субкомплексы А и В (рис. 6), моторные белки и октамерный комплекс белков ББСома (англ. BBSome) (рис. 6). Если какие-то детали выпадают, то развиваются цилиопатии. Это гетерогенная группа патологических состояний, среди которых присутствует и потеря обоняния. К сожалению, из-за повсеместности цилий (они есть на поверхности очень многих клеток в организме) одновременно нарушается работа сразу нескольких органов (почки, печень, различные протоки и т.п.) [24].
Комплекс ББСомы назван так по синдрому Барде-Бидля (англ. Bardet-Biedl syndrome). Среди вторичных симптомов этого заболевания есть и аносмия. Правда, она развивается по-разному — в зависимости от поврежденных генов. Последствия одного из выявленных генетических вариантов — дезорганизация микротрубочек в цилиях [25], [26].
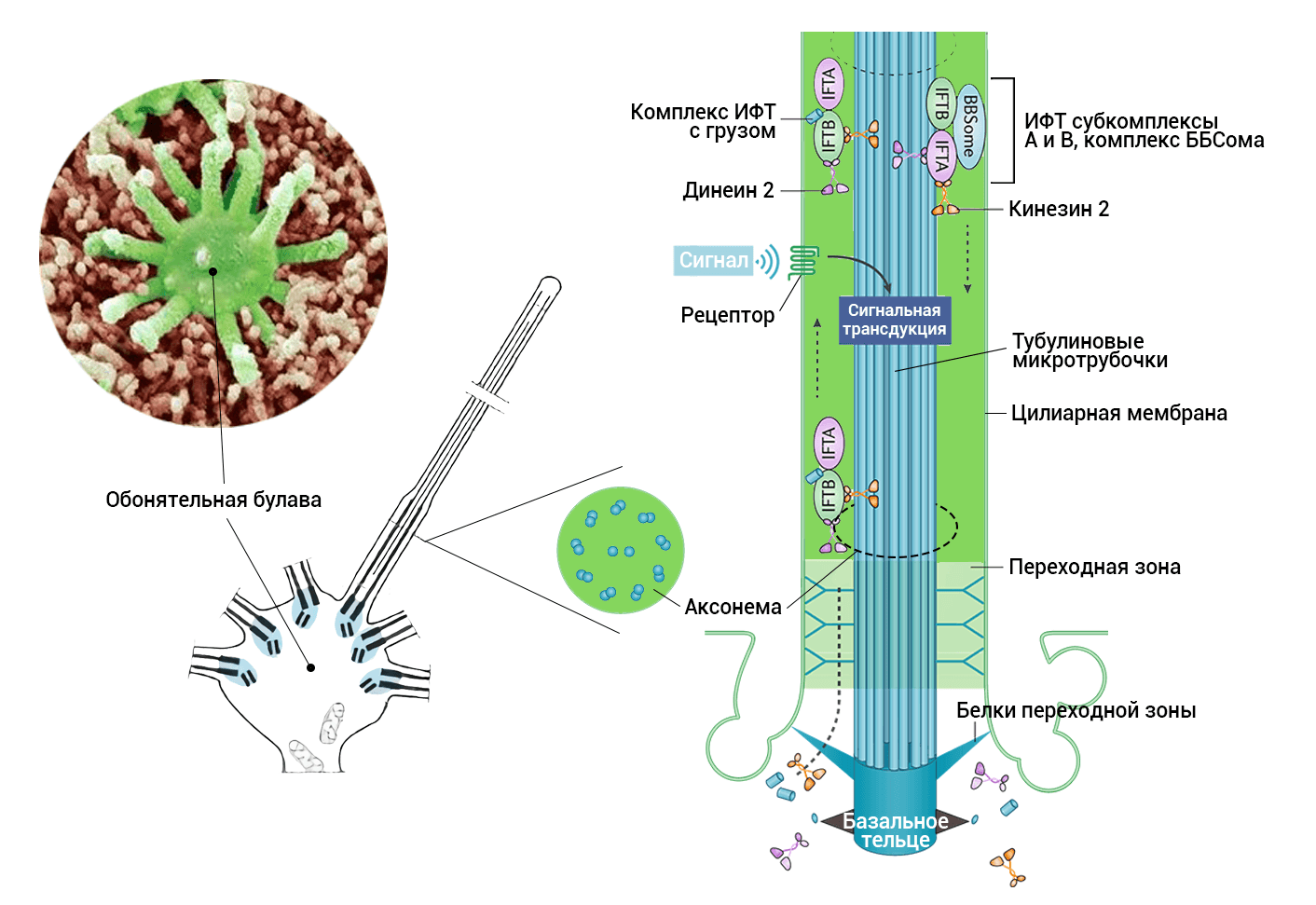
Рисунок 6. Строение неподвижных ресничек (цилий) обонятельных нейронов. Основная структура цилий — это 9 дуплетов микротрубочек и две в центре. На схеме показано расположение ещё одного необходимого элемента — базального тельца в основании цилий, а также переходной зоны, в которой и обнаруживается белок CEP290. На рисунке обозначены участники системы интрафллаггелярного транспорта — это ИФТ-частицы, состоящие из ББСомы; моторные белки (кинезины и динеины, в зависимости от направления движения), ИФТ-субкомплексы А и В. ИФТ-частицы переносят компоненты микротрубочек, цилиарной мембраны и мембранных белков.
адаптировано из [26]
Природа цилиопатий в целом пока плохо изучена, но зато некоторые из них уже можно остановить. Сейчас открываются большие перспективы для лечения моногенных цилиопатий (заболеваний, вызванных мутацией в единственном гене). В нескольких исследованиях показали принципиальную возможность вернуть реснички к рабочему состоянию, доставив обонятельным нейронам корректную версию гена для синтеза ИФТ-88 (один из белков в составе ИФТ-частиц). Интраназальная эктопическая аденовирусная терапия не только помогла улавливать запахи на уровне периферии, но и восстановила аксонные связи в вышележащих отделах анализатора [27], то есть вернула возможность по-настоящему ощущать запах.
Есть и другой пример возможного подхода к лечению. Известно, что на входе в реснички работает центросомальный белок CEP290 (англ. Centrosomal Protein 290, который назван так по своей массе). При некоторых мутациях этот страж ворот становится резко избирательным, не позволяя G-белку занять своё место в сигнальном каскаде. Результат этого вполне ожидаемый — аносмия [28]. Для многих заболеваний проверка обоняния — доступный диагностический признак, как в случае амавроза Лебера — врожденного повреждения сетчатки. Один из 11 типов этого заболевания связан с мутацией CEP290, конкретно — десятый тип. А в марте 2020 года в Nature сообщили о старте «Brilliance» — клинического испытания технологии CRISPR/Cas9. Однократное субретинальное применение препарата должно помочь при лечении амавроза лебера 10 (LCA10) [29]. Наверное, если получится вернуть зрение, то и на возвращение обоняния тоже можно рассчитывать.
У подавляющего большинства с цилиями, к счастью, все в порядке. Что же дальше? Молекула, преодолев слой мукуса и приблизившись к цилиям, окажется в ловушке рецептора, и запустится сигнальный каскад.
Уловить и усилить
Связывание одоранта с рецептором запускает классический сигнальный каскад циклического аденозиномонофосфата (цАМФ) (рис.7) За активацией рецептора следует активация упомянутого G-белка, специфичного для обоняния — Golf; потом включается аденилатциклаза АЦIII, уровень цАМФ повышается, открываются ионные каналы, потенциал на мембране меняется, и по длинному аксону уходит потенциал действия (рис. 7). Потеря любого ключевого игрока сигнального каскада закономерно приводит к аносмии, но настолько радикальные мутации наблюдают скорее в лабораторных условиях, чем в клинике.
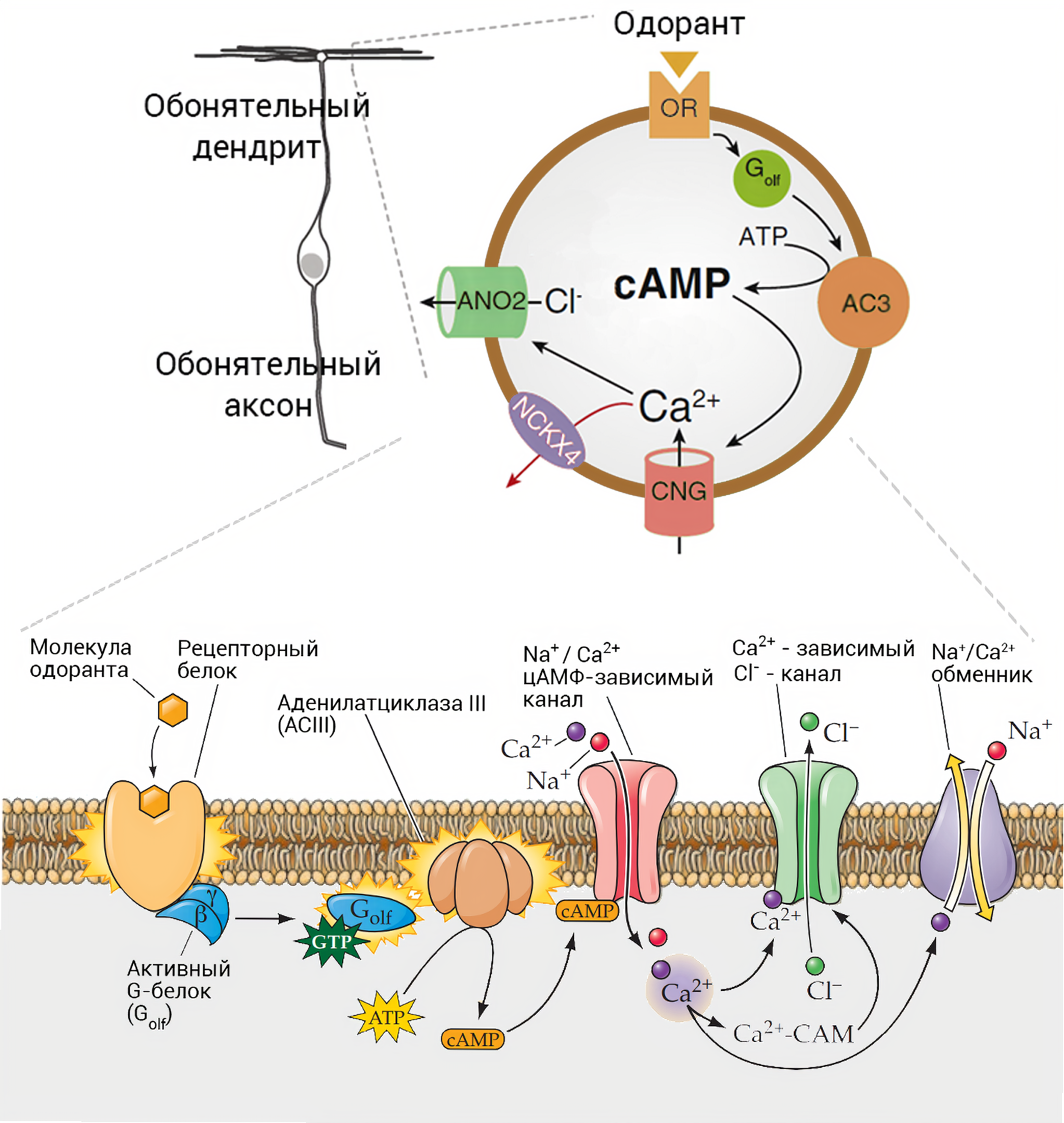
Рисунок 7. Схема обонятельной трансдукции. Связывание молекулы одоранта с рецептором запускает процесс взаимодействия с G-белком, что активирует аденилатциклазу III. Образуется цАМФ, который открывает цАМФ-зависимые каналы. В клетку поступают Ca2+ и Na+. Ca2+ cвязывается с хлорным каналом, через который Cl− выходит из клетки.
Каскад вторичного посредника цАМФ — это распространенная в организме схема усиления сигнала. Впрочем, и здесь не без странностей. Внешний мир и обонятельный эпителий разделяют около 15 микрометров мукуса. А на его ионный состав влияет множество факторов, начиная с погоды за окном. Поэтому полагаться на привычный (например, как в зрении) входящий натриевый ток было бы опрометчиво. Альтернатива? Выпускать запасённый хлор Cl−, который активно поступает через белковые транспортеры в резервуар — сому и дендрит нейрона. Получается, кальций, попавший внутрь через неселективный катионный канал CNG (cyclic nucleotide-gated), открывает канал семейства аноктаминов (Anoctamin 2) для выхода хлора. 90% деполяризации нейрона — это выходящий хлорный ток [30]! Исследуя природу рассеянного склероза в одном из крупнейших центров в Швеции, SciLifeLab обнаружили, что у аноктамина-2 и антигена вируса Эпштейна-Барра есть похожие аминокислотные последовательности. Это называется молекулярной мимикрией, которая приводит к перекрёстной реактивности между антителами к каналу и вирусу. Пока предстоит выяснить, как провоцируемая вирусом иммунная реакции вписывается в этиопатогенез рассеянного склероза. Но известно, что канал представлен и в других частях мозга, а обсуждаемых антител в бляшках было подозрительно много. Можно предположить, что потеря обоняния и атака каналов в других областях могут выступать как более ранние диагностические проявления [31]. Вообще, о событиях трансдукции в обонянии известно давно. К 1990-ым годам провели ключевые эксперименты, определяющие роль обонятельного белка Golf и вторичных посредников [32]. Эти исследования и предвосхитили Нобелевскую премию 2004 года: благодаря страстной решительности учёных работа по поиску генов обонятельных рецепторов увенчалась успехом. Как вспоминают, это было поворотным событием в изучении обоняния.
Участвуют сотни
Говорят, чувство юмора — явление расплывчатое. Оно зависит как от наших собственных вкусов и привычек, так и от окружения. Конечно, нашему восприятию запахов не приписывают национальные ярлыки, но с обонянием похожая ситуация. Наши сенсорные клетки умело настраиваются на определённые ароматы: например, учатся быстрее сообщать, что в плите стоит вкусный пирог, или напротив, стараются не замечать некоторые запахи (скажете ли вы сейчас, чем пахнет ваш дом?), а мы сами в течение жизни учимся интерпретировать запахи как приятные или неприятные. Причины этого — в пластичности и субъективности обоняния, которое более других чувств связано с повседневными предпочтениями. Во-первых, запахи вокруг начинают влиять на наше восприятие ещё до рождения [33], [34]. Во-вторых, рецепторов (очень полиморфных) к одорантам почти четыре сотни, что не сравнить с известными со школы тремя видами колбочек. В 1991 году эта цифра, которая, например, для слона в пять раз больше, взволновала научное сообщество. А разговор о первичных запахах на какое-то время свели на нет.
Благодаря кропотливой работе американских учёных Линды Бак и Ричарда Аксель были определены гены, кодирующие одорант-связывающие рецепторы. Их коллега, Стюарт Фиерштайн вспоминает, что открытие генов — это результат упорства Бак, которая поставила на кон многое. Она присоединилась к лаборатории Акселя с однозначной целью — найти эти гены, которые к тому моменту безрезультатно искали несколько групп учёных. Три года работы без публикаций оказались оправданным риском. В недавно изданной книге Smellosophy (от сочетания слов smell — запах и philosophy — философия) можно найти и воспоминания самой Бак о проделанной работе, а также мысли других пионеров в области обоняния и запахов обоняния. Автор книги — историк науки Энн-Софи Барвич, которая собрала материалы о методологических и экспериментальных проблемах в исследованиях обоняния и рассказала историю их развития, начиная с античных времен. В эпиграфе — цитата Линды Бартошук: «Обоняние — это единственное чувство, для которого мы можем создать новый стимул, которого никогда не было на земле, и мы можем его воспринимать» .
«Smell — it’s the only sense for which we can create new stimulus that’s never been on the face of the earth and we can perceive it».
Кому-то это высказывание покажется спорным, но у него есть даже количественные аргументы. Недавно, коллектив из Монелловском Центре по изучению химических чувств и Brain Team из исследовательского подразделения Google сообщили (пока на стадии препринта [35]), что более 30 миллиардов молекул в мире могут быть запахами, а знаем и изучаем мы около 0,000002%! А значит, создавать новые ароматы можно ещё долго.
Пока, правда, непонятно, сколько существует способов сложить из миллиардов одорантов запахи таким образом, чтобы мы их восприняли. В 2014 году в прессе активно обсуждали, что это «больше триллиона» [36]. Однако есть основания подозревать, что это число несколько завышено [37].
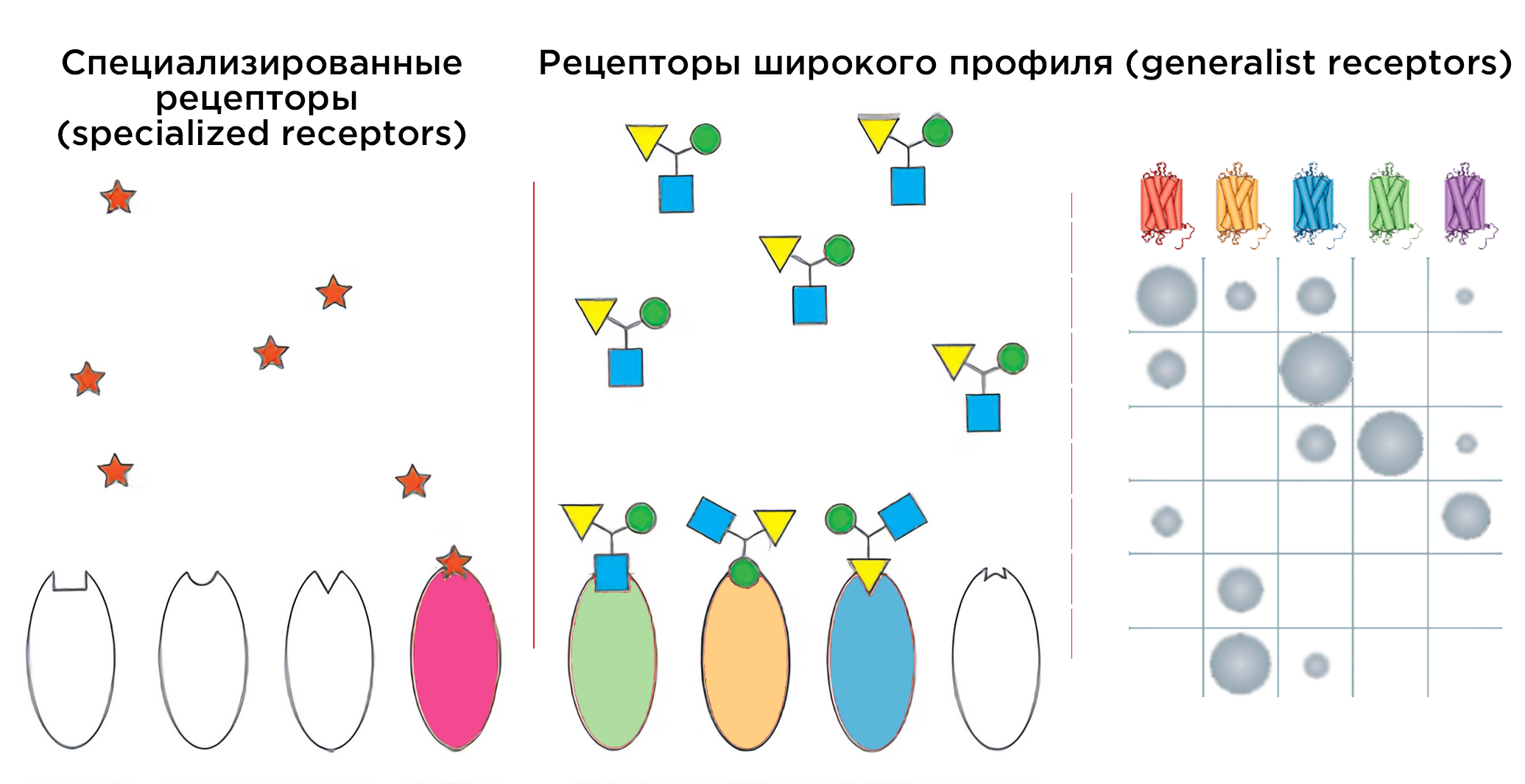
Рисунок 8. Одоранты могут активировать два типа рецепторов. Сигнальные вещества связываются со специализированными рецепторами (specialized receptors). Например, рецептор AgOr1 у малярийных комаров связывает компонент пота человека, 4-метилфенол [64]. В то же время, у другого типа рецепторов (generalist receptors) широкий репертуар связываемых одорантов. Благодаря им и работает комбинаторный принцип обоняния. На схеме справа по горизонтали — гипотетические ответы разных рецепторов на предъявляемые одоранты. Размер круга отражает силу ответа (рецепторные потенциал).
За определением генов последовал и принцип работы рецепторов — комбинаторный. Воспринимаем мы всё-таки гораздо больше, чем 400 запахов. Согласно комбинаторному принципу (рис. 8), молекула активирует несколько рецепторов, а большинство рецепторов реагируют на обширный репертуар одорантов («рецепторов широкого профиля»). Нашли и «рецепторы-специализаторы» для жизненно важных запахов, которые не следуют этому принципу (рис. 8). Но существование таких узконаправленных рецепторов у человека — предмет научного спора.
Ещё в 1967 году Джон Эймур , предрекая рецепторную природу, писал в Nature об избирательных аносмиях (selective/specific anosmia)— невосприимчивости к отдельным одорантам как о возможности разгадать обоняние. По аналогии с дальтонизмом рассчитывали установить первичные запахи и расшифровать обонятельный код [38].
Джон Эймур — один из лидеров науки об обонянии прошлого века. Среди его заслуг — создание стереохимической теории обоняния.
Оказывается, почти все мы аносмики к тем или иным веществам [39]. Однако обнаружить дефекты отдельных рецепторов сложно из-за их широкой настройки и многокомпонентности запахов. Более того, если считается, что сольная активация одного типа рецепторов не определяет запах, то как восприятие зависит от индивидуального набора генов? Выручило разнообразие резких и неприятных запахов вокруг, к которым некоторые оказывались подозрительно терпимы. Основы психофизической оценки масштабы избирательных аносмий заложили давно, а сейчас у нас есть и адекватные методы, чтобы соотнести особенности восприятия с генетической изменчивостью [40].
Самый известный пример — восприимчивость к стероиду андростенону. О том, как она зависит от генотипа рецептора OR7D4, уже писали [41]. От 20 до 30 процентов людей не находят его запах отталкивающими, а для других он будет иметь характерный запах пота. Полезно знать, что если вам явно неприятен запах андростенона, то возможно, и трюфели не вызовут у вас восторга. Считается, что присутствие этого стероида в составе делает из чувствительных к нему свиней умелых охотников. Другой случай: если ваше предложение пообедать блюдом вьетнамской кухни воспринимали с заметным отвращением, то возможно, вам повезло столкнуться с ещё одним частым аллельным вариантом. В составе ставших популярными супов фо есть кинза и кориандр. Это зелень и семена одного растения — Coriandrum sativum. Альдегиды — ключевые компоненты аромата кориандра — детектируются рецепторами по-разному. Полимофизм около гена рецептора OR6A2 связывают с наследственной составляющей неприязни к характерному для этих веществ мыльному запаху и вкусу , [42].
Вкус по большей мере определяется тем, что уловит обонятельный эпителий во время приема пищи. Это известно как обратное, или ретроназальное обоняние.
Удивительно, что часто нарушение функций рецептора меняет качественную оценку запаха, а не порог восприятия. Это, в свою очередь, помогло пересмотреть идею о том, что в обонятельном рецепторе есть нейроны, сообщающие о концентрации вещества. Просто в зависимости от концентрации активируются разные рецепторы. Но это также создает новые вопросы: как же формируется наше эмоциональное отношение к запахам? Между тем, практических последствий у таких исследований больше, чем кажется на первый взгляд. Например, одно из направлений Моннелевского центра — суметь замаскировать противный вкус жизненно важных лекарств. В частности, это исключительно важно при лечении детей. Также неприятный запах из-за метаболитов лекарств полноценно заслуживает упоминания в списке побочных эффектов. Индустрия химической и пищевой промышленности ещё больше ценит понимание коллективных антипатий и ищет способы их скрыть. Предположим, мы удовлетворили праздное любопытство и узнали, что личная неприязнь к меню соседа за столом или к самому соседу происходят из-за генетической изменчивости. Зачем же искать то, что может активировать или блокировать рецепторы? Причин много: например, есть обонятельные рецепторы, которые непосредственно участвуют в нейропередаче!
За рамками «обонятельных»
До этого речь шла только об обонятельных рецепторах из группы OR (odorant, or olfactory receptor). Однако, у человека точно есть ещё один тип рецепторов, которые были открыты в начале века в качестве участников нейромедиаторной системы следовых аминов (trace amines). Эти рецепторы, ассоциированные со следовыми аминами TAARs (trace amine-associated receptors) в носу связывают следующие соединения: триметиламин, путресцин, кадаверин. «Запах тухлой рыбы», «запах гниющего мяса», «самый мерзко пахнущий цветок» (речь идёт о раффлезии), — если бы не они, мы бы не знали таких ощущений. Хотя некоторые могут знать их по-другому. В ноябре сообщили, что в результате полногеномного поиска ассоциаций (Genome-Wide Association Studies) с участием более 9000 тысяч человек нашли вариант гена TAAR5, при котором триметиламин воспринимается как нейтральный или даже «картофельный» аромат. Искали в Исландии, где хаукарль — вяленое ферментированное мясо акулы с высоким содержанием аммиака и триметиламина — признают национальным деликатесом. Так намного легче поверить, что и другие достояния северной кухни, известные содержанием триметиламина — сюрстремминг и лютефиск — не у всех в черном списке [43]. Триметиламин у других видов — сигнальное вещество. Собственно, и наше отвращение — это наглядная иллюстрация тесной связи эмоций и химических стимулов. На таких примерах удобно изучать кодирование «отталкивающих» сигналов. Многие в курсе, что нейронные процессы в основном изучают на грызунах. Но вот интересный феномен — крысы, как и мы, ненавидят триметиламин, а мышей он привлекает!
Как и обещали, рассказываем, что же с там нейромедиаторной системой! В организме образуются и собственные лиганды к TAARs, следовые амины. Только их очень мало, отсюда и название, поэтому до обнаружения рецепторов дискуссии об их роли были не очень продуктивными. За последние двадцать лет TAARs обнаружили в структурах лимбической системы (она оркеструет эмоциональные реакции), базальных ганглиях, ретикулярной формации и других зонах. Сейчас ясно, что рецепторы вовлечены в работу дофаминовой, серотониновой систем, а также в процессы нейрогенеза. Это не только фундаментальные знания, но и реальный шаг к созданию новых лекарственных средств. Рецепторы следовых аминов активно исследуют в Институте трансляционной биомедицины СПбГУ под руководством Рауля Гайнетдинова. Одна из последних работ учёных лишний раз демонстрирует глубокую и недооценённую связь обоняния и физиологии. Оказалось, в основе положительного (антидепрессивного) действия антагонистов TAAR5 лежат непростые отношения обоняния и центральных структур, в которых присутствует этот рецептор [44]! Помимо возможного вклада в нейрохимию и фармакологию, эта работа неожиданным образом раскрывает и потенциал ароматерапии. Среди известных блокаторов рецептора TAAR5 числится Тимберол — синтетическое вещество с хвойным запахом, активно используемое в парфюмерии. В начале века почти одновременно с TAARs (их обнаружили в 2001 году), узнали и о существовании канонических обонятельных рецепторов в других тканях. Решают они, правда, более конкретные задачи. Вот в 2003 году в Science пишут о первом случае эктопической (от греч. еktos — вне и topos — место) экспрессии обонятельных рецепторов, т. е. за пределами свойственного им эпителия носа. Оказалось, что на мембране сперматозоидов есть рецептор hOR17-4 (OR1D2), участвующий в хемотаксисе при оплодотворении. А один из его агонистов — пахнущий ландышем бурженаль (bourgeonal) [45]. Новость растиражировали в медиапространстве с ожидаемым заголовками, не нуждающимися в цитировании. Сейчас известно, что бурженаль — единственный одорант, который мужчины детектируют при меньших концентрациях, чем женщины. (Про природу различий остроты нюха можно прочесть в PubMed [46]). Пусть пока это просто занимательный факт, но есть вероятность, что ему найдётся применение и в клинике — ухудшение нюха по отношению к бурженалю наблюдают в некоторых случаях идиопатического бесплодия [47].
Вообще, «обонятельных» рецепторов за пределами носа довольно много [48]. Это неудивительно, ведь по сути обоняние — это вид хеморецепции. Удобно использовать компоненты этой системы там, где требуется решить задачу распознавания малых молекул. Функциональный характер у рецепторов пока нашли не во всех тканях (а это тимус, поджелудочная железа, кожа, мышцы, сердце, печень, мозг). Но также, как и в случае с TAARs, за открытием агонистов и антагонистов следует создание новых эффективных средств. Например, рецептор OR2AT4 в кератиноцитах и волосяных фолликулах реагирует на терпеноид сандалового дерева, потенциально становясь новым средством для ускорения заживления шрамов и активации роста волос [49]. Но на этом хочется остановиться — о разнообразии рецепторов и их функций можно говорить долго. Возвращаемся к основной функции — обонятельной. Напрашивается закономерной вопрос: как именно нейроны выбирают себе рецепторы? Точнее, один тип рецептора из нескольких сотен.
Один нейрон – один рецептор
Вслед за поворотной работой 1991 года, оба будущих Нобелевских лауреата продолжили (и продолжают сейчас) исследовать нюх. Стало понятно, что если бы на мембране нейрона сидели множество разных типов рецепторов, то нейронный ответ на смесь запахов превратился бы в какофонию. Интуитивный принцип «один нейрон — один рецептор» был вскоре доказан сотрудником лаборатории Акселя. Вот только гены обонятельных рецепторов встречаются на каждой, кроме 20 и Y хромосомах [50]! Получается, что для выбора одного аллеля одного гена рецептора привлекается большое число удалённых участков генома. То, как эти контакты организуются в клетке, изучает 3D-эпигеномика, но сложные межхромосомные взаимодействия пока понимают не до конца [51]. Несколько лет назад появились данные об участии в эпигенетической регуляции «... греческих островов: Липcи, Сфактерия, Крит, Родос...». Такое оригинальное название дали ключевым обонятельным энхансерам (регуляторные модули, активирющие транскрипцию генов). Про участие других регуляторных элементов недавно писали в Nature [52], [53]. В 2019 году главный приз ежегодной премии для молодых учёных, учреждённой Science и SciLifeLab, вручили за усовершенствование метода изучения организации хроматина: Hi-C, один из методов определения конформации хроматина, применили к индивидуальным диплоидным клеткам [54]. С помощью этого нового метода Dip-C (diploid chromosome conformation capture) визуализировали, как активные обонятельные гены взаимно подавляют транскрипцию остальных (рис. 9), [55].
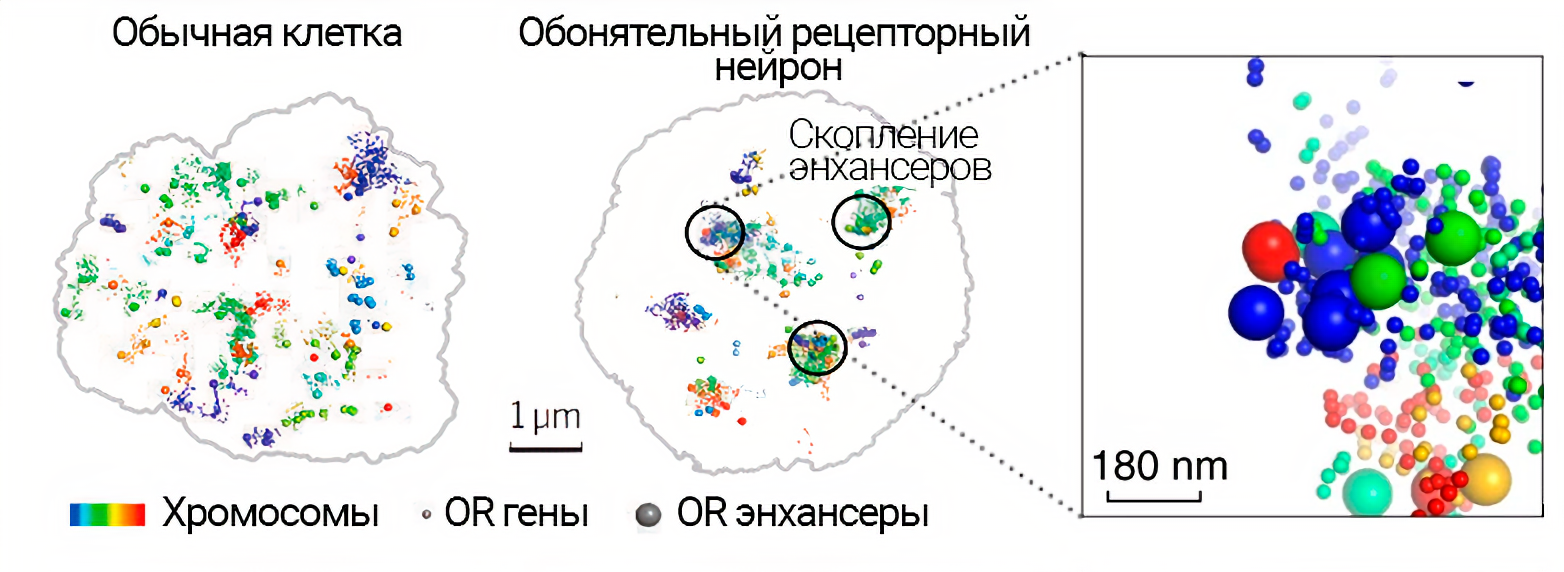
Рисунок 9. Межхромосомная агрегация генов обонятельных рецепторов OR (odorant receptors) и их энхансеров, построенная по данным метода Dip-C. Хромосомы обозначены разными цветами. Отдельно вынесена увеличенная визуализация наиболее плотного скопления генов OR и энхансеров: разные цвета обозначают принадлежность разным хромосомам; малые сферы представляют гены, а сферы с большим диаметром — энхансеры.
адаптировано из [66]
Свой рецептор (собранный из двух наборов хромосом) нейрон выбирает во время созревания. Это своеобразный «код принадлежности» нейрона. И он использует его дважды: рецепторы экспрессируются не только на цилиях, распознавая молекулы одорантов, но и на аксоне!
ГЛАВА III. Куда ведут нейроны?
Неразборчивая картография
Аксоны нейронов с одинаковыми обонятельными рецепторами встречаются в обонятельном клубочке, или гломеруле. Гломерулы — это составные единицы обонятельной луковицы (рис 10). На смесь запахов (которые мы называем одним словом: кофе, какао и т.д) реагируют определённые комбинации гломерул. Такие перекрывающиеся схемы активации называют «картами запахов», или «отпечатком запаха» (англ. «odor maps», или «odor images»).
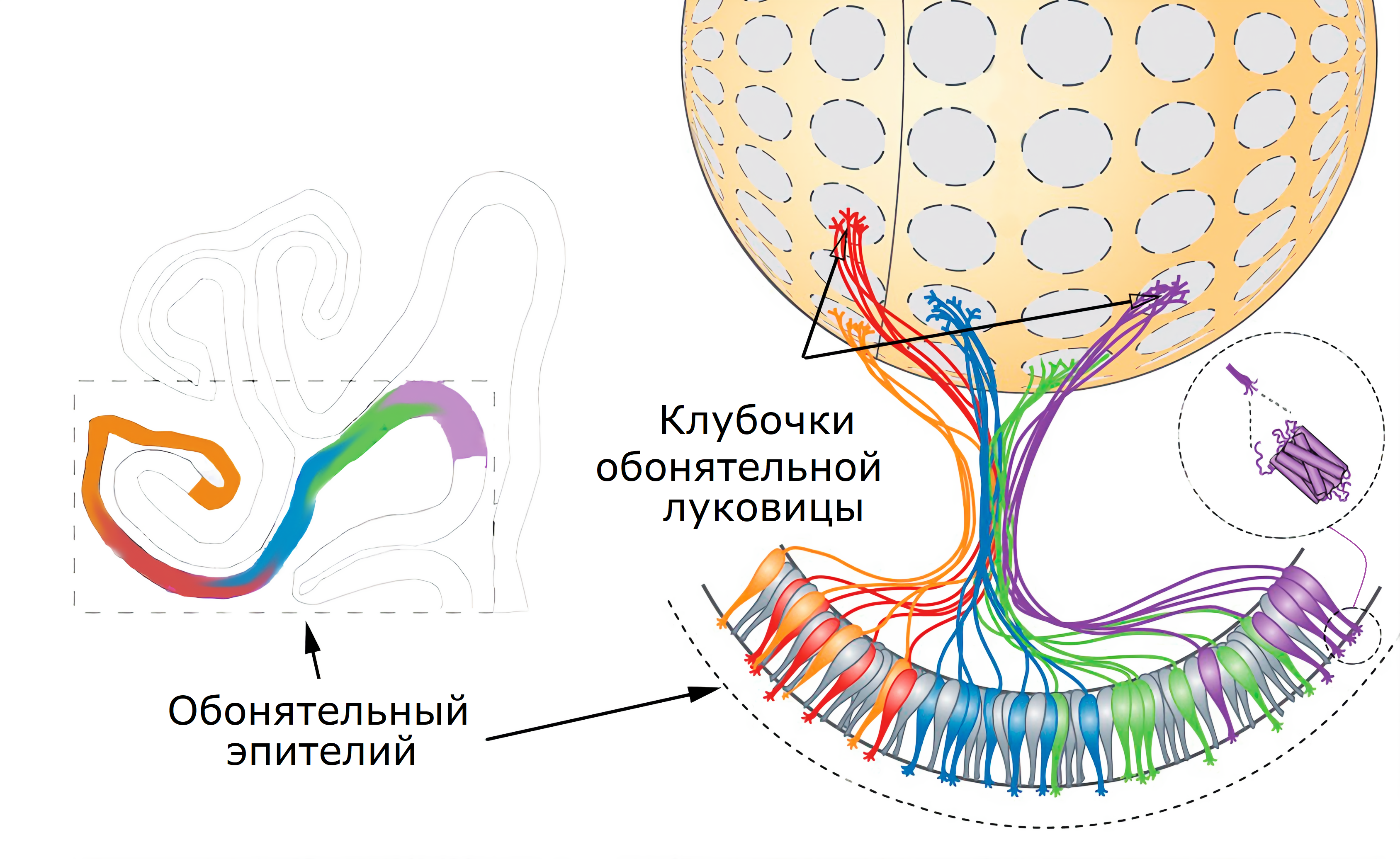
Рисунок 10. Схематическое изображение аксонов нескольких нейронов с одинаковыми обонятельными рецепторами, собранных в одном клубочке (гломеруле) обонятельной луковицы. Окраска обонятельного эпителия в носовых пазухах (рис. 11) отражает перекрывающиеся зоны экспрессии — рецепторы случайно занимают положение в пределах этих зон (т.е. они всё-таки следуют некоторым правилам топографической организации).
Нейроны с разными типами рецепторов в эпителии перемешаны, а ещё они постоянно обновляются. Как же тогда аксоны находят своих будущих соседей? Поиск своего клубочка задействует механизмы аксонального наведения (англ. axon guidance), в котором белки обонятельных рецепторов на аксонах и есть главные ориентиры. Изящное решение, но процесс этот довольно сложный. Много разных молекул участвует в формировании мозаики обонятельной луковицы: протокадегрины, цАМФ, белок ОМР — маркер обонятельных нейронов — и прочие компоненты. Эксперименты на мышах показывают, что потеря некоторых из них может нарушить правильную сортировку аксонов по клубочкам. Все детали ещё предстоит выяснить, но вклад вносят не только молекулярные взаимодействия. По дороге к клубочкам длинные аксоны нейронов пересекают продырявленную пластинку решётчатой кости (рис 11). Они проходят через неё в составе пучков, окружённых обволакивающими глиальными клетками (это и есть обонятельный нерв). К сожалению, «перерезка» аксонов костью при травмах головы грозит серьезными последствиями — аносмией или значительной гипосмией. Причина в том, что новые созревающие нейроны больше не могут добраться до гломерул обонятельной луковицы: им необходим «каркас» из существующих нейронов, который и разрушается при механических повреждениях.
Поиск своих позиций нейронами в процессе эмбриогенеза осуществляется ещё более запутанным путём, поэтому не станем описывать весь процесс в деталях. Но рассказывая об аносмии, нельзя не упомянуть одноименный гликопротеин — аносмин-1 (ген ANOS1). Раньше этот ген называли KAL1 — по синдрому Кальмана. Это заболевание, при котором нарушается половое созревание и развивается аносмия. Какая между ними связь? Нейроны, которые будут секретировать гонадотропин-рилизинг-гормон в гипоталамусе, добираются туда из обонятельной плакоды (производное эктодермы, из которой образуется обонятельный эпителий носа). Недавно удалось выяснить, что аносмин-1 — критический участник ангиогенеза в обонятельной луковице. Но ANOS1 — это один из 25 страдающих при синдроме Кальмана генов [52].
В клубочке сигнал с аксонов передаётся на дендриты митральных и пучковых клеток. Они потом отправят информацию о запахе на пирамидные клетки обонятельной коры. Схема работы обонятельной луковицы значительно усложняется из-за тормозных влияний клеток (перигломерулярных, клеток-зерен) и возвратных проекций (рис. 11).
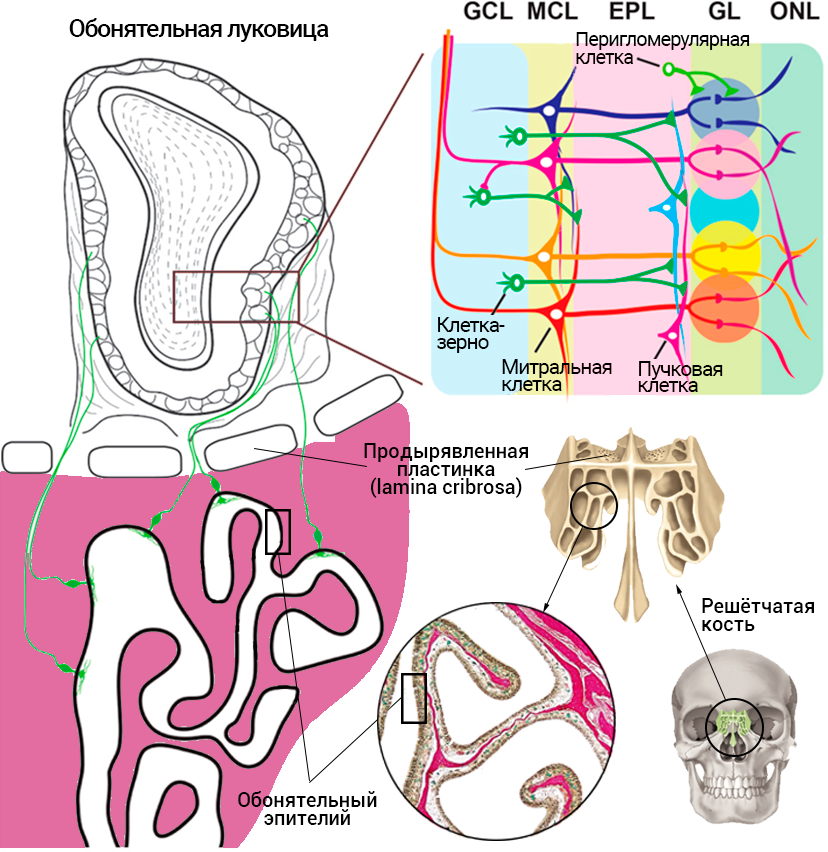
Рисунок 11. Относительное расположение решетчатой кости, обонятельного эпителия на гребнеобразных выростах решетчатой кости, носовые ходы/пазухи с выстилкой обонятельного эпителия (окраска по Ван-Гизону). Также на иллюстрации изображены аксоны обонятельных нейронов, поднимающиеся через продырявленную пластинку к обонятельной луковице. Сверху справа — схема нейронных связей в обонятельной луковице. На ней отмечены митральные и пучковые клетки — их дендриты идут из гломерул, а также изображены перигломерулярные и клетки-зерна, которые образуют синапсы с митральными и пучковыми клетками.
Кажется, что если строение луковицы принципиально не нарушено, то обонятельный сигнал хоть как-то пойдет по системе дальше? Но не в том случае, если необходимый возбуждающий глутамат не выделяется из аксонных терминалей обонятельных нейронов.
Анальгетик с побочным эффектом
В 2006 году в Nature публикуют статью, которая вызвала ажиотаж среди крупнейших игроков фарминдустрии [56]. Предыстория у исследования была не менее захватывающей — её героем стал уличный артист из Пакистана, который мог ходить по горящим углям. Выяснили, что в его семье распространена мутация в гене SCN9A, кодирующем натриевый канал Nav1.7, которая нарушает проведение ноцицептивных (болевых) сигналов. А позже оказалось, что вместе с потерей болевых ощущений (полной!) приходит и аносмия: этот канал необходим для выделения медиатора в синапсе обонятельных нейронов. Удивительно, что парой лет раньше узнали о мутации этого гена с усилением функции (gain-of-function) и противоположным эффектом — болевой сверхчувствительностью и предполагаемой гиперосмией!
ГЛАВА IV. Заключительная
К чему ведут запахи?
Неудивительно, что мифы о простоте и примитивности обонятельного анализатора ещё с прошлого века не выдерживали критики. Организация обонятельных нейронных сетей интересовала и нобелевского лауреата Эдгара Д. Эдриана. А Уилфрид Ралл и Гордон Шеперед, стоящие у истоков вычислительной нейробиологии, проводили свои пионерские работы на обонятельной луковице [57].
Обонятельная информация из луковицы проходит через различные перипетии, попадая в лимбическую систему, миндалину, орбитофронтальную кору. Пути усложняются ещё больше, если запахи проходят «ретроназально», т. е. обратным путём, как это происходит с напитками и едой. Хочется надеяться, что в будущем кто-то возьмет на себя смелость рассказать о том, что известно о нейронных сетях обоняния за последние полвека. Интересно ведь узнать, как кофе приобретает свой аромат и почему прустовские мадленки появляются в каждом втором тексте о запахах и вкусах? Про многие необычные обонятельные нарушения известно намного меньше, а это — фантосмия (обонятельные галлюцинации), какосмия (навязчивое ощущение неприятных запахов), паросмия (нарушение интерпретации запахов) и другие расстройства. (Кстати, вы правы, если подозревали, что слово «аносмия» связано с носом только по сути. В его основе греческий корень «osme» — запах и приставка «an»). Почему понять работу обоняния так непросто? Много чисто технических причин. Во-первых, когда только обнаружили гены, казалось, что скоро будет доступен весь список пар рецептор—лиганд. Оказалось, что рецепторы очень неохотно занимают место на мембранах в несвойственных им клетках (большинство нуждается в специальных белковых проводниках [58]. Во-вторых, по сравнению со зрительными экспериментами, контролировать подачу запахов куда сложнее. Вдобавок к этому, адаптация к запахам наступает очень быстро. Это явление привыкания, которое нам известно на бытовом уровне, и оно сильно ограничивает время экспериментов. И ещё одно: грантовые организации долгое время с недоверием смотрели на исследования обоняния, пренебрегая их значением. К сожалению, это гармонирует и со взглядами широкой публики. В одном из опросов 2011 года половина молодых людей ответила, что охотнее готовы расстаться с обонянием, чем с техникой (подробнее читайте в статье The Truth About Youth на странице 6). Полиморфные гены, постоянная перестройка сетей под новые запахи — всё ведет к одному результату: мы исключительно субъективно воспринимаем ароматы (представьте тысячи вариантов сине-черно-бело-золотого платья). Так ведь даже интереснее! Стоит понимать, что некоторые споры про вкус и запах разрешить в бытовых условиях не получится. И не нужно забывать, что среди нас живут те, кто не только оказывается лишен ежедневных аромаудовольствий, но и могут оказаться перед лицом серьезных заболеваний.
Стоит признать, многие важные вопросы остались за кадром. Почему работает васаби-будильник, заслуживший Игнобелевскую премию 2011 года? «Запахи» узнаёт не только обонятельный нерв, но также и тройничный! Аллилизотиоцианат васаби (это вещество есть и в горчице) связывается с ваниллоидными рецепторами соматосенсорных нейронов в обонятельной полости [58]. Благодаря тройничной иннервации мы определяем раздражающие, а также тёплые и холодные запахи. А про неосознаваемое влияние одорантов мы знаем ещё меньше.
На заре оцифровки
Монеллевский центр (США), который упоминался несколько раз, — один из ведущих центров по изучению химических чувств. Они стараются помогать аносмикам и развивают как фундаментальные, так и практические направления. А вот исследовательская группа института Вейцмана (Израиль) делает всё возможное, чтобы мы не только были с обонянием на «ты», но и научились управлять запахами. Например, в 2012 году они смогли создать «белый запах» — несколько неповторяющихся комбинаций из более 30 компонентов испытуемые определяли как одинаковый неидентифицируемый запах. Предлагали применять его для маскировки неприятных ароматов. Кажется, это пригодилось бы не только авиакомпаниям, периодически возвращающимся самолеты на проветривание. Ещё они научились «измерять запахи». Статья, недавно опубликованная в Nature, намекает на стремительное приближение пахнущих сообщений и фотографий (можно прочитать краткую выжимку из статьи от авторов). Из-за стволовых клеток обонятельную систему любят разбирать на запасные части [59]. Ещё её эксплуатируют как модельный объект. Но, к счастью, есть и желающие помочь людям, лишившимся обоняния или никогда не знавших о запахах. А для всех тех, кто не верит в роль запахов, Рэндалл Рид, один из ведущих нейробиологи обоняния, напоминает: пить кофе с крышкой на стакане почти как вино через соломинку — затея сомнительная, ведь упускаются ценные ароматы. Если загадки обоняния вас несколько заинтересовали, то можно обратиться к недавно переведённой книге профессора Паоло Пелоси, одного из последователей Джона Эймура: «Обоняние. Увлекательное погружение в науку о запахах» [60]. Среди детективных историй от первого лица и живых научно-насыщенных описаний механизмов обоняния разных видов есть вопросы, которые достойны особого внимания: поводы вернуться к обонянию представятся ещё не раз.
За помощь в подготовке иллюстраций автор выражает благодарность Глебу С. Русину.Литература
- Jessica Freiherr, Amy R. Gordon, Eva C. Alden, Andrea L. Ponting, Monica F. Hernandez, et. al.. (2012). The 40-item Monell Extended Sniffin’ Sticks Identification Test (MONEX-40). Journal of Neuroscience Methods. 205, 10-16;
- N. Aguilar Martínez, G. Aguado Carrillo, P.E. Saucedo Alvarado, C.A. Mendoza García, A.L. Velasco Monroy, F. Velasco Campos. (2018). Clinical importance of olfactory function in neurodegenerative diseases. Revista Médica del Hospital General de México. 81, 268-275;
- Loïc Briand, Corinne Eloit, Claude Nespoulous, Valérie Bézirard, Jean-Claude Huet, et. al.. (2002). Evidence of an Odorant-Binding Protein in the Human Olfactory Mucus: Location, Structural Characterization, and Odorant-Binding Properties†. Biochemistry. 41, 7241-7252;
- Guangfa Wang, Yushu Li, Zhenzhen Cai, Xincun Dou. (2020). A Colorimetric Artificial Olfactory System for Airborne Improvised Explosive Identification. Adv. Mater.. 32, 1907043;
- Giorgia Sollai, Melania Melis, Salvatore Magri, Paolo Usai, Thomas Hummel, et. al.. (2019). Association between the rs2590498 polymorphism of Odorant Binding Protein (OBPIIa) gene and olfactory performance in healthy subjects. Behavioural Brain Research. 372, 112030;
- Masashi Asakawa, Yosuke Fukutani, Aulaphan Savangsuksa, Keiich Noguchi, Hiroaki Matsunami, Masafumi Yohda. (2017). Modification of the response of olfactory receptors to acetophenone by CYP1a2. Sci Rep. 7;
- Jean-Marie Heydel, Alexandra Coelho, Nicolas Thiebaud, Arièle Legendre, Anne-Marie Le Bon, et. al.. (2013). Odorant-Binding Proteins and Xenobiotic Metabolizing Enzymes: Implications in Olfactory Perireceptor Events. Anat. Rec.. 296, 1333-1345;
- 12 методов в картинках: протеомика;
- Adrien François, Denise Grebert, Moez Rhimi, Mahendra Mariadassou, Laurent Naudon, et. al.. (2016). Olfactory epithelium changes in germfree mice. Sci Rep. 6;
- Kristi Biswas, Brett Wagner Mackenzie, Charlotte Ballauf, Julia Draf, Richard G. Douglas, Thomas Hummel. (2020). Loss of bacterial diversity in the sinuses is associated with lower smell discrimination scores. Sci Rep. 10;
- Kaisa Koskinen, Johanna L. Reichert, Stefan Hoier, Jochen Schachenreiter, Stefanie Duller, et. al.. (2018). The nasal microbiome mirrors and potentially shapes olfactory function. Sci Rep. 8;
- Alison Abbott. (2020). Are infections seeding some cases of Alzheimer’s disease?. Nature. 587, 22-25;
- Andreas Natsch, Roger Emter. (2020). The specific biochemistry of human axilla odour formation viewed in an evolutionary context. Phil. Trans. R. Soc. B. 375, 20190269;
- Jan Havlíček, Jamie Winternitz, S. Craig Roberts. (2020). Major histocompatibility complex-associated odour preferences and human mate choice: near and far horizons. Phil. Trans. R. Soc. B. 375, 20190260;
- Нос и язык, которым нужны батарейки;
- P. Pelosi. (2001). The role of perireceptor events in vertebrate olfaction. CMLS, Cell. Mol. Life Sci.. 58, 503-509;
- Federica Genovese, Marco Tizzano. (2018). Microvillous cells in the olfactory epithelium express elements of the solitary chemosensory cell transduction signaling cascade. PLoS ONE. 13, e0202754;
- David H. Brann, Tatsuya Tsukahara, Caleb Weinreb, Marcela Lipovsek, Koen Van den Berge, et. al.. (2020). Non-neuronal expression of SARS-CoV-2 entry genes in the olfactory system suggests mechanisms underlying COVID-19-associated anosmia. Sci.Adv.. 6, eabc5801;
- Leon Fodoulian, Joël Tuberosa, Daniel Rossier, Madlaina Boillat, Chenda Kan, et. al.. (2020). SARS-CoV-2 Receptors and Entry Genes Are Expressed in the Human Olfactory Neuroepithelium and Brain. iScience. 23, 101839;
- Sandra Pfister, Tamara Weber, Wolfgang Härtig, Cornelia Schwerdel, Rebecca Elsaesser, et. al.. (2015). Novel role of cystic fibrosis transmembrane conductance regulator in maintaining adult mouse olfactory neuronal homeostasis. J. Comp. Neurol.. 523, 406-430;
- Pfister S. Orchestrates Multiple Signaling Cascades in Microvillar Cells to Regulate Olfactory Epithelial Homeostasis. Zürich, 2014;
- Keith G. Kozminski. (2012). Intraflagellar transport—the “new motility” 20 years later. MBoC. 23, 751-753;
- Joel L. Rosenbaum, George B. Witman. (2002). Intraflagellar transport. Nat Rev Mol Cell Biol. 3, 813-825;
- Jeremy F. Reiter, Michel R. Leroux. (2017). Genes and molecular pathways underpinning ciliopathies. Nat Rev Mol Cell Biol. 18, 533-547;
- Heather M Kulaga, Carmen C Leitch, Erica R Eichers, Jose L Badano, Alysa Lesemann, et. al.. (2004). Loss of BBS proteins causes anosmia in humans and defects in olfactory cilia structure and function in the mouse. Nat Genet. 36, 994-998;
- Nathalie Falk, Marlene Lösl, Nadja Schröder, Andreas Gießl. (2015). Specialized Cilia in Mammalian Sensory Systems. Cells. 4, 500-519;
- Warren W. Green, Cedric R. Uytingco, Kirill Ukhanov, Zachary Kolb, Jordan Moretta, et. al.. (2018). Peripheral Gene Therapeutic Rescue of an Olfactory Ciliopathy Restores Sensory Input, Axonal Pathfinding, and Odor-Guided Behavior. J. Neurosci.. 38, 7462-7475;
- D. P. McEwen, R. K. Koenekoop, H. Khanna, P. M. Jenkins, I. Lopez, et. al.. (2007). Hypomorphic CEP290/NPHP6 mutations result in anosmia caused by the selective loss of G proteins in cilia of olfactory sensory neurons. Proceedings of the National Academy of Sciences. 104, 15917-15922;
- Heidi Ledford. (2020). CRISPR treatment inserted directly into the body for first time. Nature. 579, 185-185;
- Johannes Reisert, Jürgen Reingruber. (2019). Ca2+-activated Cl− current ensures robust and reliable signal amplification in vertebrate olfactory receptor neurons. Proc Natl Acad Sci USA. 116, 1053-1058;
- Katarina Tengvall, Jesse Huang, Cecilia Hellström, Patrick Kammer, Martin Biström, et. al.. (2019). Molecular mimicry between Anoctamin 2 and Epstein-Barr virus nuclear antigen 1 associates with multiple sclerosis risk. Proc Natl Acad Sci USA. 116, 16955-16960;
- D. Jones, R. Reed. (1989). Golf: an olfactory neuron specific-G protein involved in odorant signal transduction. Science. 244, 790-795;
- B. Schaal. (2000). Human Foetuses Learn Odours from their Pregnant Mother's Diet. Chemical Senses. 25, 729-737;
- Ximena Ibarra-Soria, Thiago S Nakahara, Jingtao Lilue, Yue Jiang, Casey Trimmer, et. al.. (2017). Variation in olfactory neuron repertoires is genetically controlled and environmentally modulated. eLife. 6;
- Emily J. Mayhew, Charles J. Arayata, Richard C. Gerkin, Brian K. Lee, Jonathan M. Magill, et. al. Drawing the Borders of Olfactory Space — Cold Spring Harbor Laboratory;
- C. Bushdid, M. O. Magnasco, L. B. Vosshall, A. Keller. (2014). Humans Can Discriminate More than 1 Trillion Olfactory Stimuli. Science. 343, 1370-1372;
- Richard C Gerkin, Jason B Castro. (2015). The number of olfactory stimuli that humans can discriminate is still unknown. eLife. 4;
- J. E. AMOORE. (1967). Specific Anosmia: a Clue to the Olfactory Code. Nature. 214, 1095-1098;
- I. Croy, S. Olgun, L. Mueller, A. Schmidt, M. Muench, et. al.. (2016). Spezifische Anosmie als Prinzip olfaktorischer Wahrnehmung. HNO. 64, 292-295;
- John E. Amoore, Delpha Venstrom, Alfred R. Davis. (1968). Measurement of Specific Anosmia. Percept Mot Skills. 26, 143-164;
- Загадка мужественного запаха;
- Nicholas Eriksson, Shirley Wu, Chuong B Do, Amy K Kiefer, Joyce Y Tung, et. al.. (2012). A genetic variant near olfactory receptor genes influences cilantro preference. Flavour. 1;
- Rosa S. Gisladottir, Erna V. Ivarsdottir, Agnar Helgason, Lina Jonsson, Nanna K. Hannesdottir, et. al.. (2020). Sequence Variants in TAAR5 and Other Loci Affect Human Odor Perception and Naming. Current Biology. 30, 4643-4653.e3;
- Stefano Espinoza, Ilya Sukhanov, Evgeniya V. Efimova, Alena Kozlova, Kristina A. Antonova, et. al.. (2020). Trace Amine-Associated Receptor 5 Provides Olfactory Input Into Limbic Brain Areas and Modulates Emotional Behaviors and Serotonin Transmission. Front. Mol. Neurosci.. 13;
- M. Spehr. (2003). Identification of a Testicular Odorant Receptor Mediating Human Sperm Chemotaxis. Science. 299, 2054-2058;
- Lisa Stowers, Darren W Logan. (2010). Sexual dimorphism in olfactory signaling. Current Opinion in Neurobiology. 20, 770-775;
- C. Sinding, E. Kemper, P. Spornraft-Ragaller, T. Hummel. (2013). Decreased Perception of Bourgeonal May Be Linked to Male Idiopathic Infertility. Chemical Senses. 38, 439-445;
- Désirée Maßberg, Hanns Hatt. (2018). Human Olfactory Receptors: Novel Cellular Functions Outside of the Nose. Physiological Reviews. 98, 1739-1763;
- Sung-Joon Lee, Inge Depoortere, Hanns Hatt. (2019). Therapeutic potential of ectopic olfactory and taste receptors. Nat Rev Drug Discov. 18, 116-138;
- Tsviya Olender, Doron Lancet, Daniel W Nebert. (2008). Update on the olfactory receptor (OR) gene superfamily. Human Genomics. 3, 87;
- Suhn K. Rhie, Shannon Schreiner, Heather Witt, Chris Armoskus, Fides D. Lay, et. al.. (2018). Using 3D epigenomic maps of primary olfactory neuronal cells from living individuals to understand gene regulation. Sci. Adv.. 4, eaav8550;
- Shoko Matsushima, Akio Shimizu, Manami Kondo, Hirotsugu Asano, Nobuhiro Ueno, et. al.. (2020). Anosmin-1 activates vascular endothelial growth factor receptor and its related signaling pathway for olfactory bulb angiogenesis. Sci Rep. 10;
- Kevin Monahan, Adan Horta, Stavros Lomvardas. (2019). LHX2- and LDB1-mediated trans interactions regulate olfactory receptor choice. Nature. 565, 448-453;
- Новый взгляд на геном: не просто цепочка генов, а трехмерная сеть, интегрирующая функциональные домены ядра;
- Longzhi Tan. (2019). Three-dimensional genome structure of a single cell. Science. 366, 964-965;
- Katie Kingwell. (2019). Nav1.7 withholds its pain potential. Nat Rev Drug Discov;
- James J. Cox, Frank Reimann, Adeline K. Nicholas, Gemma Thornton, Emma Roberts, et. al.. (2006). An SCN9A channelopathy causes congenital inability to experience pain. Nature. 444, 894-898;
- Gordon M. Shepherd. (2018). Wilfrid Rall. Neuroinform. 16, 151-152;
- Geoffrey Raisman, Ying Li. (2007). Repair of neural pathways by olfactory ensheathing cells. Nat Rev Neurosci. 8, 312-319;
- Пелоси П. Обоняние. Увлекательное погружение в науку о запахах. КоЛибри, 2020. — 304 c.;
- Wilson-Pauwels L., Stewart P., Akesson E.J., Spacey S.D. Cranial Nerves: Function and Dysfunction. People’s Medical Publishing House, 2010. 3rd Edition;
- Christopher H. Ferguson, Haiqing Zhao. (2016). Cyclic AMP Signaling in the Main Olfactory Epithelium. Chemosensory Transduction. 123-140;
- Purves D., Augustine G.J., Fitzpatrick D., Hall W., LaMantia A.-S. Neuroscience. Sunderland, Massachusetts. : Sinauer Associates, Inc., 2012. 5th Edition;
- Elissa A. Hallem, A. Nicole Fox, Laurence J. Zwiebel, John R. Carlson. (2004). Mosquito receptor for human-sweat odorant. Nature. 427, 212-213;
- Shannon DeMaria, John Ngai. (2010). The cell biology of smell. Journal of Cell Biology. 191, 443-452;
- Longzhi Tan, Dong Xing, Nicholas Daley, X. Sunney Xie. (2019). Three-dimensional genome structures of single sensory neurons in mouse visual and olfactory systems. Nat Struct Mol Biol. 26, 297-307;
- K. Miyamichi. (2005). Continuous and Overlapping Expression Domains of Odorant Receptor Genes in the Olfactory Epithelium Determine the Dorsal/Ventral Positioning of Glomeruli in the Olfactory Bulb. Journal of Neuroscience. 25, 3586-3592;
- Fumiaki Imamura, Sanae Hasegawa-Ishii. (2016). Environmental Toxicants-Induced Immune Responses in the Olfactory Mucosa. Front. Immunol.. 7.