
Не дружите, дети, с гепатитом B
27 апреля 2020
Не дружите, дети, с гепатитом B
- 8782
- 0
- 4
Гепатит В часто приводит к циррозу и раку печени, и дальнейшая жизнь человека может висеть на волоске в ожидании пересадки здорового органа
иллюстрация Ирины Ефремовой
-
Автор
-
Редакторы
-
Иллюстратор
Гепатит В — чрезвычайно опасное заболевание, которое чревато последствиями на всю жизнь. Однако с появлением вакцинации болезнь встречается всё реже. В этой статье спецпроекта «Вакцинация» мы напомним, почему так важно соблюдать плановую вакцинацию против гепатита В, особенно если речь идет о детях.
Вакцинация

Генеральный партнер спецпроекта — Zimin Foundation.
Изобретение вакцин кардинально изменило жизнь человечества. Многие болезни, уносившие тысячи, а то и миллионы жизней ежегодно, теперь практически не встречаются. В этом спецпроекте мы не только рассказываем об истории возникновения вакцин, общих принципах их разработки и роли вакцинопрофилактики в современном здравоохранении (этому посвящены первые три статьи), но и подробно говорим о каждой вакцине, включенной в Национальный календарь прививок, а также вакцинах против гриппа и вируса папилломы человека. Вы узнаете о том, что собой представляет каждый из возбудителей болезней, какие существуют варианты вакцин и чем они различаются между собой, затронем тему поствакцинальных осложнений и эффективности вакцин.
Для соблюдения объективности мы пригласили стать кураторами спецпроекта Александра Соломоновича Апта — доктора биологических наук, профессора МГУ, заведующего лабораторией иммуногенетики Института туберкулеза (Москва), — Сусанну Михайловну Харит — доктора медицинских наук, профессора, руководителя отдела профилактики НИИ детских инфекций (Санкт-Петербург), — а также Сергея Александровича Бутрия — педиатра, автора блога «Заметки детского врача».
Печень — самый крупный орган тела человека, занимающий центральное место в нашем метаболизме. Она выполняет множество функций, участвуя в обмене белков, углеводов, жиров, гормонов и витаминов, а также в обезвреживании многих веществ, попадающих в наш организм или образующихся в нем [1]. Все заболевания, связанные с воспалением печени, называют гепатитами, хотя причины, которые их вызывают, могут быть разными: инфекции, проблемы с обменом веществ, аутоиммунные заболевания и другие. Среди них Всемирная организация здравоохранения (ВОЗ) отдельно выделяет вирусный гепатит В — бич современного человечества .
О других вирусных гепатитах читайте в наших статьях «Вирус гепатита А: новое – это хорошо забытое старое» [2], «Гепатит C: решенная проблема?» [3] и «Гепатит Е – безобидное заболевание или скрытая угроза?» [4]. — Ред.
Ежегодно из-за вирусных гепатитов умирает 1,4 млн людей — это больше, чем от СПИДа, туберкулеза или малярии [5], [6], и около половины этих смертей происходит из-за осложнений, связанных с хроническим носительством вируса гепатита В [7]. По данным на 2015 год, примерно 350 млн. людей по всей планете болели хроническим гепатитом В [8], и со временем примерно у 20–30% из них разовьются осложнения в виде цирроза и рака печени [9].
Вирус гепатита В попадает в организм при контакте с кровью, половым путем или передается от больной матери (внутриутробно или во время родов) [10], [11]. Треть больных хроническим гепатитом В заразились вирусом при рождении или в раннем детстве [9], поэтому только вакцинация в первые часы жизни может гарантировать младенцам долгую и здоровую жизнь.
Кроме того, вирус устойчив во внешней среде и может сохраняться вне человеческого тела в течение семи дней [12], из-за чего много случаев заражения происходит при повторном использовании медицинских игл, шприцев и других инструментов, которые контактировали с кровью, но не прошли должную обработку. Так, например, подхватить инфекцию можно во время нанесения татуировок [11], маникюра или на приеме у стоматолога. Однако это не представляет серьезной угрозы для людей, у которых уже сформирован защитный иммунитет в результате вакцинации.
История двух гепатитов
Первые упоминания о желтушном окрашивании кожи и видимых слизистых оболочек (желтухе), которое является одним из основных симптомов гепатита В, были найдены еще на вавилонских глиняных табличках и в записях Гиппократа [13]. На протяжении многих веков описывались вспышки желтухи среди городского населения и в военных подразделениях. Но изучение этого заболевания и его источника началось лишь около 150 лет назад, в конце XIX века, а новые вспышки шли рука об руку с достижениями медицины: разработкой методик инъекций препаратов, вакцинацией и переливанием крови. На рисунке 1 приведены основные вехи развития представлений о гепатите В.

Рисунок 1. История гепатита В: от первого упоминания болезни до разработки первой вакцины. XIX–V века до н. э. Первые упоминания о желтухе, найденные на вавилонских глиняных табличках и в записях Гиппократа. VII–XX века. Вспышки желтухи среди городского населения и в военных подразделениях. 1885–1942 годы. Установлена связь между вспышками желтухи и вакцинациями от оспы и желтой лихорадки, профилактикой кори и паротита при помощи иммунной сыворотки и другими медицинскими вмешательствами. 1944–1950-е годы. Изучение вирусного гепатита на «добровольцах» (см. врезку). 1965–1967 годы. Открытие австралийского антигена и его связи с гепатитом В. 1969–1972 годы. Обнаружение связи между хроническим гепатитом В и развитием рака печени. 1972 год. Первая вакцина, защищающая от гепатита В [13].
иллюстрация Ирины Ефремовой
После наблюдений за периодом инкубации, течением болезни и способом передачи инфекции, исследователи пришли к выводу, что они имеют дело с двумя разными вирусами. Заболевания, которые эти вирусы вызывали, были названы «инфекционным» и «сывороточным» гепатитами [13], [15]. Первый имел небольшой период инкубации (20–40 дней) и передавался орально-фекальным путем: вирусом можно было заразиться из общих источников еды и воды. «Сывороточный» гепатит имел более долгий период инкубации (60–120 дней) и, как правило, передавался через кровь и ее производные (плазму, сыворотку и др.).

Рисунок 3. Барух (Барри) Бламберг в экспедиции 1958 года на Аляске, где он собирал образцы крови у изолированной группы инуитов — этнической группы коренных народов Северной Америки.
За длительный период изучения появились различные синонимы для этих заболеваний, и, чтобы избежать дальнейшей путаницы, в 1947 году английский врач Фредерик Маккаллум (Frederick Maccallum) предложил называть «инфекционный гепатит», «эпидемическую желтуху» и «острую катаральную желтуху» гепатитом А, а «сывороточный гепатит», «гепатит с длительным периодом инкубации» и «посттрансфузионный гепатит» — гепатитом В [13], [15].
Поскольку нарушения в работе печени приводят ко многим физиологическим изменениям, помимо внешней клинической картины для диагностики этих видов гепатита начали использовать результаты биопсии и различных функциональных тестов. Это позволило диагностировать случаи безжелтушного гепатита, а также обнаружить хроническую форму [13].
Большим прорывом в дальнейшем изучении вируса гепатита В, диагностике и мониторинге заболевания было открытие австралийского антигена (Au) генетиком Барухом Бламбергом (рис. 3), получившим за это в 1976 году Нобелевскую премию по физиологии или медицине (см. врезку).
Нелегкая жизнь вируса
Вирус гепатита В принадлежит к семейству гепаднавирусов (Hepadnaviridae) и является одним из самых маленьких окруженных липидной оболочкой вирусов животных. Диаметр полноценной вирусной частицы (частицы Дейна) — всего 42 нм, но во время инфекции в организме больного также образуется большое количество неинфекционных частиц диаметром 20 нм (сферических или нитевидных разной длины), которые состоят только из липидной оболочки и поверхностного белка и не имеют внутри генетического материала (рис. 4) [22].
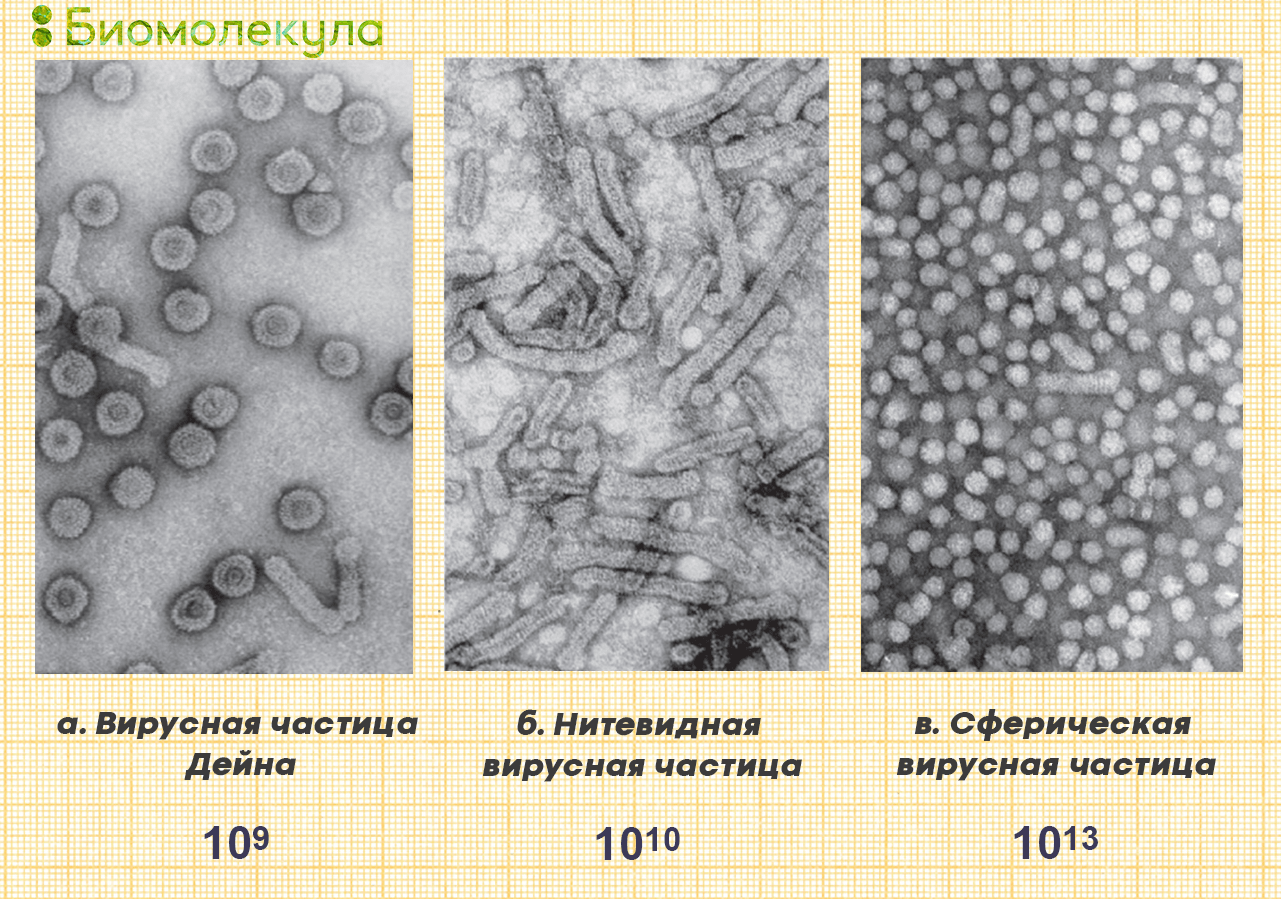
Рисунок 4. Изображение вирусных частиц, полученное методом электронной микроскопии (негативное окрашивание), и приблизительное количество частиц в 1 мл сыворотки хронического больного гепатитом В в период активного размножения вируса.
[22], рисунок адаптирован
Белок на поверхности вируса и неинфекционных частиц называют HBsAg (от англ. Hepatitis B surface Antigen — поверхностный антиген гепатита В). Это тот самый австралийский антиген, полвека назад обнаруженный в сыворотке крови австралийского аборигена. В полноценных вирусных частицах под липидной оболочкой скрыт икосаэдрический белковый капсид, хранящий в себе геном вируса — частично незамкнутую кольцевую двухцепочечную ДНК, с которой связана вирусная полимераза (рис. 5).
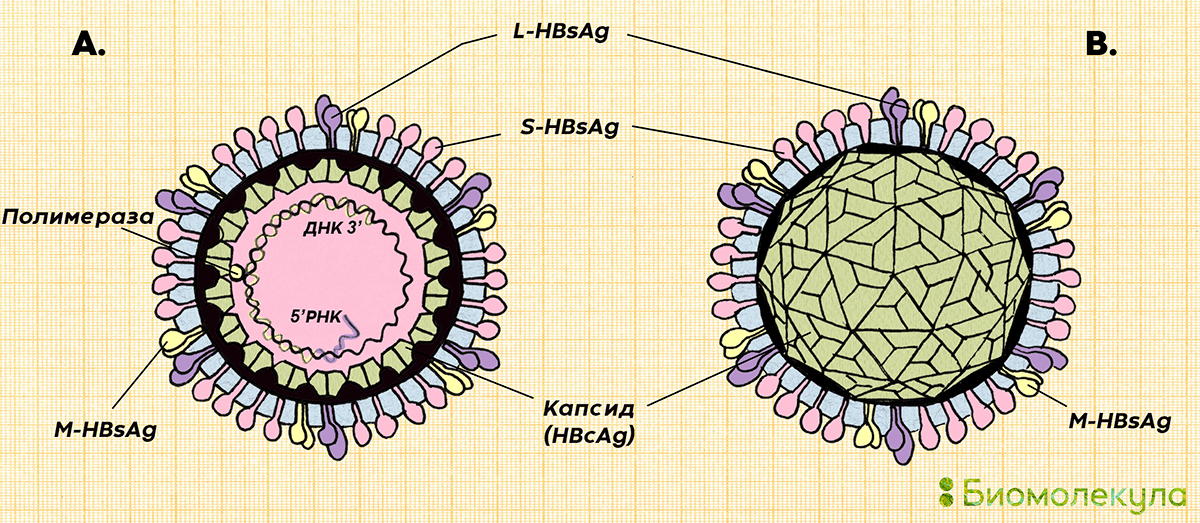
Рисунок 5. Строение вирусной частицы вируса гепатита В. Геном вируса имеет длину примерно 3,2 тыс. нуклеотидов и кодирует 7 белков: три варианта поверхностного антигена HBsAg (large, medium, small), белок капсида (HBcAg, Hepatitis B core Antigen), полимеразу и еще два белка, которые играют важную роль в модулировании иммунного ответа, — HBeAg и HBx. Из-за особенностей жизненного цикла вируса гепатита В полимераза не успевает завершить синтез второй цепочки кольцевой ДНК и разрушить остаток пре-геномной РНК, который остается в зрелой частице.
иллюстрация Ирины Ефремовой по Hepadnaviridae
Вирус гепатита В заражает преимущественно клетки печени, потому что на их поверхности находится особый полипептид — натрий-таурохолевый котранспортер (sodium-taurocholate cotransporting polypeptide, NTCP). С ним связывается самый большой поверхностный белок вируса — L-HBsAg, — в результате чего вирус попадает внутрь, попутно освобождаясь от собственной липидной оболочки, и перемещается к ядру. Здесь из него высвобождается геномная ДНК и вирусная полимераза, которая достраивает геном до полноценной замкнутой кольцевой ДНК (covalently closed circular DNA, cccDNA). Затем привлекается хозяйская РНК-полимераза II, синтезирующая РНК для последующего производства белков и геномной ДНК вируса.
Все вирусные белки синтезируются в цитоплазме, там же начинается сборка новых вирусных частиц. Для этого вместе собираются белки капсида, вирусная полимераза и пре-геномная РНК (pgRNA). Синтез новой геномной ДНК на основе РНК происходит уже внутри капсида, однако он не успевает завершиться до полной сборки вирусной частицы, поэтому в зрелом вирусе оказывается лишь частично двухцепочечная молекула.
Упакованный в белковую оболочку вирус может либо снова отправиться в ядро для нового цикла синтеза матричной РНК, белков и репликации, либо одеться в липидную оболочку, содержащую все три варианта поверхностного белка, и покинуть клетку. При этом в ходе размножения вируса образуется много побочных продуктов: пустые липидные оболочки, о которых мы уже говорили выше, а также дефектная линейная двухцепочечная ДНК, которая затем может быть встроена в геном клетки-хозяина (рис. 6) [23].
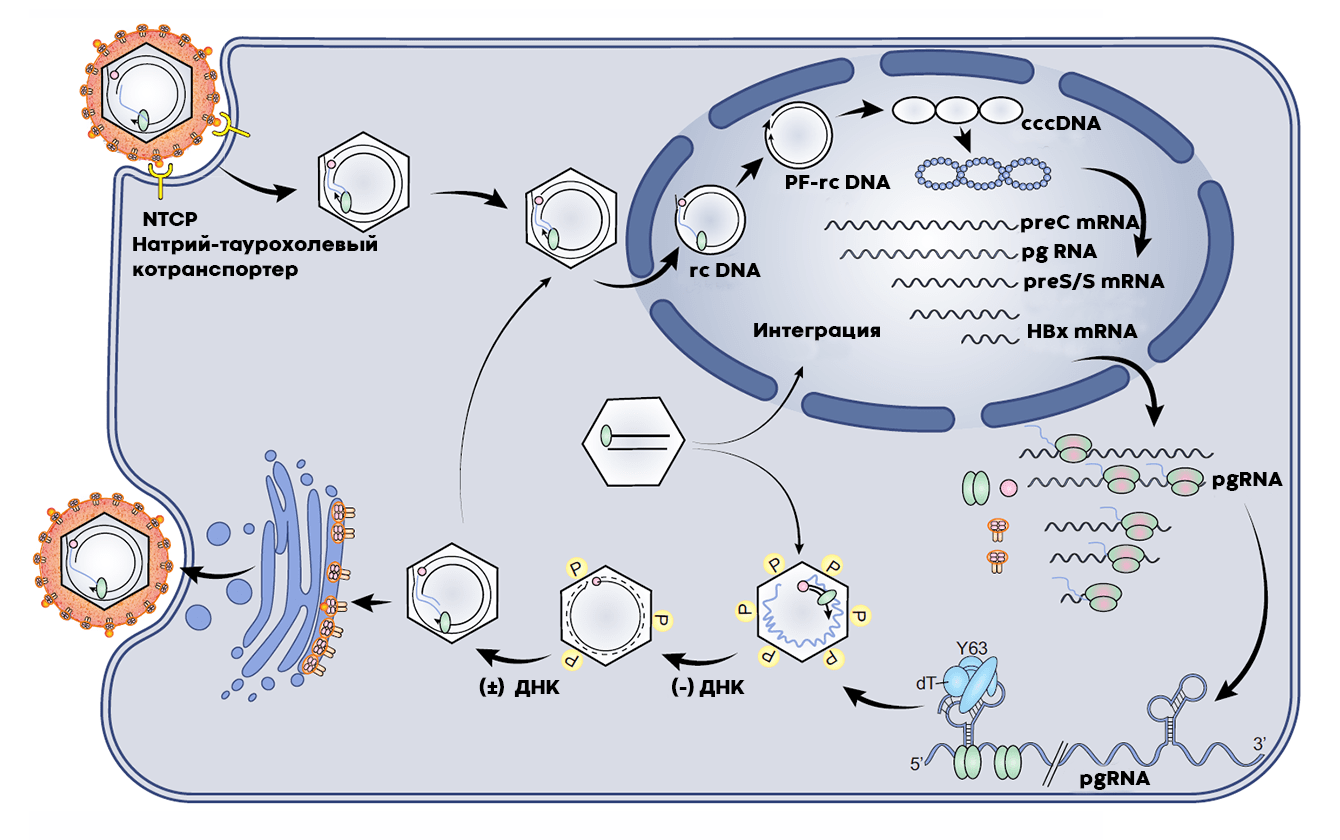
Рисунок 6. Жизненный цикл вируса гепатита В. Как и вирус иммунодефицита человека, вирус гепатита В имеет стадию обратной транскрипции, однако его геном представлен ДНК (а не РНК, как у ВИЧ). В связи с этим в классификации по Балтимору вирус гепатита В относят к отдельной группе — параретровирусам.
[23], рисунок адаптирован
Клинические проявления вирусного гепатита возникают в результате сложных отношений между вирусом гепатита В и нашей иммунной системой [24]. Сам по себе вирус не убивает клетку, и за все повреждения, наносимые печени, ответственен собственный иммунитет человека. Его основная боевая мощь представлена цитотоксическими Т-лимфоцитами, или Т-киллерами, которые убивают зараженную вирусом клетку [25]. На фоне воспаления также активируются разные типы иммунных клеток, находящиеся поблизости, и по всему организму распространяется сигнал бедствия, который привлекает другие клетки неспецифического иммунитета. Все вместе это еще больше усугубляет ситуацию в тканях печени [26], а за ее пределами может привести к развитию не связанных с печенью заболеваний — чаще всего это гломерулонефрит (поражение фильтрующих клубочков почек) и васкулит (воспаление сосудов) [24].
Какой гепатит пожелаете?
Хроническая форма гепатита В — самое опасное состояние, поскольку на его фоне часто развиваются серьезные осложнения с последующим смертельным исходом. Но хронический гепатит не возникает на пустом месте: после того, как вирус попадает в организм и заражает первые клетки, начинается острая стадия заболевания.
Острый гепатит
Как мы уже говорили, вирусом гепатита В можно заразиться при контакте с инфицированной кровью (в том числе через медицинское оборудование), половым путем или от больной матери (внутриутробно или во время родов) [10], [11]. После проникновения вируса в организм начинается острая инфекция, хотя у некоторых людей она может протекать без каких-либо симптомов (такое чаще случается у детей и младенцев). Примерно у 70% взрослых развивается субклинический (или безжелтушный) гепатит, и только у 30% — с проявлением желтухи. В некоторых случаях возникает острая печеночная недостаточность, из-за которой человек может умереть [24]. В таблице 1 приведена заболеваемость гепатитом В в России.
| Заболевание | Число в 2018 г. | Число в 2017 г. | Динамика | ||
|---|---|---|---|---|---|
| всего | показатель на 100 тыс. населения | всего | показатель на 100 тыс. населения | всего | |
| Острый гепатит В | 993 | 0,68 | 1271 | 0,87 | −22,0 % |
| Хронический гепатит В | 13615 | 9,28 | 14073 | 9,61 | −3,4 % |
| Носительство гепатита В | 12877 | 8,78 | 14859 | 10,15 | −13,5 % |
Врачи выделяют четыре стадии острого гепатита [10]:
- Инкубационный период — от 1,5 месяцев до полугода (в среднем 2–4 месяца), в который болезнь никак себя не проявляет.
- Преджелтушный период — от 1 до 4 недель (в среднем 10–14 дней). Он начинается с общего плохого самочувствия, потери аппетита, тошноты и рвоты. Воспаление печени дает о себе знать в виде тупых болей в правом боку и легкой лихорадки. Дополнительно к этому может потемнеть моча и появиться сыпь.
- Желтушный период — от 1 недели до 2–3 месяцев и более. В этот период появляется характерная для гепатита желтушная окраска тела (рис. 8). Изменение цвета начинается со склер, затем — на коже лица, туловища, слизистых, позднее — на коже конечностей. Через 5–10 дней все исчезает в обратном порядке, но на этой стадии все еще сохраняется темный цвет мочи. Очень важно, что эти симптомы ничем не отличаются от гепатита А, поэтому необходимо проведение лабораторных тестов, чтобы правильно идентифицировать заболевание.
- Период выздоровления — от 1 до 3 месяцев, в течение которых основные биохимические показатели постепенно приходят в норму.
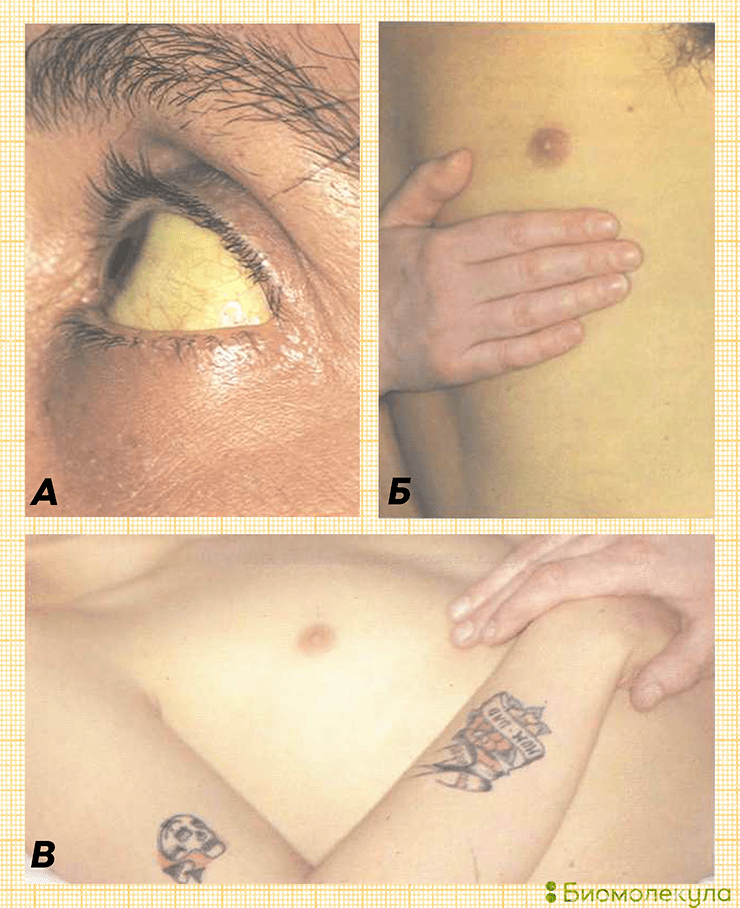
Рисунок 8. Пожелтение склер и кожи во время гепатита В. В результате разрушения тканей печени в кровоток высвобождается билирубин — продукт распада гемоглобина, обладающий особым сродством к эластическим волокнам. Именно поэтому структуры с высоким их содержанием (кожа, склеры, сосуды) легко приобретают желтушную окраску, которая сохраняется даже после того, как уровень билирубина в сыворотке нормализуется. На рисунке А приведен пример желтушности склер, на рисунках Б и В хорошо виден контраст между желтушным цветом кожи больного и нормальным цветом кожи руки здорового человека.
[11], рисунок адаптирован
Хронический гепатит
Если спустя шесть и более месяцев после перенесенного заболевания в крови все еще можно обнаружить поверхностный антиген HBsAg, то считается, что инфекция перешла в хроническую форму [9]. Это часто случается после бессимптомного течения болезни [10]. Хронический гепатит — серьезное заболевание, поскольку при нем сильно увеличивается вероятность развития цирроза и рака печени.
Бывают разные состояния хронического гепатита В, которые во многом зависят от того, как наша иммунная система реагирует на вирус [9]. Самое благоприятное из них — неактивный хронический гепатит, при котором иммунные клетки контролируют уровень размножения вируса, и нет никаких признаков заболевания, а у больного есть вероятность полного выздоровления. При другом сценарии развития событий иммунная система не уничтожает полностью вирус, но при этом и не оказывает активного давления на клетки печени. Такое состояние характеризуется слабо выраженным воспалением и незначительным проявлением симптомов. Его чаще всего можно встретить у HBsAg-позитивных детей и молодых взрослых, инфицированных в детстве. Куда опаснее, если иммунитет вновь начинает вести себя агрессивно, при этом клиническая картина становится аналогична острому гепатиту. Такое проявление нередко вызвано реактивацией вируса. На поздней стадии заболевания чаще всего встречается последний вариант течения хронического гепатита В, когда в вирусном геноме накапливаются мутации, которые превращают вирус в новый с точки зрения иммунитета патоген. Это провоцирует запуск иммунного ответа, активное воспаление и более быструю прогрессию цирроза печени.
Самые уязвимые
Главная угроза гепатита В — высокий уровень смертности от цирроза и рака печени, которые развиваются на фоне хронического течения болезни. Оказалось, что ключевой фактор перехода заболевания в хроническую форму — это возраст: чем человек младше, тем эта вероятность выше (рис. 9) [9]. Вирус гепатита В имеет много различных механизмов для подавления иммунной системы [28], которая к тому же еще не в полной мере сформирована у младенцев. По данным ВОЗ, хронический гепатит развивается у 90% новорожденных детей, зараженных от больной матери, 20–60% детей, зараженных в возрасте до 5 лет, и <20% взрослых.
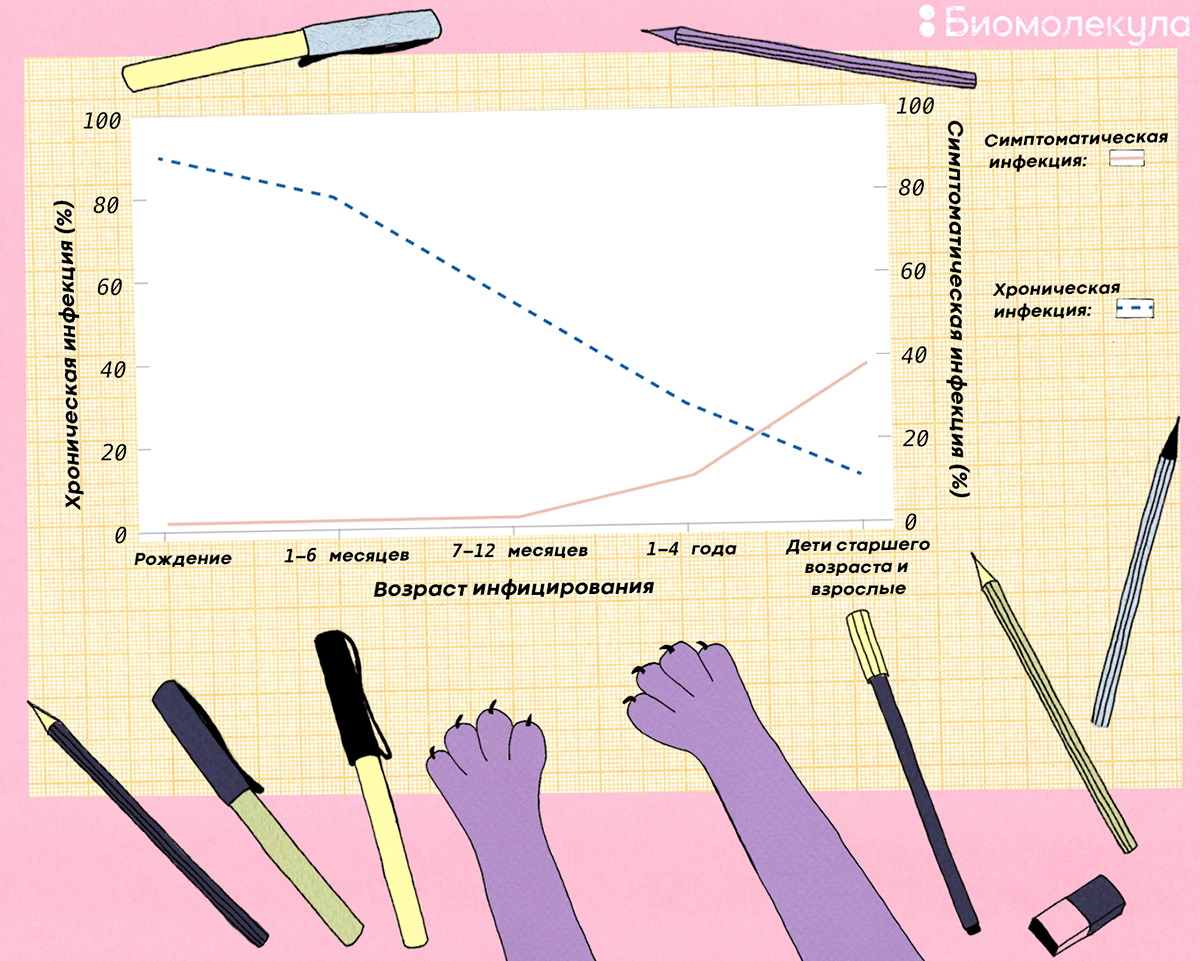
Рисунок 9. Вероятность самостоятельно выздороветь после заражения (симптоматическая инфекция, сплошная линия) или приобрести хронический гепатит В (хроническая инфекция, пунктирная линия) у людей разного возраста
иллюстрация Ирины Ефремовой по [9]
Если гепатит В перешел в хроническую форму, дальнейший прогноз неутешителен: в течение следующих пяти лет с вероятностью 8–20% может развиться цирроз печени, который затем с вероятностью в 20% приведет к полному отказу работы органа. Кроме того, каждый год в 1–5% случаев на фоне цирроза может развиться рак печени [9]. Полное уничтожение вируса на стадии хронического гепатита случается крайне редко, поэтому каждого больного ждет регулярный мониторинг состояния, противовирусная терапия, применение иммуномодуляторов в течение всей жизни и, возможно, даже пересадка печени.
Вакцинация от гепатита В
Предыстория
Возможность создания вакцины против гепатита В впервые показал Сол Кругман еще в 1971 году, введя «добровольцам» из школы Уиллоубрук разведенную в 10 раз и предварительно прокипяченную сыворотку больного гепатитом В. Это не вызвало развитие заболевания, но в дальнейшем обеспечило устойчивость к введению необработанной сыворотки, содержащей живой вирус [32]. Другие исследователи развили идею Барри Бламберга о том, что в качестве вакцины можно использовать не цельную сыворотку больного, а лишь выделенные из нее неинфекционные частицы, содержащие HBsAg, и доказали эффективность этого метода [22]. Так появились вакцины первого поколения.
Для того чтобы вакцина была свободна от живого вируса, плазму крови хронического носителя обрабатывали формальдегидом, трипсином (ферментом, разрезающим многие белки) и высококонцентрированной мочевиной. Однако это не давало 100%-ной гарантии уничтожения вируса и потому вызывало сильное беспокойство. Ситуация усугубилась, когда началось распространение синдрома приобретенного иммунодефицита (СПИДа) с плазмой крови больных гепатитом В, использовавшуюся для создания вакцины. Позже стало известно, что СПИД развивается в результате инфицирования вирусом иммунодефицита человека (ВИЧ), который можно инактивировать, увеличив количество формальдегида на этапе производства вакцины. Но возникла новая проблема: нарастающий успех и популярность вакцинации против гепатита В привели к уменьшению количества хронически больных доноров, то есть запасов плазмы крови, необходимой для создания новых партий вакцины [33]. Это стало стимулом для разработки вакцин второго поколения.
Получение принципиально новых вакцин стало возможным благодаря успехам генной инженерии. Вскоре после того, как в 1974 Уильям Робинсон описал кольцевой геном вируса гепатита В [34], появилась возможность определить нуклеотидную последовательность каждого из генов вируса, а значит и поверхностного белка HBsAg. При помощи методов генной инженерии эта последовательность была вставлена в плазмиду и перенесена в клетку, которая затем синтезировала закодированный в плазмиде белок . Сначала для этого использовали клетки млекопитающих, однако это было довольно трудоемко, дорого и не очень эффективно [33]. Настоящий прорыв случился, когда в начале 80-х Пабло Валенсуэла и Мишель де Уайльд независимо друг от друга смогли создать штаммы дрожжевых клеток (Saccharomyces cerevisiae ), содержащие плазмиды с геном поверхностного белка [22]. Это позволило наладить производство вакцины, одобренной в 1986 году. Так была изобретена первая в мире рекомбинантная вакцина, которая показала свою эффективность и безопасность и используется по сей день.
О том, как выполняются рутинные эксперименты по генной инженерии, читайте в статье «12 методов в картинках: генная инженерия. Часть II: инструменты и техники» [35]. — Ред.
О том, как еще используют пекарские дрожжи Saccharomyces cerevisiae, можно почитать в статье «Модельные организмы: грибы» [36]. — Ред.
Наши дни
Сейчас в России зарегистрировано и разрешено к применению большое количество вакцин против гепатита В как отечественного, так и зарубежного производства (табл. 2). Все вакцины обладают высокой эффективностью (80–95%) [9] и являются взаимозаменяемыми: все три или четыре вакцинации курса могут быть сделаны вакцинами от разных производителей. Также можно встретить комбинации с вакцинами против других инфекций, что позволяет сократить количество уколов для прохождения полного курса вакцинации. Одна из таких вакцин («аАКДС–ГепB+Hib») одобрена в 2019 году, и это первая отечественная вакцина для профилактики сразу пяти заболеваний: дифтерии, столбняка, коклюша, гепатита B и гемофильной инфекции. В других странах распространена комбинированная вакцина против гепатитов А и В («Твинрикс»), которая по эффективности и безопасности не уступает вакцинам против каждого из заболеваний в отдельности [37], [38]. Кроме основных компонентов в некоторые вакцины добавляют консервант тиомерсал (он же мертиолят), содержащий соединения ртути .
О том, почему этого не стоит опасаться, мы рассказывали в статье «Разработка вакцин: чем и как имитировать болезнь?» [39]. — Ред.
| Название вакцины | Производитель | Моно- или поливалентная | Культура клеток |
|---|---|---|---|
| Вакцина против гепатита В | ЗАО НПК «Комбиотех», Россия | Моновалентная | Saccharomyces сerevisiae и/или Hansenula polymorpha |
| «Регевак B» | ЗАО «Биннофарм», Россия / ЗАО «МТХ», Россия | Моновалентная | Hansenula polymorpha |
| «Эувакс B» | «Эл Джи Лайф Саенсис Лтд», Южная Корея | Моновалентная | Saccharomyces cerevisiae |
| «Инфанрикс Гекса» | GlaxoSmithKline Biologicals s.a., Бельгия | Поливалентная (дифтерия, коклюш, столбняк, полиомиелит, гемофильная инфекция, гепатит В) | В инструкции не указано |
| «Бубо-Кок» | ЗАО НПК «Комбиотех», Россия | Поливалентная (дифтерия, коклюш, столбняк, гепатит В) | В инструкции не указано |
| «Бубо-М» | ЗАО НПК «Комбиотех», Россия | Поливалентная (дифтерия, столбняк, гепатит В) | В инструкции не указано |
План вакцинации
Первую вакцинацию проводят в роддоме в первые 24 часа жизни ребенка. Это важно сделать как можно раньше, так как иммунная система еще слабо развита и организм уязвим, в то время как HBsAg-статус матери может быть неизвестен. Кроме того, даже отрицательные анализы не могут дать 100%-ной гарантии того, что мать не является носителем вируса, а при этом заражение при родах является наиболее частым способом инфицирования младенцев. Также существует вероятность заражения гепатитом В при переливании крови, которое может быть необходимо новорожденному.
Дальнейшая схема вакцинации зависит от того, относится ли ребенок к группе риска. Если нет, то еще две вакцинации проводят в соответствии с национальным календарем прививок в 1 и 6 месяцев.
Дети попадают в группу риска, если родились от матери, которая соответствует любому из ниже перечисленных критериев:
- является носителем HBsAg;
- больна вирусным гепатитом В;
- перенесла вирусный гепатит В во втором или третьем триместре беременности;
- не имеет результатов обследования на маркеры гепатита В;
- употребляет наркотические или психотропные вещества;
- из семьи, в которых есть носитель HBsAg или больной острым или хроническим вирусным гепатитом В.
Для таких детей проводят четырехкратную вакцинацию: после дозы, полученной в роддоме, следуют вакцинации в 1, 2 и 12 месяцев.
Что делать, если схема вакцинации была нарушена?
По рекомендациям ВОЗ, в случае, если расписание введения вакцин нарушено, начинать курс заново не надо. Если между первой и второй вакцинациями прошло больше времени, чем необходимо, то просто сделайте вторую прививку как можно скорее. Далее между второй и третьей вакцинациями всегда необходим перерыв минимум 4 недели. Если третья прививка также не была сделана вовремя, то и ее надо будет ввести, как только появится возможность.
Если человек не был вакцинирован при рождении, сделать прививку можно в любом возрасте по аналогичной схеме. Особенно важно провести вакцинацию людям, находящимся в группах риска [40]:
- контактирующие в быту и/или являющиеся сексуальными партнерами HBsAg-позитивных людей;
- с большим количеством сексуальных партнеров;
- мужчины, имеющие сексуальные отношения с мужчинами;
- ВИЧ-инфицированные;
- употребляющие инъекционные наркотические вещества;
- пациенты, которым часто переливают кровь или ее производные (плазма, сыворотка и др.), делают диализ;
- пациенты, которым предстоит пересадка донорского органа;
- с хроническими заболеваниями печени или последней стадией почечной недостаточности;
- заключенные в тюрьмах;
- медицинские работники и работники других сфер, в которых могут контактировать с потенциально зараженными биологическими жидкостями.
Ревакцинация
Главный показатель, по которому оценивают успешность проведенной вакцинации, — титр специфических антител против возбудителя заболевания. Но иммунитет является сложно организованной системой, в состав которой входят различные специализированные молекулы и клетки, поэтому защита организма от инфекций зависит не только от присутствия или отсутствия необходимых антител. Например, недавно показали, что у людей, начавших курс вакцинации против гепатита В в возрасте старше 6 месяцев, иммунологическая память сохраняется на протяжении как минимум 30 лет несмотря на то, что уже через 15 лет только у трети из них можно обнаружить антитела [41]. Канадский Национальный консультативный комитет по иммунизации на основании большого количества научных публикаций не нашел доказательств в пользу того, что вакцинированным в младенчестве людям необходима плановая ревакцинация [42]. В российском национальном календаре прививок (приказ Минздрава РФ от 21 марта 2014 г. №125н) тоже отсутствуют рекомендации по ревакцинации против гепатита В, однако существуют отдельные указания для медицинских работников, регулярно контактирующих с кровью, которым показана ревакцинация каждые 5 лет (МУ 3.1.2792-10. 3.1).
Иначе обстоит ситуация с больными хроническими заболеваниями, иммунитет которых ослаблен, или с пациентами, которым регулярно делают гемодиализ. Для них важно постоянно поддерживать высокий титр HBsAg-специфических антител, поэтому ВОЗ рекомендует им ежегодно сдавать анализы и проходить ревакцинацию, как только титр антител окажется ниже 10 мЕД/мл [40], [43]. Согласно методическим указаниям по профилактике инфекционных болезней в РФ пациенты отделений гемодиализа должны получать двойную дозу вакцины против гепатита В каждые 3 года (МУ 3.1.2792-10. 3.1).
Экстренная иммунопрофилактика
В случае контакта с инфицированными биологическими жидкостями (попадание их на слизистые оболочки глаз и рта, половой контакт и др.), необходимо принять срочные меры. Если человек ранее не прошел полный курс вакцинации или прошел, но имеет низкий титр специфических антител, то ему назначают четырехкратную вакцинацию. Вместе с первой прививкой (в первые 48 часов после контакта) вводят специфические иммуноглобулины человека против гепатита В. Остальные три вакцинации проводят по уже приведенной выше схеме — через 1, 2 и 12 месяцев.
Некоторые производители также предлагают для непривитых пациентов ускоренную схему вакцинации перед хирургической операцией: вторая и третья прививка через 7 и 21 день, а для пациентов отделения гемодиализа — четыре прививки, три из которых вводятся через 1, 2 и 6 месяцев.
Противопоказания
Поскольку вакцины производят с использованием дрожжевых культур, то людям с аллергией на их компоненты следует использовать эти вакцины с осторожностью. Противопоказанием также является гиперчувствительность к консерванту тиомерсалу, который входит в состав большинства вакцин.
Согласно инструкциям производителей, вакцину вводят внутримышечно: взрослым, подросткам и детям старшего возраста — в дельтовидную мышцу (плечо), а новорожденным и детям младшего возраста — в переднебоковую поверхность бедра. Введение в другое место может привести к снижению эффективности вакцинации [44] и не должно учитываться — в этом случае необходимо как можно скорее провести правильное вакцинирование [45]. Подкожное введение допустимо только для больных тромбоцитопенией и другими заболеваниями, связанными со свертываемостью крови.
Как и для прочих вакцин, противопоказанием к вакцинации против гепатита В является острое заболевание. В этом случае процедуру следуют отложить до полного выздоровления, хотя при нетяжелых ОРВИ, острых кишечных заболеваниях и других инфекциях прививку можно провести сразу же после нормализации температуры. Допускается введение вакцины на фоне нетяжелого течения заболевания, но такое решение должно приниматься совместно с лечащим врачом. Наличие какого-либо хронического заболевания само по себе не является причиной для медотвода от вакцинации, но в случае обострения необходимо дождаться, пока состояние стабилизируется, так как прививка даст дополнительную нагрузку на иммунную систему и организм в целом.
Более подробные сведения о проведении вакцинации детей и взрослых с различными нарушениями здоровья можно найти в методических указаниях МУ 3.3.1.1123-02 «Мониторинг поствакцинальных осложнений и их профилактика».
Побочные реакции
Побочные реакции в ответ на вакцину против гепатита В очень редки и обычно слабо выражены. Возникшие симптомы проходят через 2–3 дня после инъекции и не требуют медикаментозного вмешательства. Чаще всего встречается незначительная боль, покраснение и уплотнение в месте инъекции, реже встречаются незначительное повышение температуры, недомогание, усталость, боль в суставах или мышцах, головная боль, головокружение и тошнота.
В самом начале повсеместного применения новой вакцины против гепатита В, появились первые сообщения о возможной корреляции между вакцинацией и некоторыми серьезными заболеваниями, однако дальнейшие исследования не обнаружили причинно-следственных связей [46]. Вакцина против гепатита В не является живым вирусом, который размножается в организме, поэтому не представляет угрозу ни для беременной женщины, ни для ее ребенка; также можно вакцинироваться и в период кормления грудью [40]. Единственным требованием безопасности к вакцинам для беременных женщин и детей до года является отсутствие консервантов.
Возможно ли предотвратить передачу вируса от инфицированной матери к ребенку?
Хотя вирус гепатита В слишком большой для того, чтобы преодолеть трансплацентарный барьер, в 1–9% случаев все же происходит заражение плода от матерей-носителей вируса в период внутриутробного развития [47]. Это может случиться, например, в результате инфицирования плаценты, клетки которой поглотили антитела, связанные с вирусной частицей [47], или травмы, которая привела к смешению внутриутробного и материнского кровообращения (микротрансфузии) [48]. Но намного чаще вирус попадает в организм ребенка во время родов из-за травмы от хирургического вмешательства, при которой происходит смешение крови матери и ребенка, и при контакте новорожденного с материнской вагинальной жидкостью и эпителием родовых путей [48]. Наибольшему риску вертикальной (от матери к ребенку) передачи инфекции подвержены дети, у матерей которых в крови можно обнаружить HBeAg и/или высокую концентрацию вирусной ДНК (>1 млн. копий генома на мл, или 200 тыс. МЕ/мл) [48], [49], что свидетельствует об активном размножении вируса в материнском организме.
Существует несколько стратегий защиты ребенка. Независимо от того, как протекало заболевание во время беременности, сразу после рождения (в течение первых 24 часов жизни) младенцу вводят вакцину против гепатита В. Также рекомендуют вместе с вакциной внутримышечно вводить специфические к вирусу гепатита В антитела [9], хотя есть исследования, показывающие, что и просто вакцинации достаточно [33].
Если во время беременности у матери в крови было обнаружено большое количество ДНК вируса гепатита В, ВОЗ рекомендует уже в третьем триместре беременности начать противовирусную терапию [9]. В качестве препаратов применяют ингибиторы обратной транскриптазы, которую вирус использует для копирования своего генома. Такой подход уже показал свою безопасность и высокую эффективность в предотвращении передачи вируса от матери к ребенку [50].
Последующее кормление грудью, несмотря на то, что в молоке также можно обнаружить HBsAg и вирусную ДНК, не представляет серьезной опасности для младенца, который прошел необходимую иммунопрофилактику [51], [52].
Наше будущее: вакцины третьего поколения
Распространение вакцинации против гепатита В позволило снизить уровень заболеваемости во всем мире, но еще остаются люди, у которых в силу их индивидуальных особенностей даже после третьей прививки не формируется необходимое количество защитных антител. Это может происходить из-за неверного хранения и введения вакцины, пожилого возраста, ожирения, почечной недостаточности, хронических заболеваний печени, ослабленного иммунитета и генетических особенностей иммунной системы [53]. Но помимо этого, причина может быть и в составе самой вакцины: она содержит только один из трех поверхностных белков вируса (S-HBsAg), структура которого, к тому же, отличается от оригинальной, так как белок синтезируют в дрожжах, а не в естественном хозяине вируса — клетках млекопитающих.
Увеличить иммуногенность (способность вызывать иммунный ответ) вакцины против гепатита В возможно, если сделать ее антигенный состав более разнообразным и обеспечить синтез «правильных» белков, вернувшись к культивированию в клетках млекопитающих (с 70-х годов прошлого века в этой области достигнут значительный прогресс). Одним из наиболее удачных подходов оказалось производство в одной клетке сразу трех вариантов поверхностного белка вируса гепатита В (S-, M- и L-HBsAg), которые закодированы в одном гене, но синтезируются отдельно благодаря особенностям структуры гена и матричной РНК. Внесение в клетку такого гена приводит к формированию маленьких неинфекционных частиц, содержащих все три варианта поверхностного белка вируса — очень похожих на те, что отделяются от зараженной клетки во время вирусной инфекции [33].
Значительное преимущество такого варианта перед вакцинами второго поколения в том, что дополнительные белки повышают разнообразие вирусных антигенов, которые может запомнить иммунная система, и вирус уже не сможет легко спрятаться от иммунитета за счет мутаций. И самое главное то, что новая вакцина содержит участок большого поверхностного белка (L-HBsAg), с помощью которого вирусная частица связывается с клеткой печени, поэтому его нейтрализация антителами может предотвратить заражение.
Благодаря более высокой иммуногенности такая вакцина позволяет быстрее сформировать иммунологическую защиту, что позволит сократить количество иммунизаций до двух [33], [53], а следовательно, увеличить количество людей, которые пройдут курс до конца. По этой же причине она лучше подходит для экстренной иммунопрофилактики.
Несмотря на более высокую стоимость производства вакцин нового поколения, их активно пытаются внедрить в медицинскую практику [33]. Одна из таких вакцин, Sci-B-Vac (VBI Vaccines Inc.), уже одобрена в Израиле и нескольких странах Азии и Африки, а скоро будет поставляться и в Россию компанией «Фармсинтез».
Давайте решать проблему вместе
Хотя высокоэффективная вакцина изобретена более тридцати лет назад, гепатит В все еще остается серьезной проблемой здравоохранения. По оценкам группы исследователей, которая провела большой систематический анализ записей в базах данных 1965–2013 годов, наиболее высоко эндемичными оказались страны Африки и Западно-Тихоокеанского региона (рис. 10) [54].
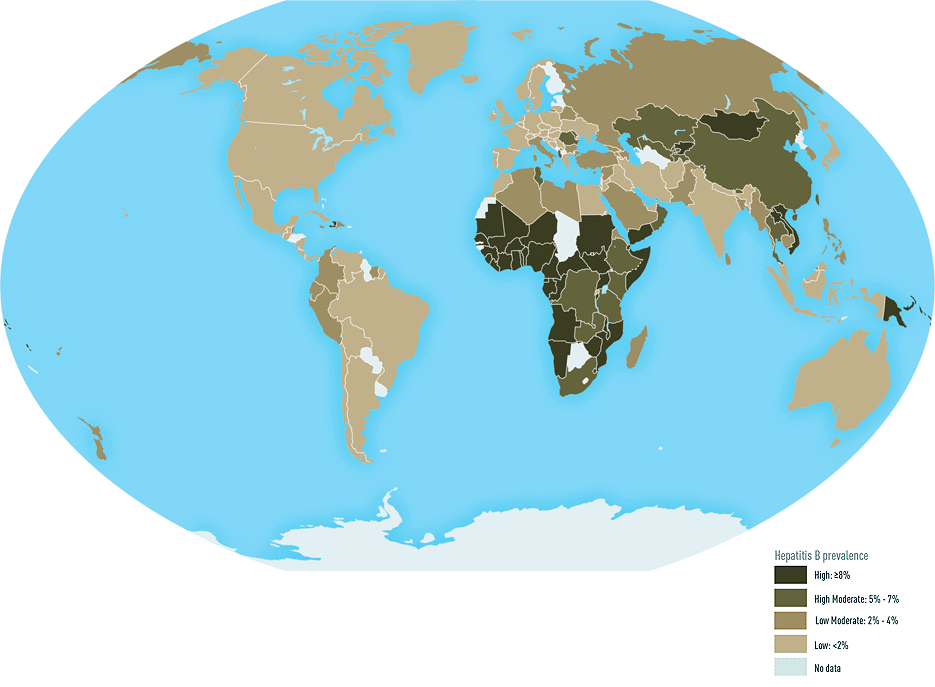
Рисунок 10. Распространение гепатита В в мире (1957–2013 гг.)
В регионах с наиболее высоким уровнем распространения гепатита В передача инфекции чаще происходит от матери к ребенку, а в странах с низкой заболеваемостью — через сексуальные связи или инъекционные наркотики [24]. Вертикальная передача от матери к ребенку стала одним из ключевых факторов в поддержании резервуара вируса в эндемичных районах (особенно в Китае и Юго-Восточной Азии), так как большинство зараженных детей в будущем станут хроническими носителями [9].
После запуска программ плановой вакцинации против гепатита В во многих странах в первые же 10 лет заболеваемость среди детей сократилась в 2–10 раз [55], но это не предел. Прогноз дальнейшего распространения инфекции позволил ВОЗ разработать отдельную программу борьбы с гепатитами В и С, основной целью которой является снижение количества случаев хронического гепатита В и С на 90% и уровня смертности в результате хронической инфекции на 65% к 2030 году. В таблице 3 перечислены ключевые направления и показатели для них, которые, по мнению ВОЗ, помогут решить поставленную задачу и предотвратить 7,1 миллиона случаев смерти из-за гепатитов В и С в период с 2015 по 2030 годы.
| Ключевые пункты | На 2015 год | К 2020 году | К 2030 году |
|---|---|---|---|
| Превентивные меры | |||
| 1. Курс из трех вакцинаций для младенцев (покрытие) | 82% | 90% | 90% |
| 2. Предотвращение передачи вируса гепатита В от матери к ребенку путем вакцинирования сразу после рождения или при помощи других подходов (покрытие) | 38% | 50% | 90% |
| 3. Проверка донорских образцов на наличие вируса (покрытие) | 89% | 95% | 100% |
| 4. Безопасные инъекции: использование стерилизованных или одноразовых инструментов в медицинской практике (покрытие) | 5% | 50% | 90% |
| 5. Обеспечение стерильными шприцами и иглами людей, потребляющих инъекционные наркотики (количество на человека в год) | 20 | 200 | 300 |
| Лечение | |||
| 1. Диагностика вирусных гепатитов В и С (покрытие) | <5% | 30% | 90% |
| 2. Лечение вирусных гепатитов В и С (покрытие) | <1% | 5 млн. (гепатит В) 3 млн. (гепатит С) |
80% могут получить доступ к лечению |
На протяжении долгого пути борьбы с вирусным гепатитом было принесено множество жертв, но и достигнуты значительные успехи. К концу 2014 года плановое вакцинирование детей против гепатита В введено в 184 странах. На рисунке 11 показано изменение доли полноценно вакцинированного населения разных стран в период с 1985 по 2018 годы. Заболеваемость вирусными гепатитами также снизилась благодаря использованию одноразовых шприцев, стерилизации медицинского оборудования и тестированию донорской крови.
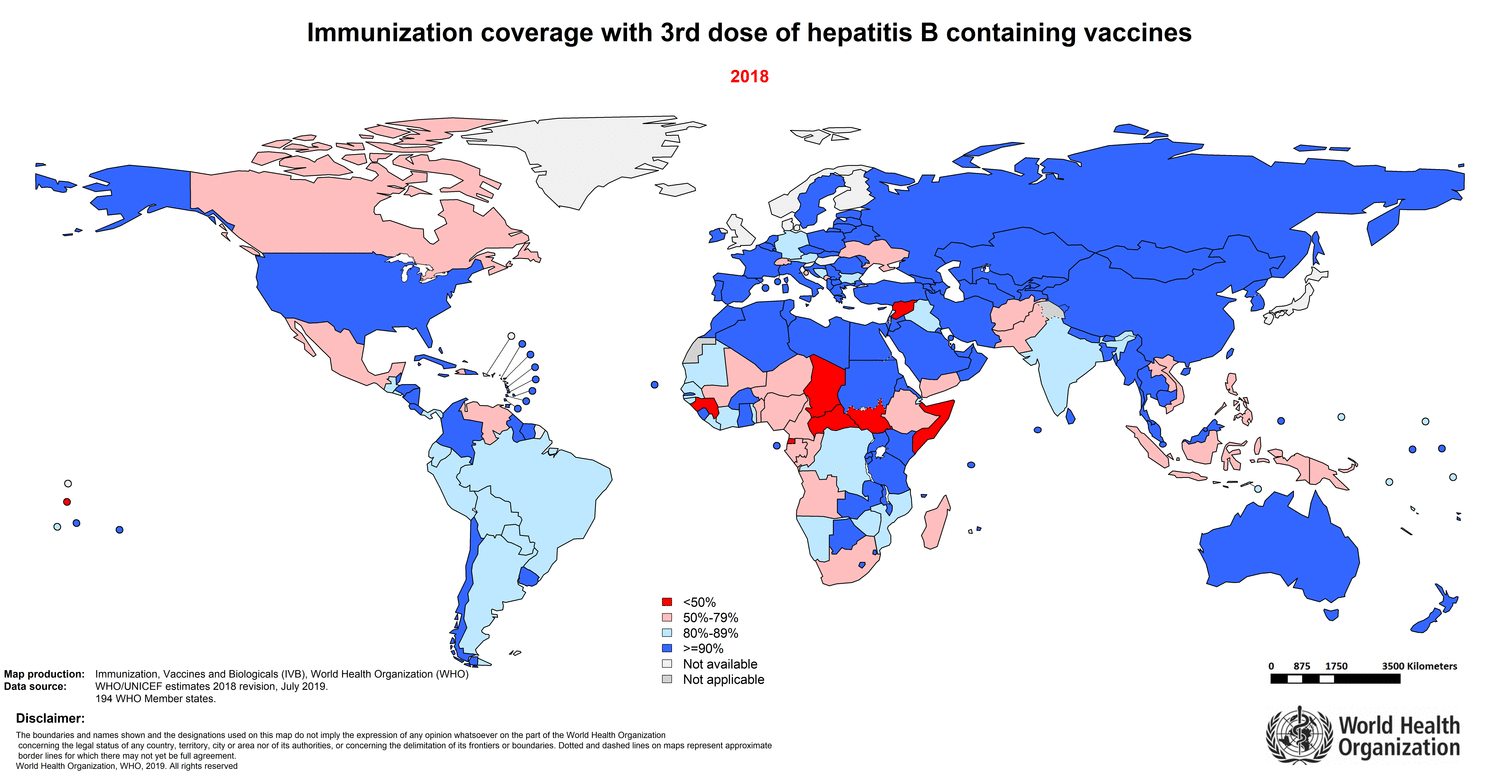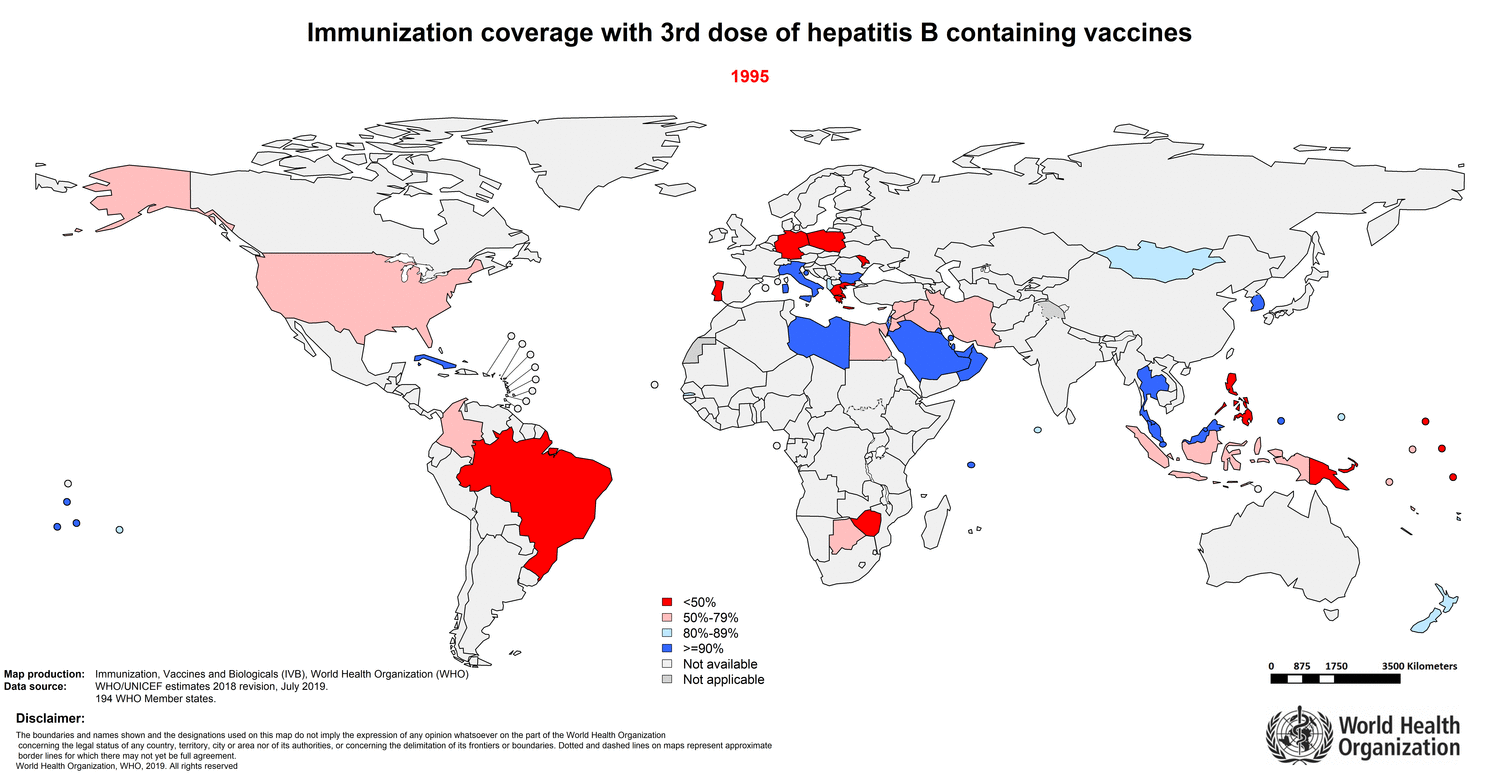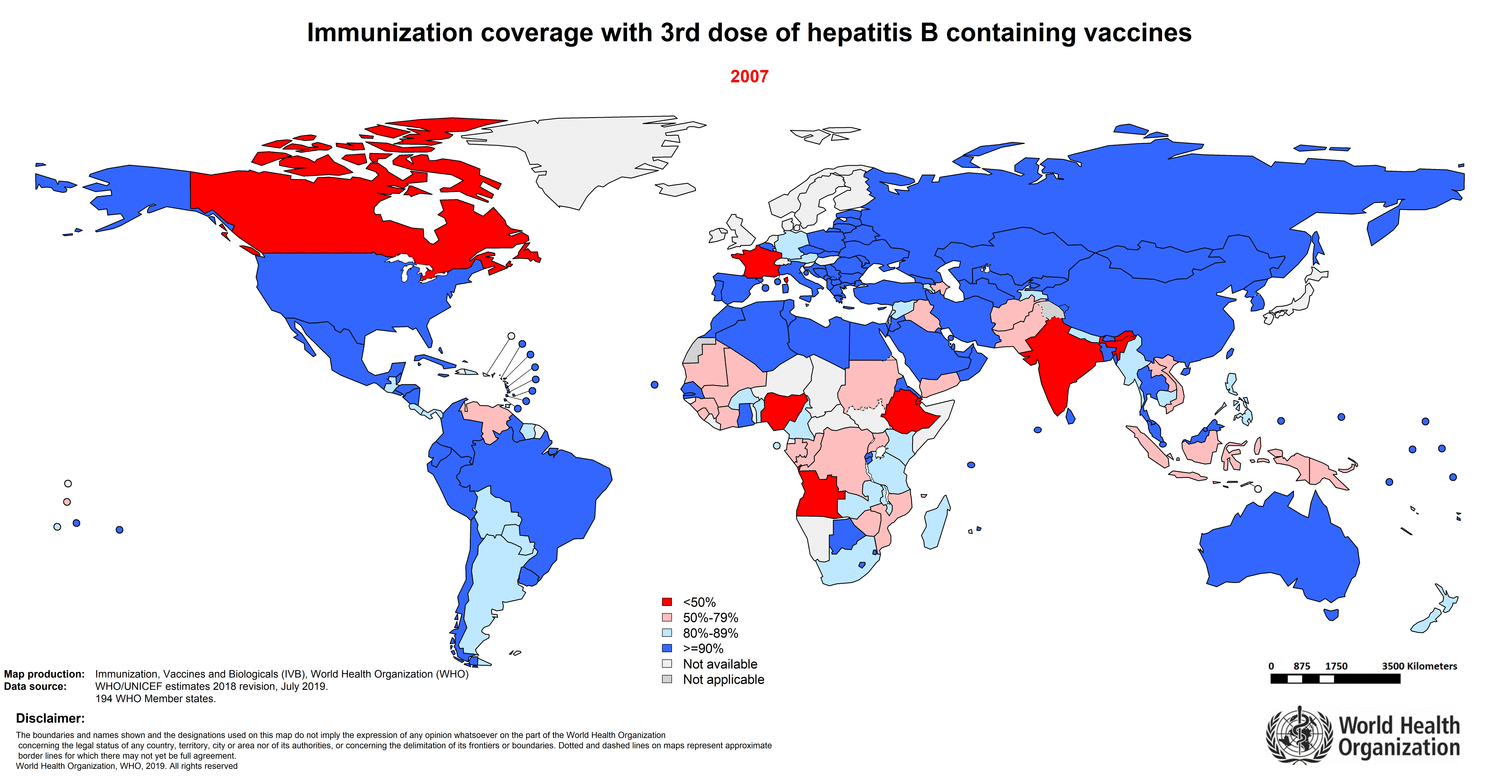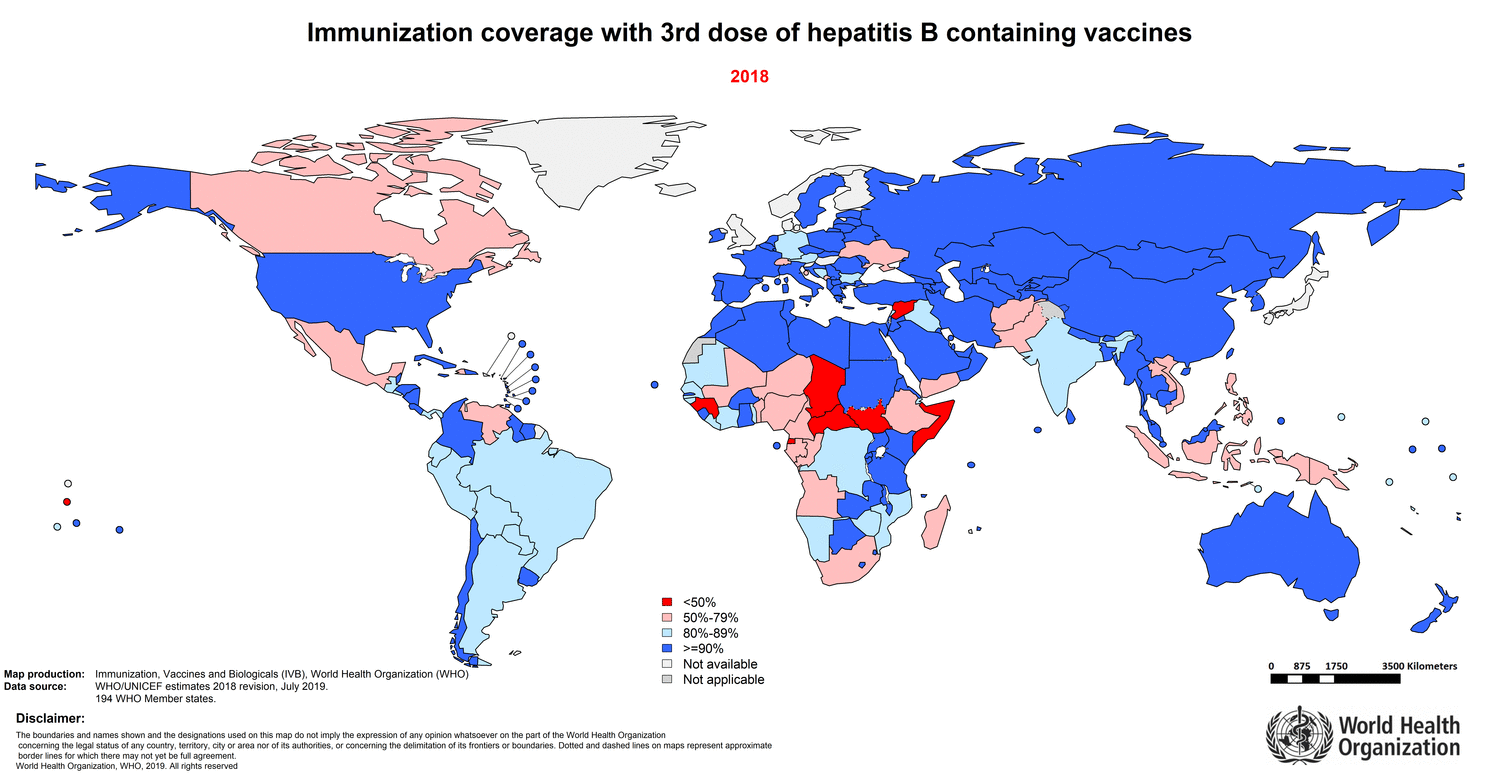
Рисунок 11. Изменение со временем доли населения, получившего трехкратную вакцинацию против гепатита В, в разных странах
Как это обычно бывает, на бумаге план выглядит простым, но на деле придется приложить немалые усилия для того, чтобы привлечь к решению проблемы заболеваемости гепатитом В все страны, которые обязаны будут организовать проведение необходимых мероприятий и выделить на это финансирование. По оценкам исследователей, расходы, необходимые для достижения приведенных целей, в среднем составят 5,5 млрд. долларов США в год [56]. Из них бóльшая часть будет приходиться на тестирование (39%) и лечение (59%). Но с каждым годом необходимые затраты будут уменьшаться благодаря распространению вакцинации, а значит и сокращению числа больных гепатитом В, поэтому выгода от такой инвестиции неоспорима.
К счастью, в России вакцинироваться против гепатита В можно совершенно бесплатно в любой городской поликлинике, поэтому не стоит надеяться на удачу и подвергать серьезному риску своих близких и детей — лучше вовремя посетить врача и пройти вакцинацию.
Литература
- Физиология человека (т. 3) / Р. Шмидт и Г. Тевс (ред.). М.: «Мир», 2005. — 228 с.;
- Вирус гепатита А: новое – это хорошо забытое старое;
- Гепатит C: решенная проблема?;
- Гепатит Е – безобидное заболевание или скрытая угроза?;
- Meryem Jefferies, Bisma Rauff, Harunor Rashid, Thao Lam, Shafquat Rafiq. (2018). Update on global epidemiology of viral hepatitis and preventive strategies. WJCC. 6, 589-599;
- Stefan Z Wiktor, Yvan J-F Hutin. (2016). The global burden of viral hepatitis: better estimates to guide hepatitis elimination efforts. The Lancet. 388, 1030-1031;
- Haidong Wang, Mohsen Naghavi, Christine Allen, Ryan M Barber, Zulfiqar A Bhutta, et. al.. (2016). Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980–2015: a systematic analysis for the Global Burden of Disease Study 2015. The Lancet. 388, 1459-1544;
- Theo Vos, Christine Allen, Megha Arora, Ryan M Barber, Zulfiqar A Bhutta, et. al.. (2016). Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990–2015: a systematic analysis for the Global Burden of Disease Study 2015. The Lancet. 388, 1545-1602;
- Guidelines for the prevention, care and treatment of persons with chronic hepatitis B infection. (2015). World Health Organization;
- Бережнова И.А. Инфекционные болезни: учебное пособие. М.: «Инфра-М», 2007. — 219 с.;
- Эмонд Р., Роуланд Х., Уэлсби Ф. Инфекционные болезни. Цветной атлас. М.: «Практика», 1998. — 440 с.;
- W BOND. (1981). SURVIVAL OF HEPATITIS B VIRUS AFTER DRYING AND STORAGE FOR ONE WEEK. The Lancet. 317, 550-551;
- Timothy M. Block, Harvey J. Alter, W. Thomas London, Mike Bray. (2016). A historical perspective on the discovery and elucidation of the hepatitis B virus. Antiviral Research. 131, 109-123;
- Jayne Hardicre. (2014). An overview of research ethics and learning from the past. British Journal of Nursing. 23, 483-486;
- Robert H. Purcell. (1993). The discovery of the hepatitis viruses. Gastroenterology. 104, 955-963;
- A.C. Allison, B.S. Blumberg. (1961). AN ISOPRECIPITATION REACTION DISTINGUISHING HUMAN SERUM-PROTEIN TYPES. The Lancet. 277, 634-637;
- B. S. Blumberg, H. J. Alter, Nancy M. Riddell, Marion Erlandson. (1964). Multiple Antigenic Specificities of Serum Lipoproteins Detected with Sera of Transfused Patients. Vox Sanguinis. 9, 128-145;
- Baruch S. Blumberg. (1965). A "New" Antigen in Leukemia Sera. JAMA. 191, 541;
- MANFRED E. BAYER, BARUCH S. BLUMBERG, BARBARA WERNER. (1968). Particles associated with Australia Antigen in the Sera of Patients with Leukaemia, Down's Syndrome and Hepatitis. Nature. 218, 1057-1059;
- IRVING MILLMAN, VERONICA ZAVATONE, BETTY JANE S. GERSTLEY, BARUCH S. BLUMBERG. (1969). Australia Antigen detected in the Nuclei of Liver Cells of Patients with Viral Hepatitis by the Fluorescent Antibody Technique. Nature. 222, 181-184;
- D.S. Dane, C.H. Cameron, Moya Briggs. (1970). VIRUS-LIKE PARTICLES IN SERUM OF PATIENTS WITH AUSTRALIA-ANTIGEN-ASSOCIATED HEPATITIS. The Lancet. 295, 695-698;
- Wolfram H Gerlich. (2013). Medical Virology of Hepatitis B: how it began and where we are now. Virol J. 10;
- Shuping Tong, Peter Revill. (2016). Overview of hepatitis B viral replication and genetic variability. Journal of Hepatology. 64, S4-S16;
- Christian Trépo, Henry L Y Chan, Anna Lok. (2014). Hepatitis B virus infection. The Lancet. 384, 2053-2063;
- Eui-Cheol Shin, Pil Soo Sung, Su-Hyung Park. (2016). Immune responses and immunopathology in acute and chronic viral hepatitis. Nat Rev Immunol. 16, 509-523;
- Silvia Piconese, Vincenzo Barnaba. (2015). Regulation of immunopathology in hepatitis B virus infection. Nat Med. 21, 548-549;
- Luan Felipo Botelho-Souza, Mariana Pinheiro Alves Vasconcelos, Alcione de Oliveira dos Santos, Juan Miguel Villalobos Salcedo, Deusilene Souza Vieira. (2017). Hepatitis delta: virological and clinical aspects. Virol J. 14;
- Robert G. Gish, Bruce D. Given, Ching-Lung Lai, Stephen A. Locarnini, Johnson Y.N. Lau, et. al.. (2015). Chronic hepatitis B: Virology, natural history, current management and a glimpse at future opportunities. Antiviral Research. 121, 47-58;
- Rebecca L. Siegel, Kimberly D. Miller, Ahmedin Jemal. (2019). Cancer statistics, 2019. CA A Cancer J Clin. 69, 7-34;
- Youhua Xie. (2017). Hepatitis B Virus-Associated Hepatocellular Carcinoma. Advances in Experimental Medicine and Biology. 11-21;
- Shaoli Lin, Yan-Jin Zhang. (2017). Interference of Apoptosis by Hepatitis B Virus. Viruses. 9, 230;
- S. Krugman, J. P. Giles, J. Hammond. (1970). Hepatitis Virus: Effect of Heat on the Infectivity and Antigenicity of the MS-1 and MS-2 Strains. Journal of Infectious Diseases. 122, 432-436;
- Wolfram H. Gerlich. (2015). Prophylactic vaccination against hepatitis B: achievements, challenges and perspectives. Med Microbiol Immunol. 204, 39-55;
- Robinson W.S., Clayton D.A., Greenman R.L. (1974). DNA of a human hepatitis B virus candidate. Journal of virology. 14, 384–391;
- 12 методов в картинках: генная инженерия. Часть II: инструменты и техники;
- Модельные организмы: грибы;
- Marina Bakker, Eveline M. Bunge, Cinzia Marano, Marc de Ridder, Laurence De Moerlooze. (2016). Immunogenicity, effectiveness and safety of combined hepatitis A and B vaccine: a systematic literature review. Expert Review of Vaccines. 15, 829-851;
- Fangjun Li, Yuansheng Hu, Youming Zhou, Lixin Chen, Wei Xia, et. al.. (2017). A Randomized Controlled Trial to Evaluate a Potential Hepatitis B Booster Vaccination Strategy Using Combined Hepatitis A and B Vaccine. The Pediatric Infectious Disease Journal. 36, e157-e161;
- Разработка вакцин: чем и как имитировать болезнь?;
- Hepatitis B vaccines: WHO position paper — July 2017. (2017). Releve epidemiologique hebdomadaire. 92, 369–392;
- Gil Klinger, Gabriel Chodick, Itzhak Levy. (2018). Long-term immunity to hepatitis B following vaccination in infancy: Real-world data analysis. Vaccine. 36, 2288-2292;
- B Henry, O Baclic. (2017). Summary of the NACI Update on the Recommended Use of Hepatitis B Vaccine. Canada Communicable Disease Report. 43, 104-106;
- Jennifer Thuener. (2017). Hepatitis A and B Infections. Primary Care: Clinics in Office Practice. 44, 621-629;
- F.E. Shaw, H.A. Guess, J.M. Roets, F.E. Mohr, P.J. Coleman, et. al.. (1989). Effect of anatomic injection site, age and smoking on the immune response to hepatitis B vaccination. Vaccine. 7, 425-430;
- National Center for Immunization and Respiratory Diseases. (2011). General recommendations on immunization — recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR. 60, 1–64;
- Penina Haber, Pedro L. Moro, Carmen Ng, Paige W. Lewis, Beth Hibbs, et. al.. (2018). Safety of currently licensed hepatitis B surface antigen vaccines in the United States, Vaccine Adverse Event Reporting System (VAERS), 2005–2015. Vaccine. 36, 559-564;
- Ahizechukwu C Eke, George U Eleje, Uzoamaka A Eke, Yun Xia, Jiao Liu. (2017). Hepatitis B immunoglobulin during pregnancy for prevention of mother-to-child transmission of hepatitis B virus. Cochrane Database of Systematic Reviews;
- Calvin Q. Pan, Zhong–Ping Duan, Kalyan R. Bhamidimarri, Huai–Bin Zou, Xiao–Feng Liang, et. al.. (2012). An Algorithm for Risk Assessment and Intervention of Mother to Child Transmission of Hepatitis B Virus. Clinical Gastroenterology and Hepatology. 10, 452-459;
- Zixiong Li, Zhenyu Xie, Hongxia Ni, Qi Zhang, Wei Lu, et. al.. (2014). Mother-to-child transmission of hepatitis B virus: Evolution of hepatocellular carcinoma-related viral mutations in the post-immunization era. Journal of Clinical Virology. 61, 47-54;
- Tram T. Tran. (2016). Hepatitis B in Pregnancy. Clin Infect Dis.. 62, S314-S317;
- J Hill. (2002). Risk of hepatitis B transmission in breast-fed infants of chronic hepatitis B carriers. Obstetrics & Gynecology. 99, 1049-1052;
- Xiangru Chen, Jie Chen, Jian Wen, Chenyu Xu, Shu Zhang, et. al.. (2013). Breastfeeding Is Not a Risk Factor for Mother-to-Child Transmission of Hepatitis B Virus. PLoS ONE. 8, e55303;
- Daniel Shouval. (2003). Hepatitis B vaccines. Journal of Hepatology. 39, 70-76;
- Aparna Schweitzer, Johannes Horn, Rafael T Mikolajczyk, Gérard Krause, Jördis J Ott. (2015). Estimations of worldwide prevalence of chronic hepatitis B virus infection: a systematic review of data published between 1965 and 2013. The Lancet. 386, 1546-1555;
- Matthew S. Chang, Mindie H. Nguyen. (2017). Epidemiology of hepatitis B and the role of vaccination. Best Practice & Research Clinical Gastroenterology. 31, 239-247;
- Shevanthi Nayagam, Mark Thursz, Elisa Sicuri, Lesong Conteh, Stefan Wiktor, et. al.. (2016). Requirements for global elimination of hepatitis B: a modelling study. The Lancet Infectious Diseases. 16, 1399-1408.







