
Клеточная мафия и коррумпированные комиссары
04 июля 2024
Клеточная мафия и коррумпированные комиссары
- 509
- 0
- 3
Для того, чтобы выдать цитотоксическим CD8+ Т лимфоцитам «лицензию на убийство», должна сформироваться «иммунная триада» из CD4+ и CD8+ Т-лимфоцитов, которые взаимодействуют друг с другом на одной дендритной клетке. Стало быть, не столько количество клеток и не только CD8+ клетки важны для уничтожения опухолевых клеток, утверждается в статье в журнале Cancer Cell. Все это важно для терапии с блокадой иммунных чекпоинтов [1].
-
Автор
-
Редакторы
Злокачественную опухоль и ее микроокружение можно сравнить с итальянской мафией периода ее расцвета — преступность множится, процветает, захватывает новые территории, а все вокруг либо закрывают на это глаза, либо оказываются вовлечены в эту порочную деятельность. В этой метафоре клетки иммунитета — коррумпированная полиция. Что же заставляет природных защитников организма обратиться против него?
Оказалось, что на один из путей поляризации макрофагов в состояние подавления иммунного ответа влияет цитидиндезаминаза. Этот белок, который убирает NH2 группу с цитозина, во многих устойчивых в иммунотерапии опухолях существенно активируется и, выполняя бесконтрольно свою функцию, увеличивает концентрацию уридиндифосфата. И уж тот-то, находясь во внеклеточном пространстве, заставляет макрофаги поляризоваться в сторону иммуносупрессии.
Международная группа исследователей, опубликовавшая работу в Nature Cancer [2], проверила, будет ли ингибирование цитидиндезаминазы оборачивать процесс вспять, и оказалось, что при лечении блокаторами иммунных чекпоинтов (anti-PD1) фармакологическое и генетическое ингибирование цитидиндезаминазы отменяет иммуносупрессию и позволяет цитотоксическим Т-лимфоцитам проникать в опухоль. И наоборот — подавление иммунного ответа возвращается или усиливается при активации цитидиндезаминазы или при введении уридиндифосфата. Эти результаты были показаны для рака протоков поджелудочной железы.
Если продолжать сицилийскую метафору, то опухоль-ассоциированные фибробласты (Cancer associated fibroblasts, CAFs) — это что-то вроде прикормленных чиновников. Изучение CAFs стало одним из трендов в онкологии порядка полутора-двух десятков лет назад и с тех пор интерес к ним не ослабевает [3], поскольку роль, которую опухоль-ассоциированные фибробласты играют в подавлении иммунного ответа, сложна, важна и разнообразна — здесь и поляризация макрофагов, и ангиогенез, и снижение активности антигенпрезентирующих клеток, и выделение антивоспалительных цитокинов, и великое множество других процессов, которыми дирижируют опухоль-ассоциированные фибробласты.
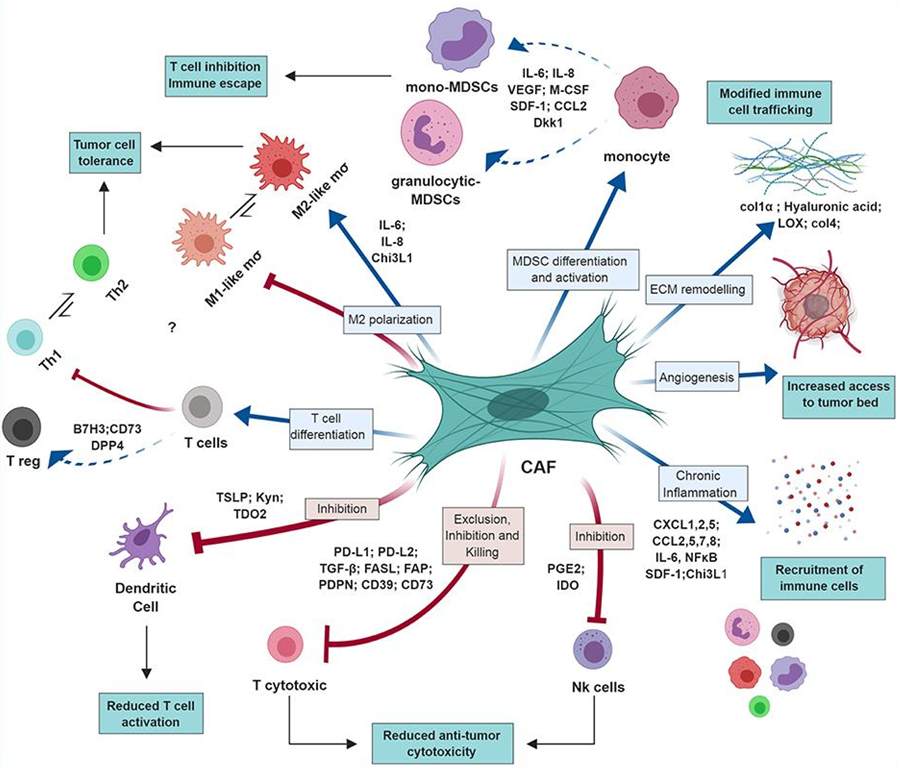
Иммуносупрессия опухоль-ассоциированными фибробластами — одно из многих видений роли фибробластов в развитии злокачественных новообразований.
Другой тренд — уже прикладной биологии, а не академической — разработка таргетных препаратов, которые бы атаковали мишени исключительно в опухоли, не задевая те же молекулы в здоровых тканях. И здесь всевозможные искусственные липосомы или выделенные из клеток везикулы естественного происхождения занимают свое место, поскольку в них можно заключить активное вещество, а сами везикулы могут конъюгировать с какой-то иной молекулой, которая будет своеобразным штрихкодом, по которому везикула достигнет адресата.
В журнале Signal Transduction and Targeted Therapy опубликовано исследование [5], авторы которого заключили в везикулы, полученные из мезенхимальных стволовых клеток костного мозга, микроРНК miR-138-5p и антифиброзный препарат пирфенидон, который подавляет рост проколлагенов I и II. Поверхность везикул была модифицирована пептидами, которые бы распознавались рецептором интегрин альфа-5 для более прицельной атаки на CAFs. Микро-РНК miR-138-5p ингибировала активацию сигнального пути трансформирующего фактора роста-бета (TGF-β), играющего важную роль в развитии опухолей. Кроме того, микроРНК подавляла синтез коллагена и вместе с пирфенидоном участвовала в перепрограммировании CAFs.
Результаты были проверены на мышах с пересаженными как человеческими, так и мышиными опухолями поджелудочной железы, и эффективность была доказана.
Но еще до того, как опухоль начнет рекрутировать клетки, подавлять иммунитет и формировать комфортную для себя нишу, еще раньше сбой дают белки-онкосупрессоры. Есть мнение, что инактивирующие мутации в генах-онкосупрессорах опаснее и важнее для формирования злокачественного новообразования, чем мутации в протоонкогенах. И бесспорной звездой в исследованиях по молекулярной онкологии является онкосупрессор p53. По разным данным ген TP53 мутирует в разном количестве опухолевых клеток — от трети до более чем половины — неудивительно, что он привлек такое внимание исследователей.
Но при всей очевидной важности этого белка до сих пор не существует таргетного препарата для p53. Авторы статьи [6], опубликованной в Journal of Hematology & Oncology, утверждают, что создали моноклональные антитела на основе иммуноглобулинов G и A для таргетной терапии при мутации p53 — замены глутаминовой кислоты на лизин в 285 положении. При этом дизайн антител исключает кросс-реактивность к нативному p53 («дикого типа»). Антитела по задумке должны синтезироваться непосредственно в организме, а сам препарат, вводимый в данном случае модельным организмам — мышам — являлся плазмидами (кольцевыми молекулами ДНК), заключенными в липидные наночастицы.
Ученые утверждают, что терапия их моноклональными антителами имела устойчивый противоопухолевый эффект, способствовала инфильтрации иммунных клеток, в том числе CD8+ лимфоцитов, которые продемонстрировали вариативность противоопухолевой активности и естественных киллеров в опухоль. Мало того, авторы даже утверждают, что наблюдали эффект сдерживания метастазирования. Однако чтобы терапия работала, на опухолевых клетках должен быть представлен рецептор к иммуноглобулину G TRIM21. Недавно было продемонстрировано [7], что TRIM21 взаимодействует с мутантным p53 с заменой аргинина на гистидин в 175 положении. Похоже, авторам статьи удалось показать, что TRIM21 взаимодействует также и с мутантом p53 E285L.
Больше статей:
- Immune checkpoint inhibitors for POLE or POLD1 proofreading-deficient metastatic colorectal cancer [8] — эффективность терапии блокаторами иммунных чекпоинтов при колоректальном раке с дисфункцией каталитической субъединицы ДНК-полимеразы.
- Integrated analysis of tertiary lymphoid structures and immune infiltration in ccRCC microenvironment revealed their clinical significances: a multicenter cohort study [9] — о клинической значимости третичных лимфоидных структур и опухоль-инфильтрующихся лимфоцитов при светлоклеточном почечно-клеточном раке.
- Circulating receptor activator of nuclear factor kappa-B ligand (RANKL) levels predict response to immune checkpoint inhibitors in advanced non-small cell lung cancer (NSCLC) [10] — о зависимости между концентрацией растворимой формы белка RANKL из семейства факторов некроза опухоли и прогнозом выживаемости у пациентов с прогрессирующим немелкоклеточным раком легкого.
- Expression of VISTA regulated via IFN-γ governs endogenous T-cell function and exhibits correlation with the efficacy of CD19 CAR-T cell treated B-malignant mice [11] — о рецепторе/лиганде VISTA и о том, какую роль он играет в активации эндогенных Т-лимфоцитов.
- Protein O-fucosyltransferase 1 promotes PD-L1 stability to drive immune evasion and directs liver cancer to immunotherapy [12] — о том, как О-фукозилтрансфераза 1 регулирует микроокружение опухоли и способствует избеганию иммунного ответа при гепатоцеллюлярном раке печени.
- Metabolic Profiling of Glioblastoma Stem Cells Reveals Pyruvate Carboxylase as a Critical Survival Factor and Potential Therapeutic Target [13] — пируваткарбоксилаза необходима для выживания и обновления стволовых клеток глиобластомы; ингибирование этого фермента и снижение концентрации глутамина приводит к дифференцировке и гибели стволовых клеток глиобластомы.
- Targeting a disintegrin and metalloprotease (ADAM) 17-CD122 axis enhances CD8+ T cell effector differentiation and anti-tumor immunity [14] — о посттрансляционном регуляторном механизме в CD8+ Т-лимфоцитах и потенциальных терапевтических мишенях для увеличения эффективности CAR-T-терапии
Литература
- Gabriel Espinosa-Carrasco, Edison Chiu, Aurora Scrivo, Paul Zumbo, Asim Dave, et. al.. (2024). Intratumoral immune triads are required for immunotherapy-mediated elimination of solid tumors. Cancer Cell;
- Tommaso Scolaro, Marta Manco, Mathieu Pecqueux, Ricardo Amorim, Rosa Trotta, et. al.. (2024). Nucleotide metabolism in cancer cells fuels a UDP-driven macrophage cross-talk, promoting immunosuppression and immunotherapy resistance. Nat Cancer;
- Erik Sahai, Igor Astsaturov, Edna Cukierman, David G. DeNardo, Mikala Egeblad, et. al.. (2020). A framework for advancing our understanding of cancer-associated fibroblasts. Nat Rev Cancer. 20, 174-186;
- Lea Monteran, Neta Erez. (2019). The Dark Side of Fibroblasts: Cancer-Associated Fibroblasts as Mediators of Immunosuppression in the Tumor Microenvironment. Front. Immunol.. 10;
- Pengcheng Zhou, Xuanlong Du, Weilu Jia, Kun Feng, Yewei Zhang. (2024). Engineered extracellular vesicles for targeted reprogramming of cancer-associated fibroblasts to potentiate therapy of pancreatic cancer. Sig Transduct Target Ther. 9;
- Dafei Chai, Junhao Wang, Chunmei Fan, Jing-Ming Lim, Xu Wang, et. al.. (2024). Remodeling of anti-tumor immunity with antibodies targeting a p53 mutant. J Hematol Oncol. 17;
- Juan Liu, Cen Zhang, Dandan Xu, Tianliang Zhang, Chun-Yuan Chang, et. al.. (2023). The ubiquitin ligase TRIM21 regulates mutant p53 accumulation and gain of function in cancer. Journal of Clinical Investigation. 133;
- M. Ambrosini, B. Rousseau, P. Manca, O. Artz, A. Marabelle, et. al.. (2024). Immune checkpoint inhibitors for POLE or POLD1 proofreading-deficient metastatic colorectal cancer. Annals of Oncology. 35, 643-655;
- Yu-Qi Wang, Wen-Jin Chen, Wang Zhou, Ke-Qin Dong, Li Zuo, et. al.. (2024). Integrated analysis of tertiary lymphoid structures and immune infiltration in ccRCC microenvironment revealed their clinical significances: a multicenter cohort study. J Immunother Cancer. 12, e008613;
- Michele Iuliani, Sonia Simonetti, Leonardo Cristofani, Silvia Cavaliere, Alessio Cortellini, et. al.. (2024). Circulating receptor activator of nuclear factor kappa-B ligand (RANKL) levels predict response to immune checkpoint inhibitors in advanced non-small cell lung cancer (NSCLC). J Immunother Cancer. 12, e009432;
- Donghai Tang, Li Zhao, Fen Yan, Chunxiao Ren, Kailin Xu, Kai Zhao. (2024). Expression of VISTA regulated via IFN-γ governs endogenous T-cell function and exhibits correlation with the efficacy of CD19 CAR-T cell treated B-malignant mice. J Immunother Cancer. 12, e008364;
- Qianyu Li, Wenyun Guo, Yifei Qian, Songling Li, Linfeng Li, et. al.. (2024). Protein O-fucosyltransferase 1 promotes PD-L1 stability to drive immune evasion and directs liver cancer to immunotherapy. J Immunother Cancer. 12, e008917;
- Ophélie Renoult, Mélanie Laurent--Blond, Hala Awada, Lisa Oliver, Noémie Joalland, et. al.. (2024). Metabolic Profiling of Glioblastoma Stem Cells Reveals Pyruvate Carboxylase as a Critical Survival Factor and Potential Therapeutic Target. Neuro-Oncology;
- Lina Sun, Anjun Jiao, Haiyan Liu, Renyi Ding, Ning Yuan, et. al.. (2024). Targeting a disintegrin and metalloprotease (ADAM) 17-CD122 axis enhances CD8+ T cell effector differentiation and anti-tumor immunity. Sig Transduct Target Ther. 9.






