
Как генетика и пол влияют на эффект нейролептиков
20 февраля 2021
Как генетика и пол влияют на эффект нейролептиков
- 1476
- 0
- 6
-
Авторы
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: В этой статье мы попытались разобраться в том, почему лекарства работают по-разному у мужчин и женщин, и в том, что, с точки зрения фармакогенетики, может помешать эффективно лечить шизофрению нейролептиками.
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2020/2021.

Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.

Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Введение
Известно, что на фармакокинетику и фармакодинамику лекарственных препаратов влияет множество факторов. Это не только возраст, различные заболевания, вредные привычки, образ жизни пациента, но пол и мутации в генах. Генетические вариации, чаще всего представленные однонуклеотидными полиморфизмами (ОНП), по последним данным [1], определяют до 50% побочных эффектов от лекарственных препаратов и резистентности к ним у пациентов с шизофренией. В свою очередь гены, в которых находятся ОНП, кодируют определенные белки, участвующие в процессах метаболизма — превращения — лекарственных средств в организме. Найденные ОНП не имеют привязки к полу, но все-таки, как оказалось, именно он существенно влияет и на проявление, и на течение болезни, и на восприятие лекарств организмом пациента.
Женщины и мужчины хоть и болеют одними и теми же заболеваниям, но переносят их по-разному. И речь здесь идет даже не о частоте распространенности или склонности к заболеванию среди представителей определенного пола, а именно о тяжести их течения и разной эффективности лекарств у мужчин и женщин. Например, женщины тяжелее переносят болезни суставов (спондилоартрит) [15], а смертность и осложнения от сердечно-сосудистых заболеваний выше у мужчин [16]. Известно, что люди испытывают дискомфорт и страдания из-за заболевания, ограничивающего их жизнь. Однако есть и другие, которые вносят изменения, преобразующие жизнь, включая исцеление в психологической, социальной и духовной сферах, независимо от исхода болезни. Необходимо отметить, что в психофармакологии именно конечный результат — социальная адаптация пациента — очень сильно зависит от эффективности и безопасности препаратов. Ведь именно в этой сфере представлен широчайший спектр лекарственных препаратов с разнообразными и далеко не всегда до конца выясненными механизмами действия, способными вызвать массу побочных эффектов в связи с влиянием на центральную нервную систему. К данной категории относятся и нейролептики, которые до сих пор подвергаются тщательному изучению.
Различные аллельные варианты гена могут существенно влиять на кодируемые ими белки и, далее, на фармакологический ответ. Сюда относятся: ферменты биотрансформации, транспортеры, молекулы-мишени, белки, которые сопряжены с молекулами-мишенями. Действие этих белков в совокупности формирует ответ на лечение. ОНП представляют собой либо замену, либо вставку, либо выпадение одного нуклеотида. Именно ОНП отвечают за изменение фармакологического ответа на лекарство в целом. Здесь возможны разные варианты развития фармакологического ответа: либо лекарство слишком мощно воздействует на пациента, что приводит к большей степени выраженности побочных эффектов, либо пациент склонен к развитию резистентности, то есть не восприимчив к действию данного лекарства, или же у пациента все параметры находятся в пределах обозначенной нормы. В первом случае врачи стараются подбирать лекарство с наименьшим спектром побочных эффектов или же значительно снижают дозировку. Во втором случае анализируют, к каким конкретно препаратам у пациента возможно развитие резистентности. И в третьем случае врачи просто подбирают препарат и прописывают дозировку по стандарту [1].
Основные генетические маркеры, связанные с изменением метаболизма нейролептиков
Метаболизм лекарств осуществляется в печени, в большей степени — различными подсемействами цитохрома Р450. Самыми важными являются: CYP2D6, CYP2C19, CYP2C9, CYP1A2, CYP3A4.
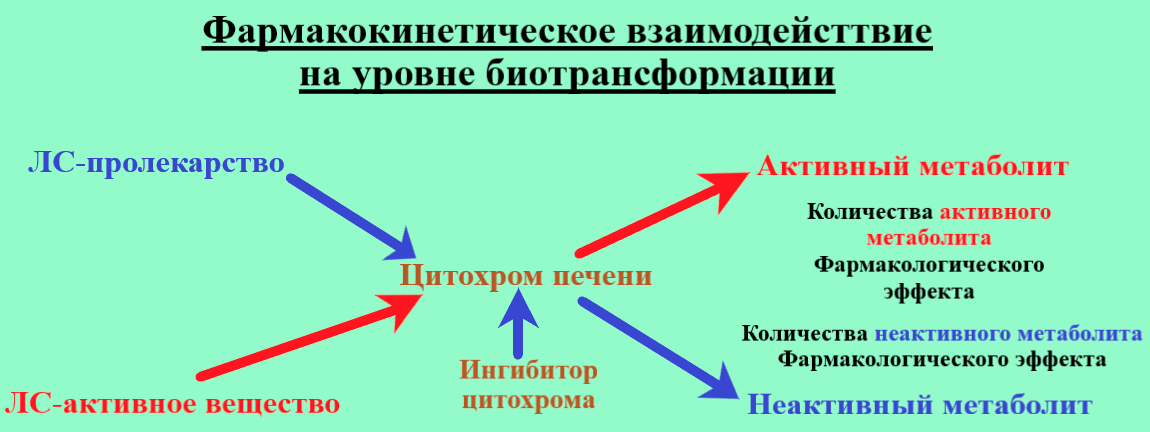
Рисунок 1. Фармакокинетическое взаимодействие на уровне биотрансформации
В транспорте многих лекарств участвует, в том числе и Р-гликопротеин, который кодируется геном MDR1. Этот транспортер помогает лекарствам проникать через гематоэнцефалический барьер — барьер между центральной нервной системой и кровеносной системой, — что очень важно, например, для нейролептиков и в целом для препаратов, применяемых в психиатрии.
Рассмотрим маркеры, которые в большей степени влияют на метаболизм и транспорт нейролептиков. [1]
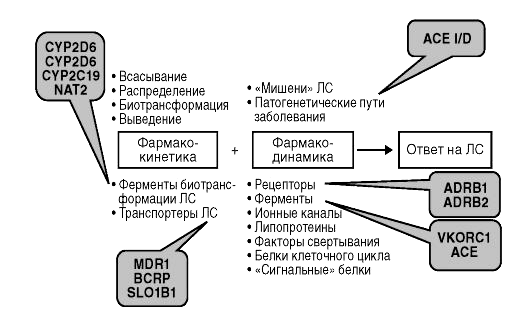
Рисунок 2. Модификации генов, которые влияют на действие и метаболизм лекарств
CYP2D6
- Если пациент гомозиготен или гетерозиготен по так называемым медленным аллельным вариантам: CYP2D6*3, CYP2D6*4, CYP2D6*5, CYP2D6*6, CYP2D6*7, CYP2D6*9, CYP2D6*10, CYP2D6*41, то не рекомендуется применение типичных — старых, мощных, — нейролептиков или же применение типичного нейролептика галоперидола в малых дозах. Возможно применение атипичных — более новых — нейролептиков, например, таких как клозапин и оланзапин. Это объясняется тем, что у таких пациентов медленный метаболизм, в связи с чем лекарство дольше задерживается в организме и длительнее выводится. Все это чревато развитием побочных эффектов, среди них наиболее неприятным является экстрапирамидное расстройство, которое значительно осложняет жизнь и социальную адаптацию пациента, даже приводя к мысли о суициде.
- Дупликация функциональных аллелей CYP2D6*1, CYP2D6*2. Здесь стоит отметить важные моменты: не рекомендуется применение типичных нейролептиков; рекомендуется применение атипичных нейролептиков, например, таких как клозапин и оланзапин.
- Генотип CYP2D6*1/*1. Это значит, что пациенту можно прописывать как типичные, так и атипичные нейролептики по стандарту [1–4].
CYP1A2
- Ингибитором этого фермента является антидепрессант флувоксамин, который способен повышать токсичность таких препаратов, как клозапин и оланзапин.
- Табакокурение снижает эффективность всех нейролептиков, поэтому курящим пациентам на время лечения придется в разы сократить употребление табака.
- Кофеин, оральные контрацептивы, антибиотик ципрофлоксацин являются конкурентными ингибиторами, поэтому повышается риск побочных эффектов нейролептиков. Для предотвращения нежелательных реакций следует ограничить себя в потреблении продуктов, содержащих кофеин, а также оральных контрацептивов и антибиотиков из группы фторхинолонов.
- «Быстрый» аллельный вариант CYP1A2*1F(AA): такие пациенты обладают быстрым метаболизмом — лекарства не задерживаются надолго в организме и быстро выводятся. Поэтому им рекомендуется прописывать дозировку выше стандартной [1–4].
CYP3A4
- В отличие от мужчин, у женщин активность этого фермента выше [1], из-за чего лекарства метаболизируются быстрее и обладают меньшей эффективностью.
- Пациенты, гомозиготные или гетерозиготные по этому аллелю, резистентны ко многим нейролептикам. Это необходимо учитывать при выборе лекарств [1], [5–7].
- Грейпфрутовый сок является ингибитором этого фермента, что тормозит превращение, метаболизм лекарств, приводит к слишком сильно выраженным побочным эффектам. На время лечения следует отказаться от его применения.
- У пациентов с этим аллелем выявлена слабая эффективность нейролептиков рисперидона и оланзапина.
MDR1
- MDR1 влияет на проходимость нейролептиков через гематоэнцефалический барьер.
- Изменение активности этого транспортера ведет к изменению количества нейролептиков, которые пройдут через биологический барьер.
- T-аллель полиморфных вариантов G2677T/A и C3435T гена MDR1. У пациентов с такой генетической особенностью выражен хороший ответ на нейролептик оланзапин.
- C-аллель полиморфизма C3435T гена MDR1. У носителей такого полиморфизма, выявлена невосприимчивость не только ко многим нейролептикам, но также к антидепрессантам [1] и нормотимикам [1], [8–11].
Гены системы серотонина
Генетические особенности серотониновой системы тоже оказывают свое влияние на фармакологический ответ при приеме нейролептиков, а также на течение самого психического заболевания.
Так, если пациенты гомозиготны по 102-му положению гена 5-НТ2А, то подвержены более тяжелому течению шизофрении, большим количествам госпитализаций в клинику. Также отмечено, что такие пациенты более чувствительны к действию нейролептика рисперидона. Это должны взять во внимание лечащие врачи, поскольку такие пациенты считаются одними из самых тяжелых [12].
Фармакогенетическое тестирование
Для того чтобы обнаружить аллельные варианты генов, рассмотренных выше, необходимо провести фармакогенетическое тестирование, которое проводится только с согласия пациента или его представителя. Перед этим врач-психиатр подробно рассказывает о том, что такое фармакогенетическое тестирование, зачем и как оно проводится, для чего необходимо и что дадут результаты этого теста. В качестве биологического материала могут выступать кровь, слюна, соскоб буккального эпителия. Тестирование проводится в несколько этапов:
- Выделение ДНК из представленного образца биологического материала пациента.
- Проведение полимеразной цепной реакции (ПЦР).
- При необходимости проведение рестрикционного анализа.
- Выявление и описание результатов.
После получения результатов составляется подробный отчет, в который обязательно входит перечень и объяснение найденных аллельных вариантов, какие лекарственные препараты подходят пациенту, а какие — не нужно применять [1].
Половые особенности
Как уже упоминалось выше, не только аллельные варианты генов могут влиять на процессы фармакокинетики и фармакодинамики лекарств, но также огромный вклад вносят половые особенности [17]. Дело в том, что шизофрения протекает у мужчин и женщин по-разному (рис. 3). Если говорить о риске ее развития, то мужчины/женщины находятся в соотношении 1,4:1 [17]. Выделим некоторые яркие особенности, которые по отдельности присущи женщинам и мужчинам [17].
На рисунке 3 мы видим различия течения шизофрении у женщин и мужчин. Также видим, что для женщин при лечении шизофрении больше подходят типичные нейролептики (например аминазин и галоперидол), а для мужчин атипичные нейролептики (например оланзапин и клозапин). Таким образом, можно сделать вывод, что пол имеет большое значение при течении такого психического заболевания, как шизофрения. Это учитывается врачами-психиатрами при назначении нейролептиков.
Заключение
Как мы видим, такие характеристики, как генетические особенности и пол пациента, очень важны при назначении нейролептиков, ведь они влияют на метаболические процессы внутри организма и на течение психических заболеваний (рис. 4). Не раз было показано, что даже непсихотропные препараты, применяемые для лечения пациентов с шизофренией, могут существенно повлиять на качество их жизни и вернуть в социальную среду [18]. Получение новых знаний об особенностях организма пациента поможет врачам бороться с такими проблемами, как внезапные, непредсказуемые и тяжелые нежелательные реакции на препараты или отсутствие эффекта от лекарств. Это, в свою очередь, улучшает качество медицинской помощи пациентам и дает надежду на скорейшее их выздоровление.
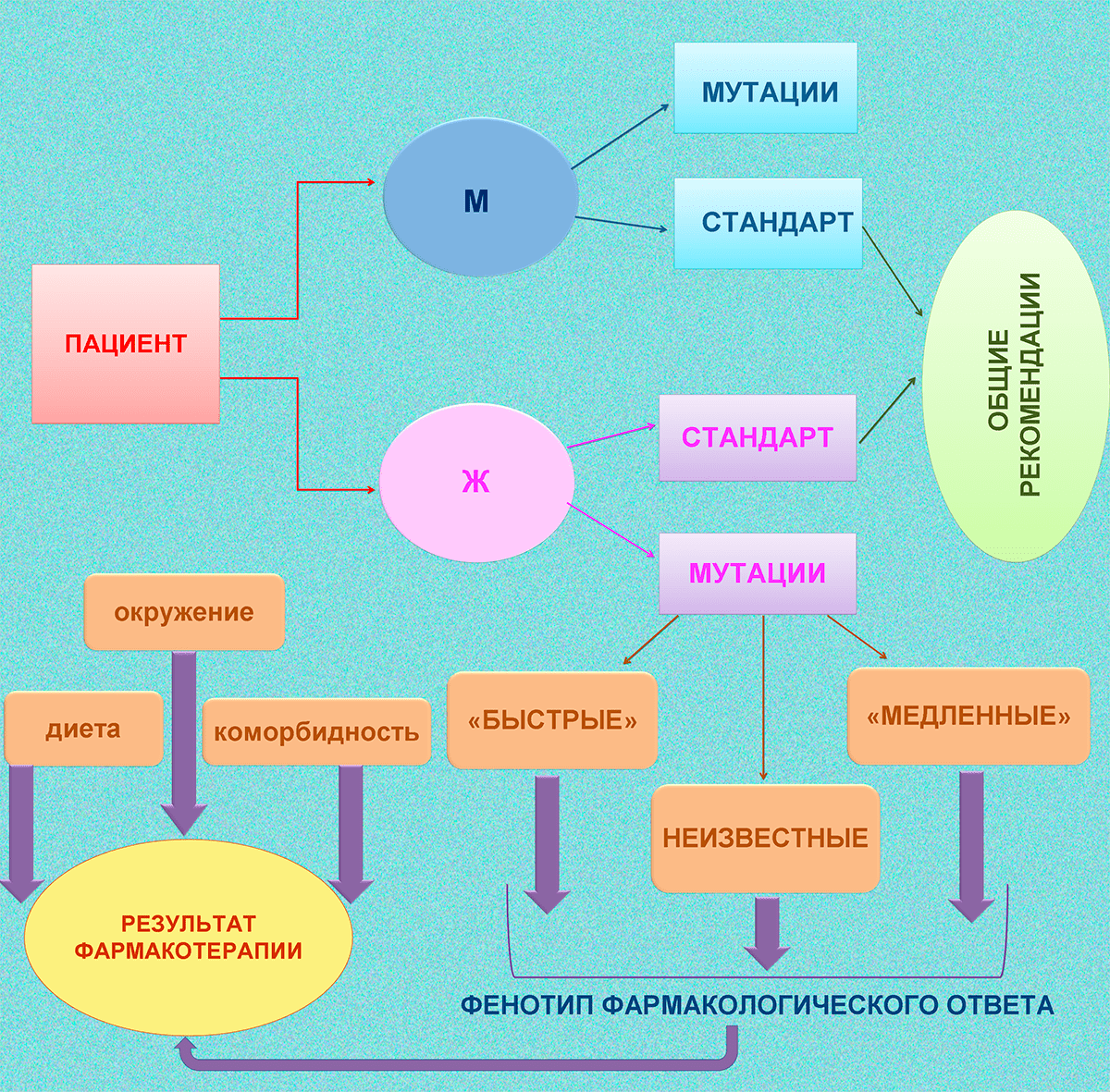
Рисунок 4. Общая схема влияния генетики и пола на фармакологический ответ. Эта информация необходима врачам-психиатрам при составлении плана лечения для пациентов с психическими заболеваниями, а именно шизофренией.
Литература
- Докукина Т.В., Гилеп А.А., Старцев А.И., Голубева Т.С., Махров М.В., Гайдукевич И.В. и др. Интерпретация результатов фармакогенетического тестирования у пациентов с психическими и поведенческими расстройствами при назначении психотропных лекарственных средств. Минск: «Мисанта», 2016. — 54 с.;
- Михеева О.М. (2011). Печень и лекарственный метаболизм. «Экспериментальная и клиническая гастроэнтерология». 2, 121–124;
- Сюняков Т.С. (2014). Молекулярная генетика и фармакогенетика биполярного аффективного расстройства: обзор материалов 26-го Конгресса Европейской коллегии нейропсихофармакологии. «Психиатрия». 3, 73–87;
- Сычев Д.А., Игнатьев И.В., Раменская Г.В., Кукес В.Г. Клиническая фармакогенетика. М.: «ГЭОТАР-МЕДИА», 2007. — 248 с.;
- Shingo Kakihara, Reiji Yoshimura, Koji Shinkai, Chima Matsumoto, Makiko Goto, et. al.. (2005). Prediction of response to risperidone treatment with respect to plasma concencentrations of risperidone, catecholamine metabolites, and polymorphism of cytochrome P450 2D6. International Clinical Psychopharmacology. 20, 71-78;
- J. Du, A. Zhang, L. Wang, J. Xuan, L. Yu, et. al.. (2010). Relationship between response to risperidone, plasma concentrations of risperidone and CYP3A4 polymorphisms in schizophrenia patients. J Psychopharmacol. 24, 1115-1120;
- K L Bigos, R R Bies, B G Pollock, J J Lowy, F Zhang, D R Weinberger. (2011). Genetic variation in CYP3A43 explains racial difference in olanzapine clearance. Mol Psychiatry. 16, 620-625;
- Eva J Brandl, James L Kennedy, Daniel J Müller. (2014). Pharmacogenetics of Antipsychotics. Can J Psychiatry. 59, 76-88;
- David W. Boulton, C.Lindsay DeVane, Heidi L. Liston, John S. Markowitz. (2002). In vitro P-glycoprotein affinity for atypical and conventional antipsychotics. Life Sciences. 71, 163-169;
- Nada Bozina, Martina Rojnic Kuzman, Vesna Medved, Nikolina Jovanovic, Jadranka Sertic, Ljubomir Hotujac. (2008). Associations between MDR1 gene polymorphisms and schizophrenia and therapeutic response to olanzapine in female schizophrenic patients. Journal of Psychiatric Research. 42, 89-97;
- Кукес В.Г., Сычев Д.А., Раменская Г.В., Игнатьев И.В. (2007). Фармакогенетика системы биотрансформации и транспортеров лекарственных средств: от теории к практике. «Биомедицина». 1, 29–47;
- Иванов М.В. и Чомский А.М. (2012). Фармакогенетические аспекты нейролептической терапии психических расстройств. «Обозрение психиатрии и медицинской психологии». 4, 40–43;
- Березанцев А.Ю. (2017). Нейробиологические и психосоциальные аспекты гендерных различий в клинических проявлениях и течении шизофрении. «Неврология, нейропсихиатрия, психосоматика». 4, 77–81;
- Булгакова М.Д. Каталептогенная активность галоперидола у крыс и ее изменение в зависимости от функционального состояния яичников и надпочечников: дис. ... канд. биол. наук. — Волгоград, 2015. — 170 с.;
- T. Rusman, R. F. van Vollenhoven, I. E. van der Horst-Bruinsma. (2018). Gender Differences in Axial Spondyloarthritis: Women Are Not So Lucky. Curr Rheumatol Rep. 20;
- Vera Regitz-Zagrosek, Georgios Kararigas. (2017). Mechanistic Pathways of Sex Differences in Cardiovascular Disease. Physiological Reviews. 97, 1-37;
- Mitchell B. Crawford, Lynn E. DeLisi. (2016). Issues related to sex differences in antipsychotic treatment. Current Opinion in Psychiatry. 29, 211-217;
- Piyumi Fernando, Iris E.C. Sommer, Alkomiet Hasan. (2020). Do we need sex-oriented clinical practice guidelines for the treatment of schizophrenia?. Current Opinion in Psychiatry. 33, 192-199.








