Использование метанотрофных бактерий в биоремедиации
03 апреля 2025
Использование метанотрофных бактерий в биоремедиации
- 87
- 0
- 0
Обложка — показательное изображение, как бактерия из чашки Петри может изменить мир.
Рисунок в полном размере.
коллаж составлен автором статьи при помощи ИИ и программ фоторедакторов
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: На нашей планете живут самые разные микроорганизмы, многие из них участвуют в процессах связанных с регулированием тех или иных процессов и показателей на территории своего обитания. Правильное использование таких бактерий-регуляторов может привести к решению проблем, связанных с экологией. Одна из групп таких бактерий-экологов — метанотрофы: они способны поглощать и перерабатывать парниковый газ метан, поэтому вызывают исследовательский интерес. В этой статье я расскажу подробнее о пользе бактерий и поиске их «под ногами» в г. Калининград.
Конкурс «Био/Мол/Текст»-2024/2025
Эта работа опубликована в номинации «Своя работа» конкурса «Био/Мол/Текст»-2024/2025.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Известно, что помимо СО2, существуют и другие газы, которые при достижении определенной концентрации негативно влияют на экологию и климат, соответственно. Один из этих газов — метан (СН4), и он же заслуженно занимает 2 место по уровню выделения (около 600 миллионов метрических тонн в год) и влияния на повышение температуры на планете.
Повышение температуры на планете, в свою очередь, влияет на различные сферы жизни человека, и не только: хуже всходят посевы, уменьшаются показатели выживаемости живых существ из-за ухудшения их адаптации к новым температурам и условиям, так как где-то резко становится излишне жарко, где-то излишне холодно, засухи в одних местах и потопы в других. И хотя геологи и прочие специалисты по нашей планете считают, что эти процессы естественные, есть основания полагать, что в случае с воздействием антропогенных факторов (наших человеческих усилий), естественные процессы происходят в разы быстрее и потому не приносят некоего развития сообществам проживающим на планете, а наоборот, губительно сказывается на них.
Известно, что метан выделяется в качестве продукта жизнедеятельности всех животных, в том числе людей, а также: от мусорных полигонов, от болот, от захоронений, от тающих слоев «вечной мерзлоты», и, конечно, в процессах производства метан часто становится невольным «соседом», особенно при выработке различных полезных ископаемых.
Выделяясь, метан становится весьма влиятельным газом, который может годами болтаться в атмосфере и создавать «парниковый эффект», влиять негативно на рост различных растений, здоровье человека, становиться причиной пожаров или взрывов. И таким образом мы как бы оказываемся в неприятном метановом лабиринте, с одной стороны — из него некуда деться, с другой стороны — существуют природные регуляторы для многих встречающихся в природе процессов и веществ.
What is it: «Биоремедиация»?
И тут мы переходим к биоремедиации, это как раз использование природных регуляторов в целях улучшения показателей экологии. Если обратимся к банальной поисковой системе, то узнаем, что:
Сложность биоремедиации заключается в малой изученности сообществ микроорганизмов, которые проживают вне живого существа, и при этом, не являясь патогенными или паразитирующими, что-то да делают в природе. Технически для науки такие микроорганизмы долгое время казались бессмысленной массовкой, и таким исследованиям до сих пор уделяется недостаточно внимания, а зря.
Сейчас довольно просто представить себе, например, человеческий кишечник, в котором прочно обосновались разного рода бактерии, исполняющие различные функции, связанные с пищеварением. Известно, что без микробиома человек будет, как минимум, страдать. То же самое происходит с природными системами. Где-то главенствуют одни бактерии, где-то другие, но факт в том, что бактерии (и разные другие не видимые глазу организмы) выполняют огромный массив работы и внутри человека, и в почве, и в воде, и т.д. (везде-везде).
Особенность биоремедиации в том, что она работает примерно по принципу «Бифиформа», но на больших территориях планеты. Уже сейчас можно купить препараты для очистки воды и почвы от нефти, биопрепараты для скотомогильников, и так далее. И такие средства состоят из различных непатогенных бактерий, часто даже подобранных исходя из региональных особенностей микроорганизмов, их устойчивости к температурам, сочетаемости с другими микрососедями и так далее. Но у готовых препаратов есть минусы: небольшие запасы, маленькие сроки годности, стоимость, небольшой выбор готовых препаратов (так как они разрабатываются под часто встречающиеся ситуации заказчиков, как правило, крупных коммерческих предприятий), низкий или нулевой КПД для регионов с не подходящими для работы препарата условиями. Игнорировать такие минусы можно научившись использовать экобактерии «в потоке», и для этого необходимо их изучать с различных сторон.
Метановый лабиринт и бактерии в нем
А теперь представьте, что есть бактерии, обладающие ферментной системой метаномоноксигеназой, могут поглощать метан в пропорции: литр кислорода/литр метана и на выходе давать еще и литр питательной среды для разного рода растений и животных? Звучит как фантастика, которая может стать реальностью и решить одномоментно множество проблем, связанных с экологией. В недалеком прошлом, в СССР, для подкормки крупного рогатого скота белком использовался препарат «Гаприн», собственно, размноженные в биореакторе и высушенные метанотрофные бактерии. И именно в условиях биореактора были получены результаты 1:1:1. В конце прошлого десятилетия «Гаприн» обрел вторую жизнь, год назад был составлен ГОСТ Р 71301-2024 специально для этой подкормки из метанотрофных бактерий.

Рисунок 2. Гаприн.
комикс составлен автором статьи при помощи ИИ и программ фоторедакторов
Для того, чтобы активировать метаномоноксигеназу, необходимо некоторое количество кислорода и непосредственно метана, и, возможно, ионы металла [1]; их, в свою очередь, впитывают, как губки, мхи. Благодаря чему, по мнению ряда исследователей [2], метанотрофные бактерии в большей степени проживают на мхах и постоянно участвуют в регуляции метана в атмосфере. Тут важно отметить — мхи используют в качестве субстрата камни и различные поверхности, на которых не каждое растение сумеет удобно разместиться, и таких территорий довольно много, часто они остаются после плохой ликвидации производств, полигонов.
Те же Романцевские горы, которые появились вследствие разработки полезных ископаемых и отсутствия работ по грамотной ликвидации предприятия и рекультивационных мер. На территории тех же Романцевских гор находятся десятки видов мхов [3].
Поиск бактерий «под ногами»
Исходя из позиции: мхи + метанотрофы = дешевая биоремедиация, у меня сложилась теория о восстановлении «природной» микрофлоры нарушенных земель без использования готовых дорогих препаратов, а используя «свежие» микроорганизмы высеянные в регионе, где планируется биоремедиация нарушенных земель, но в районах с ненарушенным биогеоценозом. Таким образом, можно было бы избежать различных рисков связанных с влиянием новых для конкретной территории бактерий (от того, что бактериальный препарат не сработает, до потенциального вреда от бактерий в препарате для животных проживающих на заданной территории).
Поэтому я попыталась высеять метанотрофных бактерий «из под ног» во мхах на территории г. Калининграда, используя методики, которые до меня работали у других исследователей данных бактерий. Спойлер: дальше я расскажу о действиях, которые предпринимала для поиска и идентификации бактерий.
Результаты поиска
Объектами исследования служили мхи Сeratodon purpureus и Sphágnum, мхи были отобраны в качестве объектов исследования в связи с тем, что метанотрофные бактерии традиционно считаются ассоциантами мхов.
Субъектами исследования стали бактерии выделенные с проб мха при помощи накопительной избирательной среды.
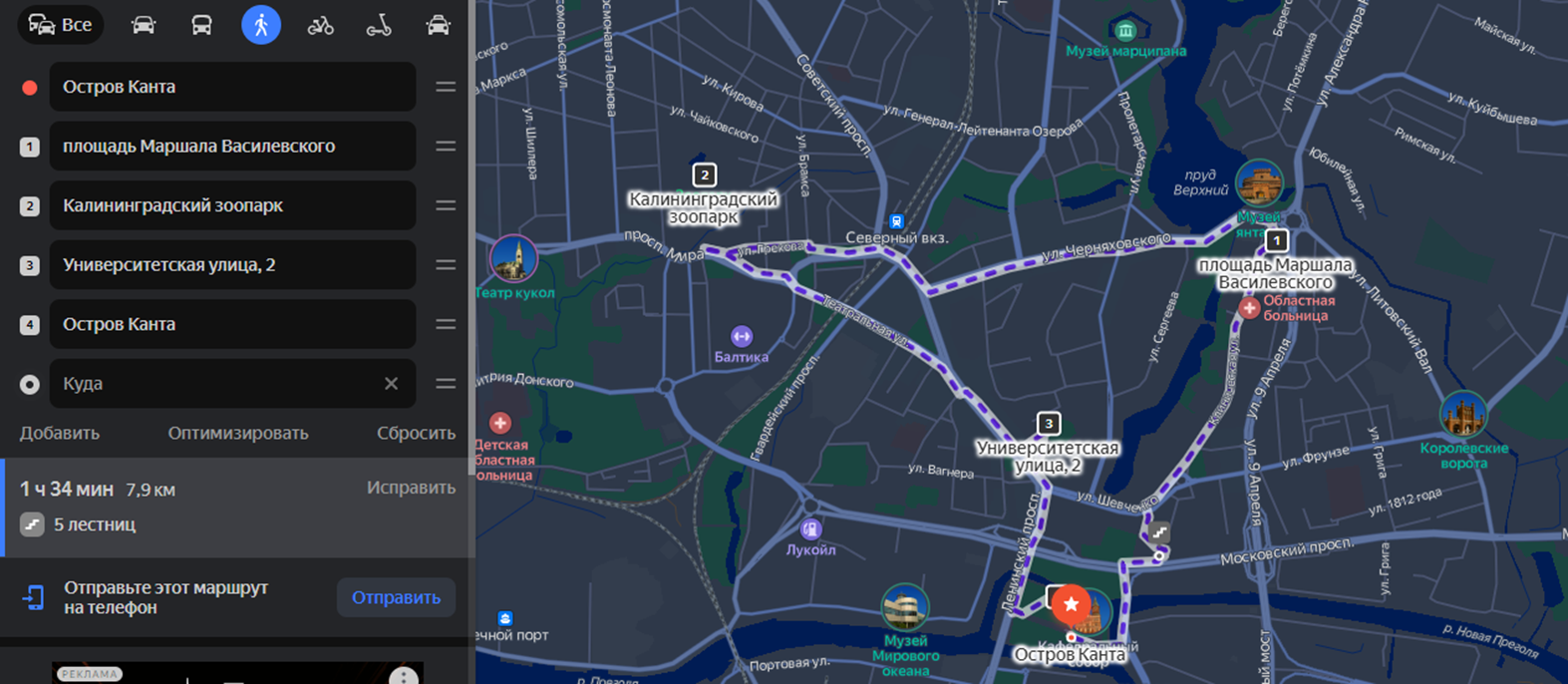
Рисунок 3. Карта точек отбора проб.
Яндекс Карты
Отбор проб производился с 4 точек в черте г. Калининград:
- о. Канта,
- ул. Университетская,
- парк у пл. Василевского,
- канализационный люк возле вольера слона в городском Зоопарке.
Были собраны 4 смешанные пробы, каждая по 50–60 грамм, мхов Сeratodon purpureus и Sphágnum.

Рисунок 4. Место на о. Канта, где была отобрана 1 проба.
фото автора статьи
Пробы собирались в стерильные пластиковые баночки для сдачи анализов на 100 мл при помощи пластикового ножа из стерильного набора, после чего крышка неплотно закручивалась для доступа кислорода, и пробы переносили в лабораторию. Хранение мха до перемещения в накопительную среду проходило в условиях тени и комнатной температуры.
Чтобы получить среду, нужную для развития метанотрофных бактерий, либо близкую к нужной по условиям проживания, использовалась жидкая накопительная избирательная среда с добавлением метанола. В таблице представлен ее рецепт:
| Название | Количество (г/л) |
|---|---|
| KH2PO4 | 2 |
| (NH4)2SO4 | 2 |
| NaCI | 0,5 |
| MgSO4 * 7H2O | 0,025 |
| FeSO4 * 7H2O | 0,002 |
| Дистилированная вода | 1000 |
| Метанол | 5 |
Особенность данной накопительной избирательной среды в том, что бактерии изначально подвергаются тестированию на устойчивость к метанолу (в дикой природе метанотрофные бактерии питаются метанолом). Большинство других бактерий в среде с метанолом не развиваются и гибнут, таким образом, добавление метанола в накопительную среду дает преимущества для выживаемости только нужных нам метанотрофных бактерий.
Пробы мха по 5 гр переносились в большие треугольные колбы на 250 мл, в которые была добавлена простерилизованная среда. После чего пробы закрывались фольгой и ватным тампонажем для избежания контаминации, то есть загрязнения другими организмами (бактериями и др.). Каждая проба инкубировалась 14 дней на качалке при температуре 28 градусов по Цельсию.

Рисунок 5. Инкубирование в качалке.
фото автора статьи
Полученная в результате инкубирования накопительная культура переносилась на среду с агаром чашки Петри при помощи автоматической пипетки и наконечника на 1000 мкл. Чашки выставлялись в различные условия: термостат на 36 градусов по Цельсию, термостат — на 28 градусов по Цельсию, холодильник — с 4 градусами по Цельсию.
Чтобы получить чистую культуру, при помощи металлической петли визуально просматриваемые колонии переносились в новые чашки петри с той же средой на агаре. Для получения круглых колоний понадобилось не менее 3 переносов с каждой пробы.
Для получения чистой культуры в жидкой среде культура переносилась с чашки Петри при помощи петли в колбы на 250 мл, наполненные стерилизованной в автоклаве и остывшей средой. Колбы также помещались в различные условия: комнатная температура (19–22 градуса по Цельсию) и термостат на 36 градусов по Цельсию.
В дальнейшем использовалась та же среда в жидком и твердом виде (с агаром), и добавлялись различные ферменты сверх состава среды, по отдельности:
- L-метионин — 0,05% от объема,
- Сахароза — 1% от объема,
- CaCl — 0,5% от объема.
Ферменты подбирались исходя из результатов исследований сред для культивации метанотрофных бактерий от других исследователей.
Все работы проводились в ламинарном боксе, специальном столе с особенным потоком воздуха, не допускающим попадания посторонних микроорганизмов. Для каждой пробы менялись наконечники пипетки, металлическая петля стерилизовалась при помощи спиртовки. Все жидкости и все ферменты, за исключением метанола и L-метионина, подвергались автоклавированию при 121 градусе по Цельсию.
Результаты культивирования
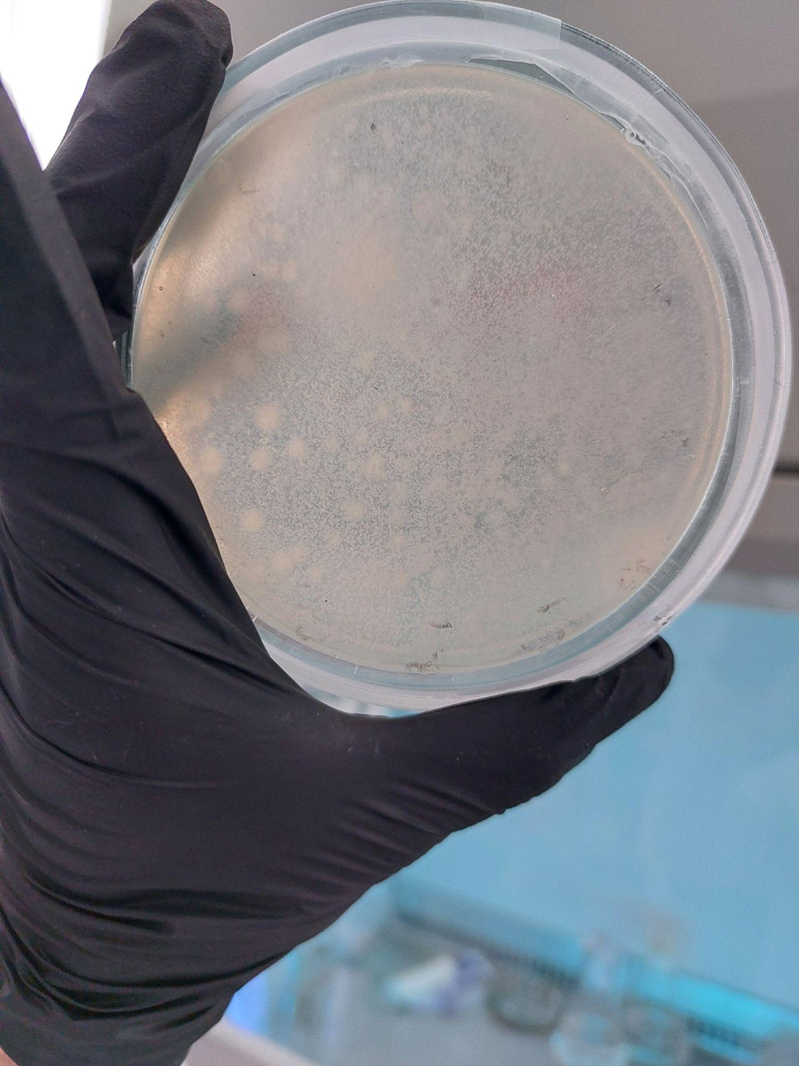
В результате культивирования были получены 9 накопительных культур, в пробах 3, 4, 5 была явно видна розовая хлопьеобразная взвесь, в пробах 1 и 2 взвесь присутствовала, но в более светлых оттенках, пробы 6–7 похожи на пробу 1 и 2, а проба 8 осталась прозрачной, 9 проба дала зеленый осадок при тех же условиях.

Рисунок 7. Розовая взвесь.
фото автора статьи
В жидкой среде пересаживание до более чистых культур дало результат у пробы 1 и 2. У пробы 1.1.1 — появились значительные коричневые вкрапления, однако, визуально похожие на грибок. У пробы 2.1.1 — шарообразные светлые плавающие колонии с розовой серединой. Обе культуры развивались в течение 2 недель при комнатной температуре. После чего были рассажены вновь на 1.1.1.1 и 1.1.1.2, и 2.1.1.1 и 2.1.1.2. Пробы 1.1.1.2 и 2.1.1.2 были помещены в термостат на 36 градусов, первую неделю наблюдался бурный рост, после чего культур визуально больше не становилось. Культуры, находящиеся при комнатной температуре, развивались медленнее, и визуально массы меньше.
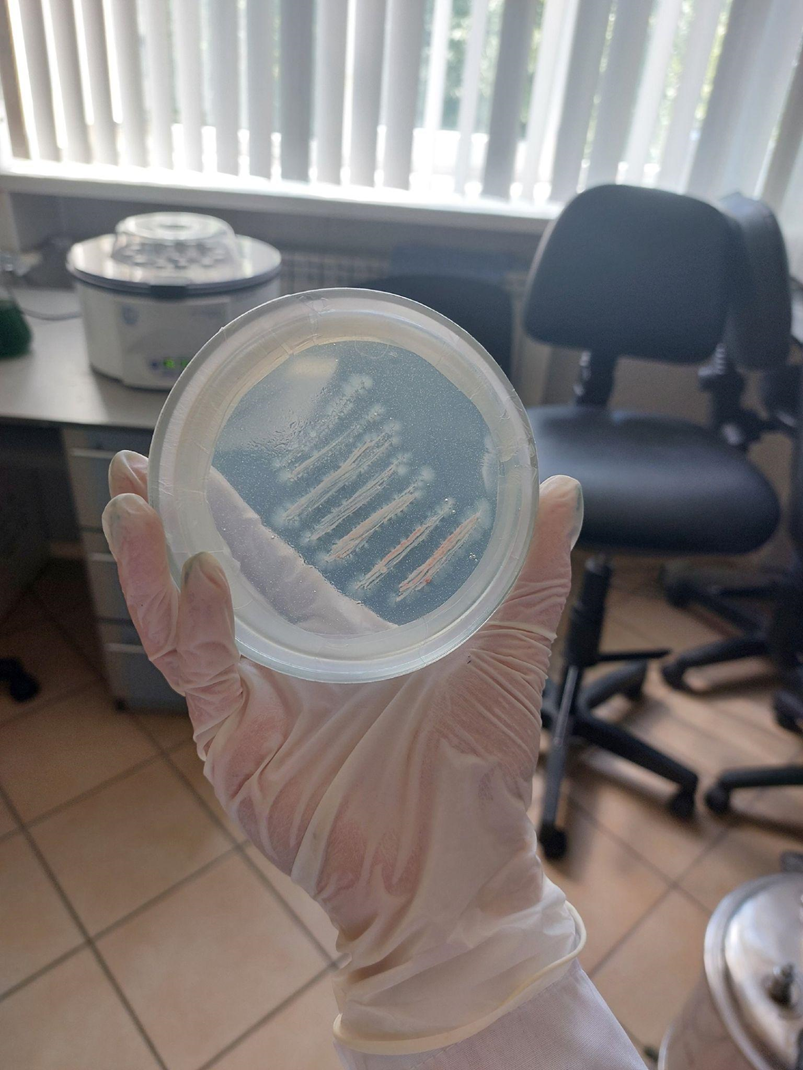
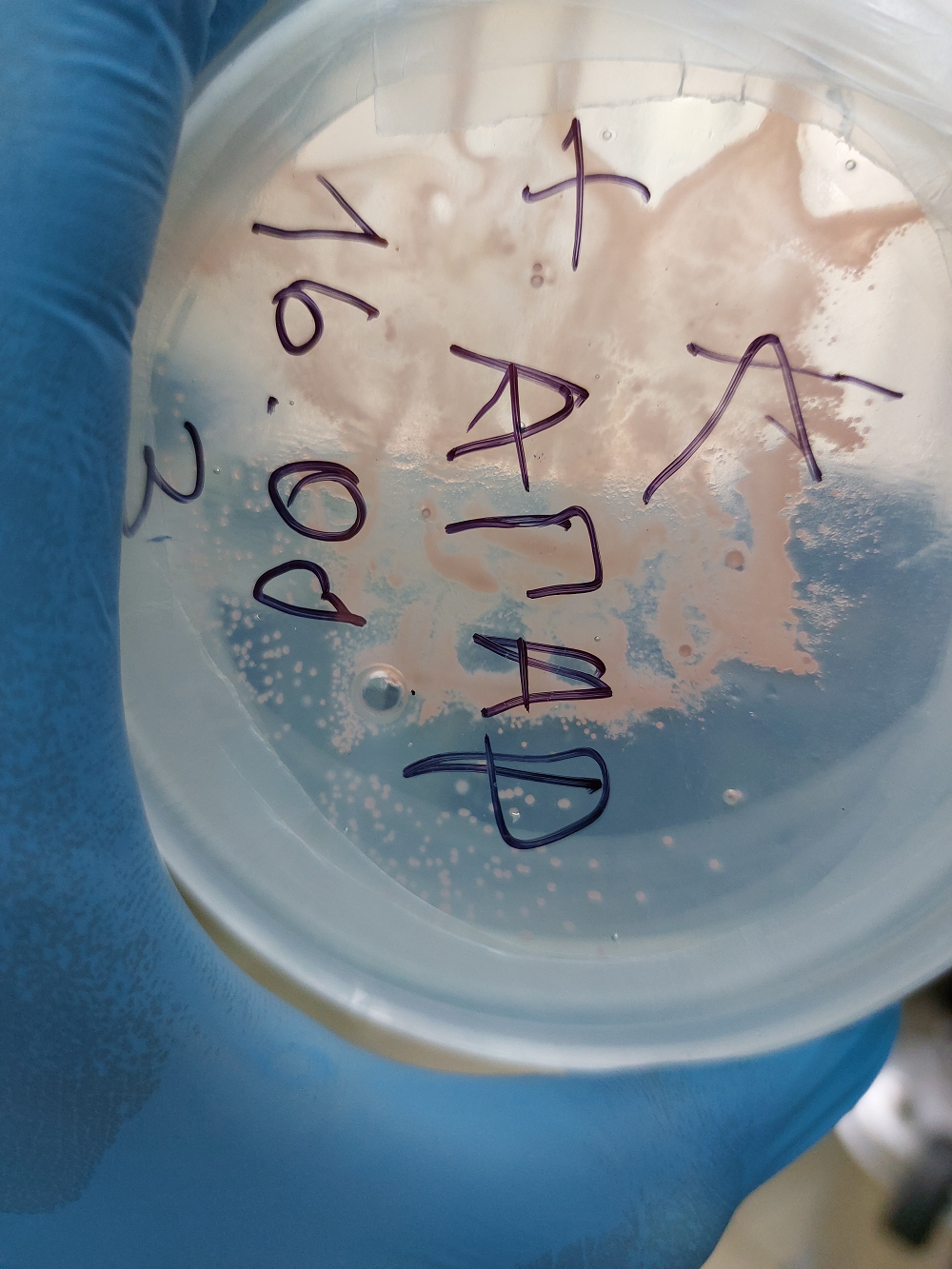
На твердой среде пробы 1–5 давали стабильный результат с глянцевыми красноватыми культурами, которые «расползались» по следам метанола, изредка «выдвигаясь» круглыми колониями по сторонам от участков, на которые бактерии были пересажены истончающим штрихом. Пробы 6–7 давали «сдвоенные» результаты, они меняли окраску в процессе культивирования, при пересадке розовых колоний могли вырасти похожие на розовые, но при этом сине-зеленые, и наоборот. Проба 8 — очень тонкие светлые колонии. Проба 9 — только плесень, поэтому исключена из дальнейшего исследования.
На пробе 2.2 были обнаружены «наросты» похожие на растительные. Однако идентифицировать их не удалось.
Рисунок 9. Проба 2.2.
фото автора статьи
Дальше расскажу, что получилось, а пока о морфологии экологически полезных бактерий.
Метанотрофные бактерии — прокариоты, грамотрицательные, в зависимости от штамма их форма отличается, в основном палочки и кокки. У большинства метанотрофных бактерий есть 2 типа клеток, вегетативные, активные клетки, и экзоспоры, покоящиеся формы, способные на выживание в экстремальных условиях.
Метанотрофные бактерии часто имеют окраску, связанную с выделением каротиноидов, в связи с этим их колонии на твердой среде (без добавления красителей) при визуальном осмотре выглядят розовыми, темно-розовыми, красными, темно-оранжевыми, но могут поменять свой цвет со временем, возможно, исчерпав запасы для метаболического продуцирования каротиноидов. Форма колоний — круглая, до пары миллиметров, поверхность — глянцевая, при пересадке петлей тягуче-жидкие, сохраняющие цвет и глянец, и на самом деле эти колонии очень сильно напоминают капли красного плотного блеска для губ. Знание морфологии бактерий помогает в идентификации бактерий без ДНК-тестирования.
Результаты идентификационных анализов
Все бактерии со всех проб (1–8) — грамотрицательные палочки.
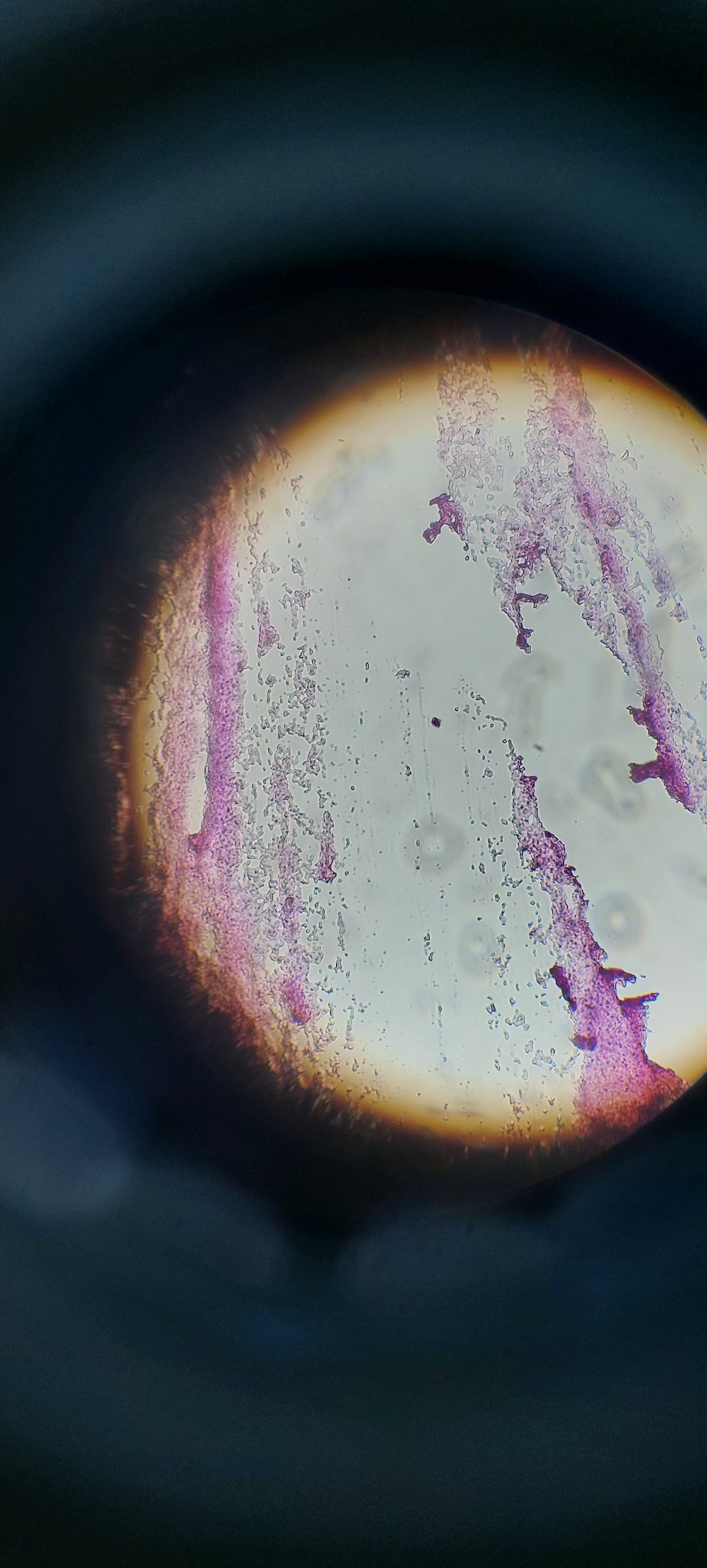
Рисунок 10. Вид под микроскопом.
фото автора статьи
Метод окраски экзоспор по Шеффер-Фултону не дал результат только на 8 пробе.
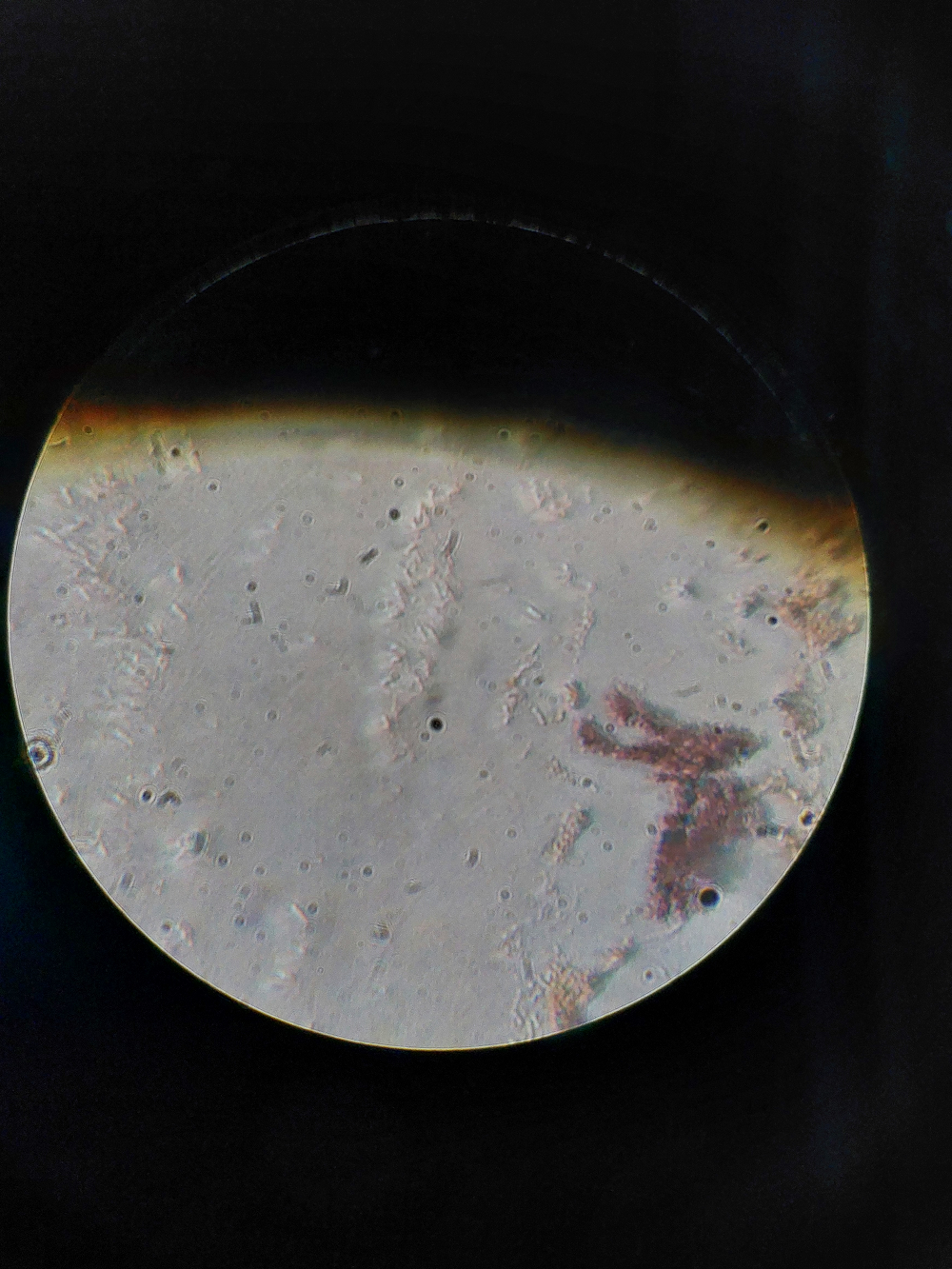
Рисунок 11. Окрашенные розовым — вегетативные клетки, зеленые вкрапления — экзоспоры.
фото автора статьи
Выживаемость в метаноле показывает, что бактериям не причиняет никакого вреда этот спирт, а развитие колоний в метаноле говорит о том, что микроорганизмы используют его для питания.
Пробы от 1 до 8 показали результаты выживаемости при разных показателях метанола:
- 0,5% от объема среды,
- покрытие 500 мкл на бактериальный пересев в чашках Петри,
- бактериальный пересев на 500 мкл метанола на твердый агар в чашках Петри.
Выживаемость в этаноле отсутствует, что говорит о том, что бактерии не способны использовать этанол в питании или противостоять этанолу. Культуры смываются этанолом с поверхности агара, при пересадке на агар с 100 мкл этанола — не развиваются, высыхают.
Рисунок 12. Белое пятно на пробирке, выделенное с 1 из проб ДНК.
фото автора статьи
Выделить ДНК на текущий момент получилось из проб 2.1.1.2 и 4.1. Проверка выделенных образцов на Qubit 2.0 Fluometer (прибор для количественного определения ДНК и РНК в пробе) показала следующее количество материала:
- 4.2 /2 — 200 ng/ml, 40ng/ul
- 4.1 /1 — 235 ng/ml, 47 ng/ul
- 2.1.1.1/ 2 — 93,6 ng/ml , 18,7 ng/ul
- 2.1.1.1/ 1 — >600, green rfu 46001,49
- Пустой — 3 ng/m
Рисунок 13. 2.1.1.1/ 2 — 93,6 ng/ml , 18,7 ng/ul.
фото автора статьи
Чтобы убедиться, что ДНК была выделена именно с метанотрофной бактерии, и определить наличие гена pmoa, свойственного метанотрофным бактериям, использовались пары праймеров для реакции ПЦР:
- a189f и a682r
- cmo182-f и cmo568-r
И, увы, но они не дали вообще никакого результата.
Особенности исследования
До меня при указанной выше среде многие исследователи могли, как минимум, поддержать жизнь в бактериях, а при помощи 2 пар праймеров — доказать, что это те самые бактерии. И если по морфологическим признакам исследование прошло успешно, так как обнаруженные бактерии похожи на представителей метанотрофов, то ПЦР-тестирование не дало результата совсем.
Вполне возможно, что дело во мне, и я при ПЦР-тестировании, например, допустила контаминации с микроорганизмами, которые питаются данными бактериями, это вполне возможно, ведь данный проект выполнялся мной в рамках обучения, и я — неопытный исследователь бактерий. И именно поэтому я приняла решение участвовать в данном конкурсе, вдруг именно вы занимаетесь такими исследованиями и готовы к сотрудничеству, обмену мнениями и готовы дать рекомендации?
Благодарю за внимание!
Литература
- Вершинский А. П. (2024). Система фильтрации воздуха мхом. Юный ученый. 3, 218–221;
- Anuliina Putkinen, Tuula Larmola, Tero Tuomivirta, Henri M. P. Siljanen, Levente Bodrossy, et. al.. (2012). Water Dispersal of Methanotrophic Bacteria Maintains Functional Methane Oxidation in Sphagnum Mosses. Front. Microbio.. 3;
- Попова Н. Н. (2020).Биофлора памятника природы «Кондуки» (Тульская область). Флора и растительность Центрального Черноземья. Материалы межрегиональной научной конференции, 166–168.;
- Абрамочкина Ф.Н., Безрукова Л.В., Кошелев А.В., Гальченко В.Ф., Иванов М.В. (1987). Микробиологическое окисление метана в пресноводных водоемах. Микробиология. 56, 464–471;
- Андреев Л.В., Гальченко В.Ф. (1978). Жирнокислотный состав и идентификация метанотрофных бактерий. Доклады АН СССР. 239, 1465–1468;
- Андреев Л.В., Гальченко В.Ф. (1983). Идентификация метатрофных популяций методом газовой хроматографии. Тезисы докл.конф. Хроматография в биологии и медицине. 39–40;
- Андреев Л.В., Троценко Ю.А., Гальченко В.Ф. (1977). Жирнокислотный состав метилотрофных бактерий. Тезисы докл.междунар.симпоз. 14–16;
- Безрукова Л.В., Николенко Ю.И., Нестеров А.И., Гальченко В.Ф., Иванов М.В. (1983). Сравнительный серологический анализ метанотрофных бактерий. Микробиология. 52, 800–805;
- Беляев А.С., Черных Н.А., Гальченко В.Ф., Иванов М.В. (1995). Детекция метилотрофов в природных образцах методом амплификации фрагмента moxF-гена. Микробиология. 64, 788–791;
- Гальченко В.Ф., Сузина Н.Е. (1977). Особенности строения мембранного аппарата метанотрофных бактерий. Тезисы докл. междунар.симпоз. 2–14;
- Гальченко В.Ф, Большиянов Д.Ю, Черных Н.А, Андерсен В. (1995). Бактериальнын процессы фотосинтеза и темновой ассимиляции углекислоты озерах Оазиса Бангер Хилле, Восточная Антарктида. Микробиология. 64, 833–844.