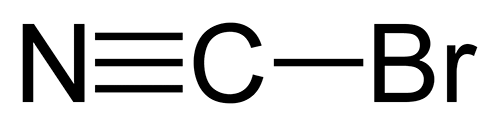Являются ли ксенобиотики ксенобиотиками? Одна из сторон разнообразия природных соединений
21 августа 2018
Являются ли ксенобиотики ксенобиотиками? Одна из сторон разнообразия природных соединений
- 2982
- 2
- 4
На этой невообразимо сложной схеме изображен метаболом одного-единственного вида — человека. А таких видов на нашей планете миллионы! Рисунок в полном размере.
сайт stomfaq.ru
-
Автор
-
Редактор
Статья на конкурс «био/мол/текст»: В предыдущей статье я ставил задачу осветить возможности биодеградации неприродных веществ, производимых человеком. В этой работе приведу ряд примеров выработки самими живыми организмами веществ, традиционно считающихся чуждыми живой природе. Это расширяет представления о возможностях биосферы и открывает фундамент, на котором стоит биодеградация.
Конкурс «био/мол/текст»-2018
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2018.

Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

Спонсором приза зрительских симпатий выступил медико-генетический центр Genotek.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Загадочный инцидент
19 февраля 1994 года в больницу г. Риверсайд (Калифорния) доставили 31-летнюю пациентку Глорию Рамирез, у которой диагностировали терминальную стадию рака шейки матки. Молодая женщина умерла в больнице. Случай печальный, но для опытного персонала достаточно рядовой. Однако то, что произошло дальше, никак нельзя назвать рядовым случаем. Медперсонал обратил внимание на странный чесночный запах, исходивший от тела. Более того, у контактировавших с ним врачей появились симптомы отравления! Эта история получила огласку в газетах, журналисты дали Глории прозвище «токсичная леди». Но разобраться в причинах до конца никто не смог.
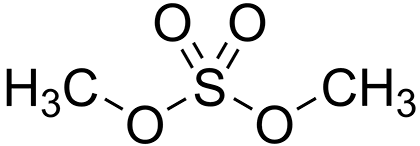
Рисунок 1. Диметилсульфат.
здесь и далее для формул «Википедия»
Впоследствии врачи обратили внимание на сходство симптоматики с отравлением диметилсульфатом. Диметилсульфат — сложный эфир метилового спирта и серной кислоты (рис. 1). Как очень сильный метилирующий агент используется в химии, чрезвычайно токсичен. При попадании на кожу вызывает раздражение и язвы. Сильный мутаген и канцероген. Известно, что биологическое метилирование ДНК играет колоссальную роль в регуляции генома, поэтому любой метилирующий агент, попадающий в организм, должен эту самую регуляцию нарушать. Но откуда он оказался в организме несчастной Глории? Об этом инциденте опубликовали статью в журнале Forensic Science International. В ней высказали очень смелое предположение о том, что диметилсульфат образовался в организме женщины в результате эндогенного окисления безобидного растворителя диметилсульфоксида (ДМСО, димексид), используемого в составе кремов, а также в качестве криопротектора в медицине [1]. Известно, что ДМСО в человеческом организме окисляется, превращаясь в диметилсульфон. Некоторые бактерии окисляют диметилсульфон дальше, но диметилсульфат предусмотрительно не образуют. Авторы статьи утверждали, что в организме Глории окисление пошло именно по пути образования летального метаболита.
Лично у меня эта история вызывает большие сомнения. В самом деле, ДМСО известен как один из самых нетоксичных растворителей — этим-то и объясняется его широкое применение в медицине и косметологии. К превращению в опасный диметилсульфат он совсем не склонен. Наверняка смерть Глории Рамирез произошла по другой причине, нежели описанной в [1]. Но на этот случай следует посмотреть и с другой стороны. Метаболизм каждого человека индивидуален. И, может быть, случилось так, что Глория оказалась единственным человеком на миллиард, для которой ДМСО противопоказан. Никто ведь не проверяет действие препаратов на миллиарде человек!
Для нас же важно другое. Если бы версия с эндогенным образованием диметилсульфата подтвердилась, то это крайне опасное вещество можно было бы отнести к числу природных, пусть даже в роли летального метаболита.
Дело в том, что ДМСО не только широко применяется человеком. Он еще и в несметных количествах образуется в воде морей и океанов в результате жизнедеятельности водорослей [2] (рис. 2). Именно предшественник ДМСО, летучий ДМС (диметилсульфид) обладает характерным «запахом моря». Следовательно, любой метаболит ДМСО тоже является природным веществом.
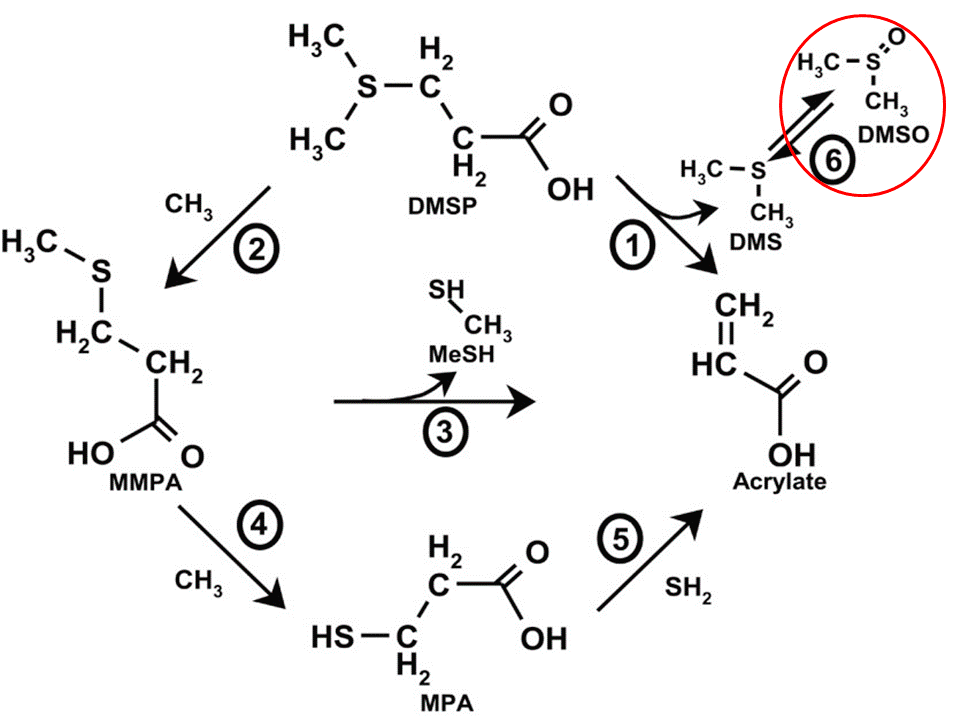
Рисунок 2. Биосинтез ДМСО динофлагеллятами из рода Pfiesteria и бактериями Roseobacter spp. Следует обратить внимание на то, что помимо ДМСО продуцируется еще одно вещество, больше ассоциирующееся с промышленностью, чем с живой природой, — акриловая кислота, мономер полиакрилатов.
[2], рисунок с изменениями
Искусственное или натуральное?
Изучением природных соединений занято множество научных коллективов во всем мире. Для этой цели внедряют изощренные методы анализа. Результаты исследований тоже впечатляют — на основе природных веществ создают лекарства, пестициды, биоразлагаемые пластики, косметику и другие необходимые предметы.
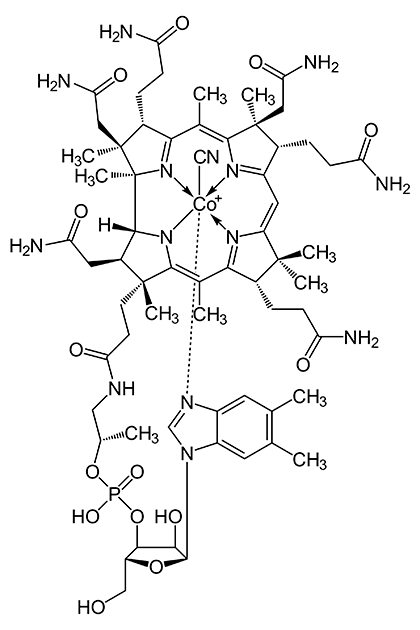
Рисунок 3. В представлении большинства химиков природные вещества, постоянно фигурирующие на страницах учебников биохимии, — это соединения невообразимо сложных структур и зачастую с непроизносимыми названиями. Витамин В12 (кобаламин) — типичное природное вещество, одна из самых сложных мономерных молекул [4]. Сложность строения, наличие оптической изомерии и определенных групп в молекуле (тетрапиррольный цикл, сахар) служат базовыми отличиями биоорганического соединения от органических, традиционно производимых из нефти, угля и природного газа.
Тем не менее, знакомясь с трудами по химии природных веществ, невольно замечаешь, что исследования эти посвящены поиску отличий природной химии (биохимии, биоорганической и бионеорганической химии) от классических органической и неорганической, исследующих продукты переработки полезных ископаемых. Как правило, делают акцент на сложности природных структур (высокой молекулярной массе, оптической изомерии) и трудности их препаративного синтеза. Выдающийся американский химик, лауреат Нобелевской премии Роберт Вудворд [3] синтезировал хлорофилл и кобаламин (рис. 3) [4] исключительно для демонстрации могущества науки — никакого практического значения эти блестящие синтезы не имели.
Изначально органическая химия (как следует из самого названия этой дисциплины) занималась изучением веществ из живых организмов. В ХХ веке, по мере роста добычи полезных ископаемых, акцент стал смещаться. Органическая химия стала изучать нефть, природный газ, горючие сланцы, уголь, а также бесчисленные продукты их переработки. Причина этого проста — большинство органических веществ рентабельнее получать из нефти и природного газа, чем, например, из растений. В результате дисциплине, изучающей вещества биологического происхождения, дали несколько тяжеловесное наименование «биоорганическая химия».
Сейчас между органической и биоорганической химией создан некий барьер — утверждение, что большинство полученных химиками веществ не встречается в природе. Речь в первую очередь идет о простейших органических веществах, большинство из которых обладает высокой токсичностью. Собственно говоря, само определение «ксенобиотик» пришло оттуда, в переводе с древнегреческого оно означает «чуждый жизни».
Биологический энциклопедический словарь дает ксенобиотикам такое определение [5]:
- Ксенобитики
- (от греч. xenos — чужой и biotos — жизнь) чужеродные для организмов соединения — пестициды, препараты бытовой химии, лекарственные средства и тому подобное.
Барьер подкрепляется общественным сознанием, постоянно разграничивающим «натуральное» и «искусственное». Особенно крепок барьер в отношении химии. Мой коллега, тоже популяризирующий науку, Аркадий Искандерович Курамшин много пишет и говорит на тему хемофобии — страха общественности перед химическими веществами. И барьер этот во многом препятствует внедрению биодеградации: слишком прочно укоренилось мнение, что биосфера не способна перерабатывать продукты химической промышленности, потому что она с ними незнакома. Приведенными ниже примерами попытаемся доказать, что это не так.
На самом деле, живые организмы, и в первую очередь микробы, сами способны синтезировать токсичные вещества, не так давно считавшиеся несуществующими в природе (рис. 4). Конкретных примеров можно привести множество. Постараюсь выбрать самые показательные.

Рисунок 4. Живая природа — кладезь разнообразных веществ. Особенно в тропиках.
И такое есть в природе
В предыдущей статье «Биодеградация ксенобиотиков как самозащита природы» [6] я рассказывал про биодеградацию боевого отравляющего вещества иприта (ди-β-хлорэтилсульфида). Это страшное вещество (наверное, к счастью) в природе не найдено. Тем не менее растворитель и сырье в производстве винилхлорида — 1,2-дихлорэтан, — структура которого имеет отдаленное сходство с ипритом, тоже очень токсичен. Для него характерны выраженные канцерогенные свойства. И токсичность эта, помимо прочего, связана с метаболизмом дихлорэтана и других дигалоэтанов. В организме млекопитающих происходит ферментативное замещение одного из атомов галогена на сульфгидрильную группу глутатиона — трипептида, обусловливающего окислительно-восстановительный потенциал внутренней среды организма. В результате образуются производные глутатиона, имеющие структуру —S—CH2—CH2—Hal, что, фактически, половина молекулы иприта (рис. 5)! Они так и называются — «полуиприты» (half yperite, half mustard) [7]. Свойства этих веществ сходны со свойствами иприта. Они являются алкилирующими агентами, сшивают молекулы ДНК и белков. Следует указать на то, что один из представителей 1,2-дигалоэтанов, 1,2-дибромэтан (рис. 6), является метаболитом арктических водорослей [8]!
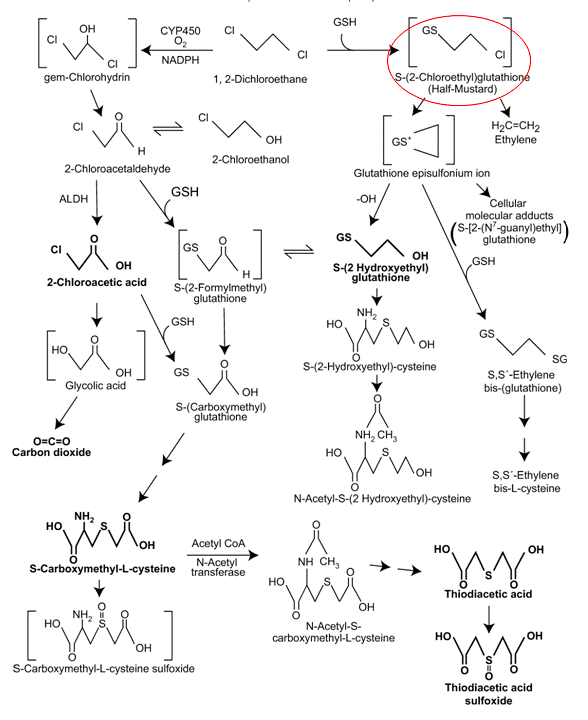
Рисунок 5. Метаболизм 1,2-дигалоэтанов сопровождается образованием ипритов!
[7], рисунок с изменениями
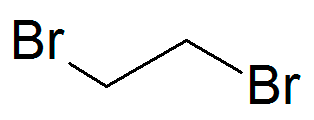
Рисунок 6. 1,2-Дибромэтан — метаболит водорослей и фумигант для пропитки древесины
Следовательно, образующийся из него полуиприт β-бромэтилсульфид тоже можно отнести к природным соединениям.
Азид натрия — известный консервант. Правда, не пищевой! Действие азида сходно с действием цианидов, описанным в [6]. Но азид (состоящий из трех атомов азота анион азотистоводородной кислоты, HN3) еще токсичнее. Азотистоводородная кислота и ее соли — не только ядовитые, но и взрывчатые вещества. Некоторые из них применяют в качестве детонаторов. Упомянутый выше азид натрия используют в подушках безопасности автомобилей — при ударе он со взрывом разлагается на газообразный азот, мгновенно заполняющий подушку, и металлический натрий.
![6-азидотетразоло[5,1-a]фталазин 6-азидотетразоло[5,1-a]фталазин](/img/content/2426/07.azidotetrazoloftalazin.png)
Рисунок 7. 6-азидотетразоло[5,1-a]фталазин — метаболит динофлагелляты Gymnodinium breve.
сайт chemspider.com
Конечно, очень нелегко представить азиды в качестве природных веществ. Тем не менее одноклеточная водоросль Gymnodinium breve, относящаяся к группе динофлагеллят и известная своей чрезвычайной ядовитостью, продуцирует метаболит экстраординарной химической структуры с мудреным названием 6-азидотетразоло[5,1-a]фталазин (рис. 7) [9].
Эта молекула, пожалуй, бьет рекорд среди природных соединений по числу атомов азота — их в ней восемь, причем они собраны в цепочки по три (собственно, азидная группа) и пять (!) атомов, что опять-таки нехарактерно для биологических молекул. Наверное, нет другой биологической молекулы, содержащей тетразоловый цикл. К сожалению, о свойствах азидотетразолофталазина сообщается очень мало. Но, судя по структуре, вещество должно обладать всеми свойствами азидов, то есть быть ядовитым и очень термодинамически неустойчивым, склонным возгораться и взрываться. Следует добавить, что, будучи открытым в восьмидесятые годы, азидотетразолофталазин до сих пор остается единственным известным природным соединением, содержащим азидную группу (рис. 1). Аминокислота L-β-азидоаланин не в счет — она образуется из поступающего в организм неорганического азида, то есть, является «полуприродным» веществом. По всей видимости, эволюция всеми силами избегает закреплять метаболические пути, ведущие к таким молекулам, как азиды. Но и в этом правиле, как в любом другом, возникло исключение, и оно демонстрирует возможности метаболизма в живой клетке.
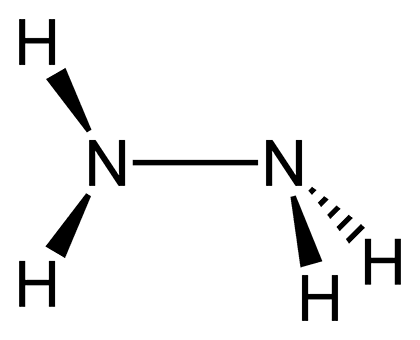
Компонент ракетного топлива и сырье в производстве фунгицидов, гидразин (рис. 8а) по токсическим свойствам не уступает азиду и относится к веществам первого класса опасности. Он также пожаро- и взрывоопасен, оставляет ожоги на коже (рис. 8б).
Так вот, морская бактерия Brocadia anammoxidans [10] является единственным известным живым организмом, вырабатывающим гидразин! Он образуется как полупродукт анаэробного окисления аммиака (так называемого анаммокс-процесса ), в специальных органеллах, именуемых анаммоксосомами (рис. 9). Конечно, гидразина бактерия выделяет мало, и промышленным его источником станет вряд ли. Но зато брокадия и ей подобные микроорганизмы получают другое применение — они очищают сточные воды от аммиака и нитратов.
Об этом метаболическом пути можно прочитать в статье «Аммонийный датчик анаммокс-бактерии» [11].
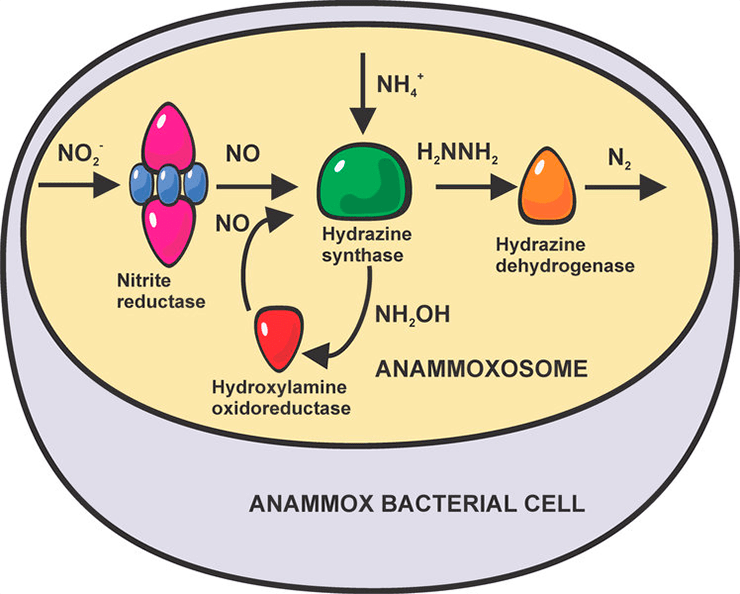
Рисунок 9. Анаэробное окисление аммония нитритом до молекулярного азота. Промежуточным продуктом является гидразин.
Про несимметричный диметилгидразин (гептил) вкратце уже рассказывалось в статье [6]. Он еще токсичнее, чем незамещенный гидразин. Я был чрезвычайно изумлен, когда узнал, что гептил образуется при аэробной биодеградации взрывчатого вещества нитрата триметиламмония. Этот метаболический путь представлен в замечательном обзоре [12], посвященном как раз биодеградации взрывчатых веществ. Это само по себе поразительно. Но попробуем порассуждать далее.
Нитрат триметиламмония — это соль. И, подобно любой соли, она состоит из основания и кислотного остатка. В данном случае, это триметиламин и нитрат (остаток азотной кислоты). Любопытно, что оба компонента являются продуктами жизнедеятельности бактерий, их азотного обмена! Таким образом, чрезвычайно токсичный компонент ракетного топлива (рис. 10) условно тоже можно считать природным веществом! Конечно, трудно себе представить, чтобы где-то в природе скопилось большое количество нитрата триметиламмония. То есть гептил (опять же к счастью для всего живого!) не может образоваться естественным путем в сколько-нибудь заметных количествах. В лучшем случае, на уровне нескольких молекул. Но, с точки зрения химика, даже одна молекула означает присутствие вещества.

Рисунок 10. Несимметричный диметилгидразин является компонентом большинства видов жидкого ракетного топлива.
сайт wall.alphacoders.com
О диоксинах говорят и пишут много. Точнее, о полихлордибенздиоксинах — именно их имеют в виду под словом «диоксин». В статье [6] рассказывалось о «нехороших» полиароматических углеводородах, образующихся в результате неполного сгорания органики. Диоксины (рис. 11а) также образуются при сжигании поливинилхлорида, резины, любой органики, содержащей галогены. Их химическое строение и свойства (наличие плоских ароматических колец, чрезвычайно высокая стабильность, растворимость в липидах) очень сходны со строением и свойствами полиароматики. И токсические свойства похожи тоже. Канцерогены, иммунодепрессанты, мутагены и тератогены, их токсичность на три порядка выше, чем у зарина (10−6 г/кг живого веса!). Чрезвычайно стабильны в окружающей среде. Галогенированные дибенздиоксины до недавнего времени считались смертельными для любых форм жизни. В устах экологов диоксины — любимая страшилка, и надо признать, небезосновательная. Именно их образованием в результате неполного сгорания определяется опасность для окружающей среды поливинилхлорида — одной из самых широко используемых пластмасс, в остальном совершенно неядовитой.
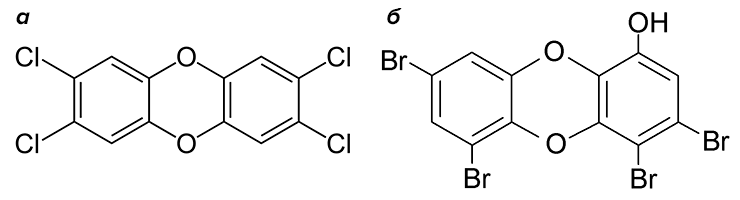
Рисунок 11. Оказывается, даже такие страшные загрязнители, как галогенированные дибензодиоксины, вырабатываются живыми организмами! а — 2,3,7,8-тетрахлордибензо-пара-диоксин, образующийся при неполном сгорании ПВХ. б — спонгиадиоксин А, один из природных диоксинов.
Как оказалось, изомерные гидрокситетрабромодибензо[1,4]диоксины и гидрокситрибромодибензо[1,4]-диоксины (рис. 11б) вырабатывают морские губки Dysidea dendyi (рис. 12) [13]. Они получили наименование «спонгиадиоксины», то есть «диоксины из губок». Подобно антропогенным диоксинам, спонгиадиоксины очень ядовиты, обладают цитотоксичностью и рассматриваются в качестве потенциальных агентов для химиотерапии рака. Это подстегивает интерес к их изучению. Для нас же главное, что Природа «научилась» создавать вещества этого класса задолго до человеческой цивилизации.

Рисунок 12. Морская губка Dysidea dendyi
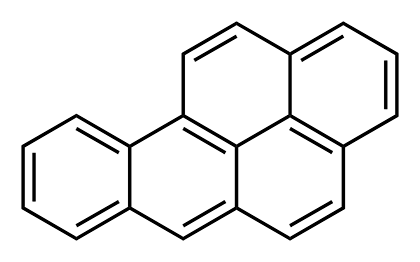
Рисунок 13. Бензпирен
Про бензпирен в статье [6] уже рассказывалось. Это мутаген и канцероген, вещество первого класса опасности (рис. 13). Благодаря высокой устойчивости аккумулируется в организме, передается по пищевой цепи. Именно поэтому бензпирен, наряду с диоксинами, чаще всех других химических веществ упоминается экологами.
Тем не менее актиномицет Streptomyces lavendulae (штамм Tü 1668) вырабатывает антибиотик с говорящим названием — бензпиреномицин, являющийся производным бензпирена [14] (рис. 14). Подобно спонгиадиоксинам, бензпиреномицин обладает цитотоксичностью. Воистину, возможности метаболических путей живых организмов поражают !
Вообще, актиномицеты это очень интересная группа бактерий, о чем рассказывается в статье «„Зеленые“ революционеры» [15].
В статье «Роль слабых взаимодействий в биополимерах» [16] я уже рассказывал про супермутагены 5-галоурацилы, способные встраиваться в ДНК, и механизм их действия. Так вот, коллектив авторов из Китая выделил сам 5-фторурацил и ряд его производных из губки Phakellia fusca (рис. 15) [17]!

Рисунок 15. Кто бы мог подумать, что 5-галоурацилы, используемые для увеличения числа мутаций в научных исследованиях и селекционных работах, тоже встречаются в природе? На фотографии — губка из рода факеллия. Вверху слева: 5-фторурацил — супермутаген!
сайт tolweb.org
Самый простой гормон
Этилен (этен), С2Н4, считается самым востребованным органическим веществом, производимым промышленностью. В год в мире производится более ста миллионов тонн этилена. И эта цифра растет! Дело в том, что этилен является очень важным сырьем, из которого производят полиэтилен, дихлорэтан, технический этиловый спирт и целый ряд других ценных продуктов. Еще не так давно этилен применяли для медицинского наркоза. Потребность в этилене настолько велика, что к химическим предприятиям подводят специальные трубы — этиленопроводы, — по которым этот газ подается под давлением.
Но этилен — не только продукт переработки природного газа. Еще это, пожалуй, самая простая молекула, обладающая гормональным действием. Практически все растения, начиная с зеленых водорослей и заканчивая самыми высокоорганизованными цветковыми, вырабатывают этилен в качестве фитогормона (рис. 16). Этилен — газ, соединение очень летучее, поэтому он является своеобразным средством общения среди растений. Благодаря ему растения синхронно зацветают и синхронно же приносят плоды. Растение, объедаемое гусеницами, может «сообщить» соседям, чтобы они выделяли больше токсинов: поврежденный лист или плод продуцирует этилена больше, чем здоровый. Этилен стимулирует рост проростков и цветение, созревание плодов и опадение листьев осенью. Как и любой гормон, этилен в тканях растения воздействует на рецепторы и запускает каскад передачи сигнала, приводящий к активации одних генов и инактивации других.

Рисунок 16. Все зеленые растения выделяют в атмосферу этилен. Особенно с приходом осени, с началом опадения листьев.
сайт giphy.com
В XIX веке, когда уличные фонари были не электрическими, а газовыми, подметили, что ветки деревьев вблизи таких фонарей неестественно скручиваются, а плоды созревают быстрее. Так и было обнаружено гормональное действие этилена — ведь он содержится как примесь в природном газе. В настоящее время в теплицах и овощехранилищах в воздух специально подмешивают этилен, чтобы ускорить цветение и созревание. Хотя это увеличивает пожароопасность таких помещений (этилен — газ горючий!), но все равно рентабельно.
В растениях этилен производится метаболическим циклом Янга (рис. 17) [18]. Кроме растений, продуцентами этилена являются бактерии и грибы.
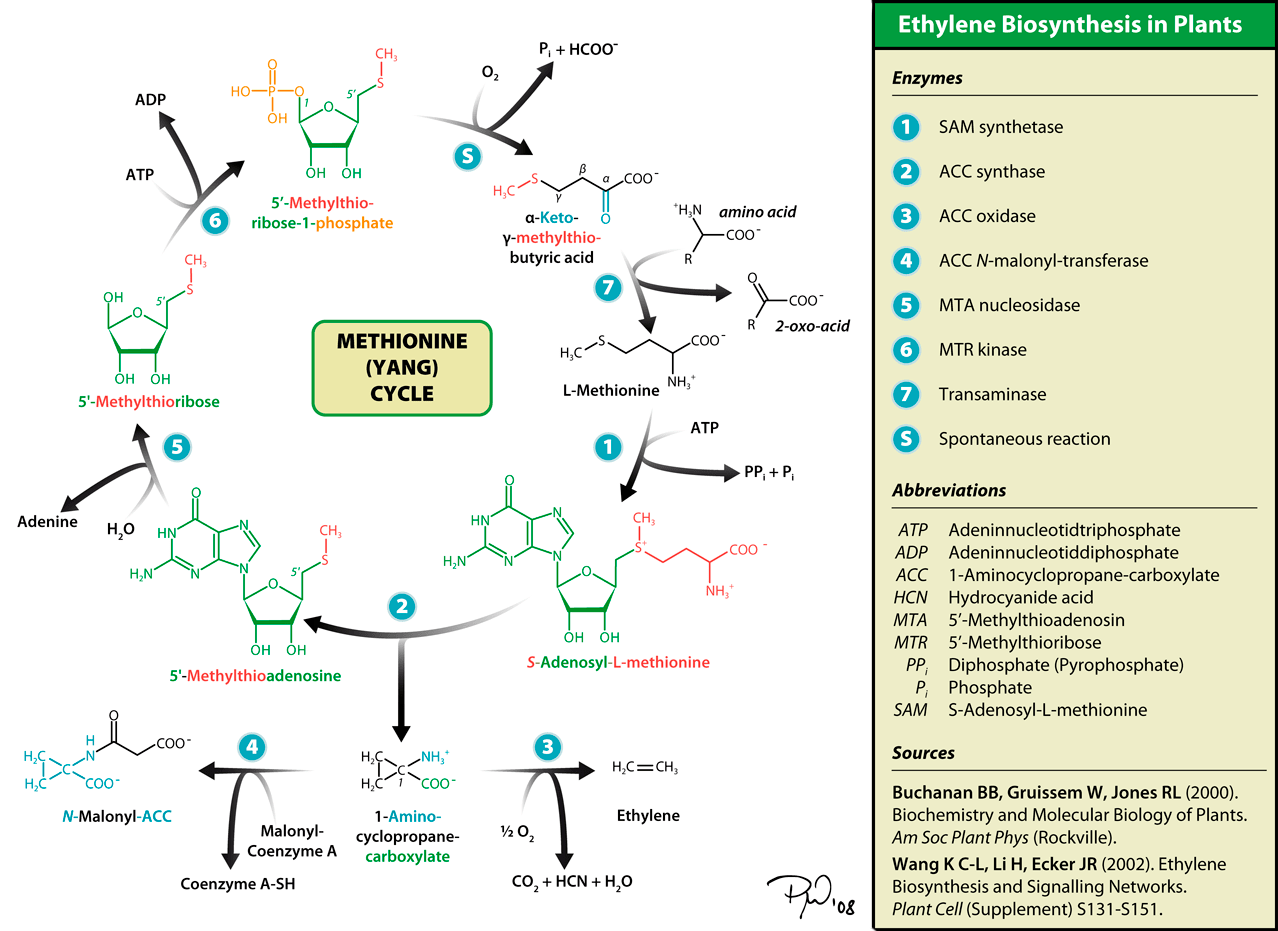
Рисунок 17. Цикл Янга — биосинтез этилена растениями
Однако, рассказывая про этилен, я не упомянул еще один важный технологический продукт его переработки — окись этилена (рис. 18). В промышленности это вещество получают, окисляя этилен кислородом в присутствии катализатора — тонкодисперсного серебра. Этиленоксид является газообразным веществом, и отличительная особенность этого соединения — высокая химическая активность. Окись этилена огнеопасна и взрывоопасна, смесь с воздухом чрезвычайно легко детонирует. Теплота сгорания этого вещества очень высокая. Вещество ядовито: раздражает кожу и слизистые оболочки, подавляет центральную нервную систему, обладает выраженным мутагенным и канцерогенным действием. Сильный бактерицид: используется для газовой стерилизации, например, шприцев. Относится ко второму классу опасности, то есть является высокоопасным веществом. Чрезвычайно химически активно, вступает в многообразные реакции. Легко димеризуется и полимеризуется, продуктами являются, соответственно, растворитель диоксан и полимер полиэтиленгликоль.
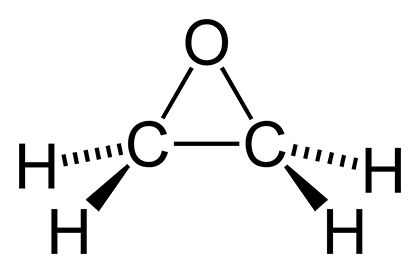
Рисунок 18. Этиленоксид (окись этилена, оксиран)
Свойства этиленоксида определяются строением его молекулы. Она представляет собой трехчленный цикл и имеет вид равностороннего треугольника с острыми углами. Такие значения углов достигаются сильным искривлением и напряжением межатомных связей. Молекула окиси этилена буквально пересыщена энергией. Ее можно уподобить туго скрученному резиновому жгуту, готовому самопроизвольно и с большой силой распрямиться. Этим объясняется высокая склонность окиси этилена к реакциям с раскрытием цикла. Токсичность определяется образованием β-гидроксиэтильных аддуктов с азотистыми основаниями ДНК и аминокислот, как показано на рисунке 19.
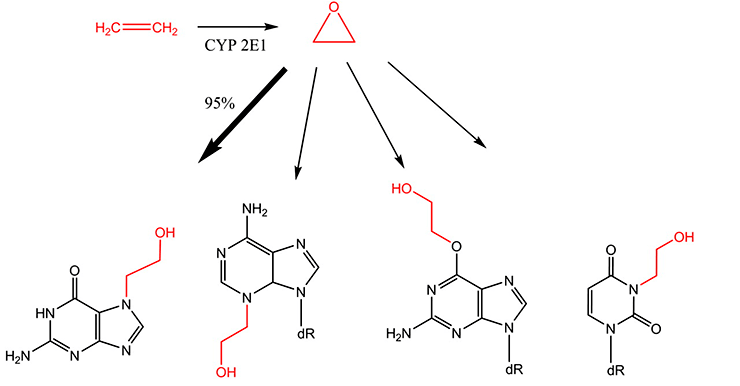
Рисунок 19. Эндогенное превращение этилена в этиленоксид и далее — в аддукты азотистых оснований ДНК.
[19], рисунок с изменениями
Казалось бы, какое отношение окись этилена может иметь к живой природе? Это губительный яд, вот и все. Но вот что интересно. Окись этилена является естественным метаболитом этилена (рис. 19), который благодаря зеленым растениям всегда присутствует в атмосфере [19]. Этилен окисляется ферментом цитохромом P450 2E1 и превращается в искомое соединение. Конечно, этиленоксид никогда не накапливается в организме в токсичных дозах и существует только в виде короткоживущего интермедиата. Микроорганизмы, усваивающие этилен, способны эффективно обезвреживать эндогенный этиленоксид, превращая его в ацетил-КоА. Но для нас с вами важно то, что благодаря постоянному поступлению в организм этилена этиленоксид в очень малых дозах присутствует в организме так же постоянно! То есть является полноценным природным веществом.
Аромат лета
Лето, вне всякого сомнения, замечательное время года. Солнце, жара, пляж... И запах скошенной травы, конечно. Если в давние времена аромат сена прочно ассоциировался с сельской местностью, то в последние годы стали очень уж усердно косить газоны в городах. И мало кто в моменты любования природой задумывается над тем, какие вещества придают этот запах траве. Таких веществ несколько, но главное из них — кумарин (рис. 20). Химическое название — лактон орто-оксикоричной кислоты (вот все любование испортят ученые такими названиями!). Кумарин своим запахом отпугивает насекомых, поэтому растения используют его для защиты. Для человека он практически безвреден, хотя периодически появляется информация о канцерогенном действии кумарина. Широко применяется в парфюмерии в качестве отдушки.

Рисунок 20. Ученые даже аромат сена описали в виде формул. Донник лекарственный Melilótus officinális — один из продуцентов кумарина. Внизу слева — кумарин.
сайт horsedvm.com
Сам-то кумарин безвреден, но при гниении биомассы растений, богатых этим веществом (например, донника (рис. 20), в результате метаболических процессов, запускаемых гнилостной микрофлорой, кумарин окисляется до 4-гидроксикумарина, а затем димеризуется. Образующийся дикумарин — опасный яд. Он блокирует работу витамина К и препятствует свертыванию крови. Животные, поевшие запрелое сено, рискуют умереть от потери крови при малейшей царапине! В середине ХХ века биологическую активность дикумарина тщательно изучили и создали более эффективные антикоагулянты. Например, варфарин (рис. 21а) — продукт конденсации кумарина и бензилиденацетона, — еще более эффективен, чем дикумарин. Он является лекарством от тромбозов и одновременно крысиным ядом — все зависит от дозировки! В отличие от дикумарина, в природе варфарин не найден. Однако его предшественники являются природными веществами — бензилиденацетон, известный антисептик, выделен из энтомопатогенной бактерии Xenorhabdus nematophila [20].
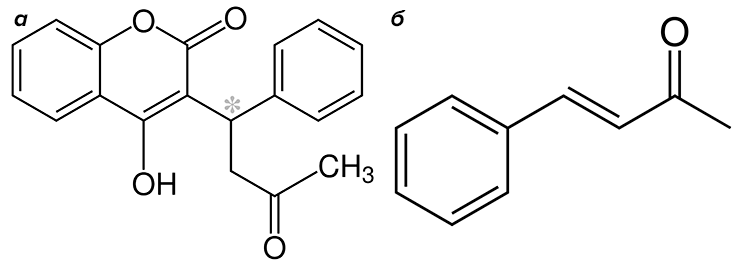
Рисунок 21. Яд для крыс, лекарство от тромбоза и продукт ферментативной реакции в одном лице — варфарин. а — структурная формула варфарина (звездочкой обозначен хиральный атом, определяющий оптическую изомерию молекулы: товарный продукт представляет собой рацемат, то есть смесь двух оптических изомеров). б — бензилиденацетон, известный антисептик и предшественник варфарина.
Крайне любопытной стала работа авторов из Китая, которые получили варфарин конденсацией 4-гидроксикумарина и бензилиденацетона (рис. 21б) при помощи фермента липазы из различных организмов [21]. То есть варфарин можно получить при помощи биологического катализатора — фермента, — из биологических предшественников! Стало быть, условно и варфарин можно считать природным. Более того, можно пофантазировать, что в процессе эволюции какой-нибудь организм «научится» синтезировать варфарин. Или уже научился, просто еще не обнаружен. Скажете, что это просто фантазии? Но ведь все разнообразие вторичных метаболитов в природе возникло вот так — в результате случайных комбинаций генов и кодируемых ими веществ-предшественников.
Конденсацией 4-гидроксикумарина получены новые антикоагулянты, еще более эффективные, чем варфарин — например, родентицид бромадиолон. Кто знает, может быть, и его в скором времени получат ферментативной реакцией?
О самом важном
Каждый из нас наслышан об охватившем человечество энергетическом кризисе. Что поделать, наша цивилизация не может существовать без невозобновляемых энергоносителей. Но наступит время, когда нефть, природный газ и даже каменный уголь иссякнут. И что тогда?! Совершенно правильным решением стал поиск альтернативных источников энергии. Желательно, возобновляемых. Энергию солнца и ветра оставим в покое — нас-то интересует биология. И здесь список тем, посвященных возобновляемой энергетике, весьма обширен. Кто-то рапс предлагает сеять, кто-то — культивировать богатые липидами одноклеточные микроводоросли или получать биогаз из отходов. Одним из достаточно оригинальных решений можно признать микодизель (рис. 22). Название говорит само за себя: этот вид дизельного топлива предлагается добывать из... грибков!

Рисунок 22. Заправка с микодизелем
сайт justdial.com
Произрастающие в Южной Америке грибки Gliocladium roseum и Muscodor albus (рис. 23а) выделяют в окружающую среду смесь летучих компонентов, содержащую, в частности, такие неожиданные для живой природы компоненты как бензол, нафталин и даже [8]-аннулен (рис. 23б и 23в). Американские исследователи предлагают использовать ее в качестве альтернативного топлива — «микодизеля» [22]! Скажу честно: рентабельность получения автомобильного горючего из южноамериканских грибков вызывает большие сомнения. Но исследования микодизеля имеют большой теоретический интерес, поскольку открывают новые, неизведанные ранее стороны биохимии. А как известно, нет ничего практичнее хорошей теории. Может быть, исследования микодизеля лягут в основу производства новых лекарств — кто знает?
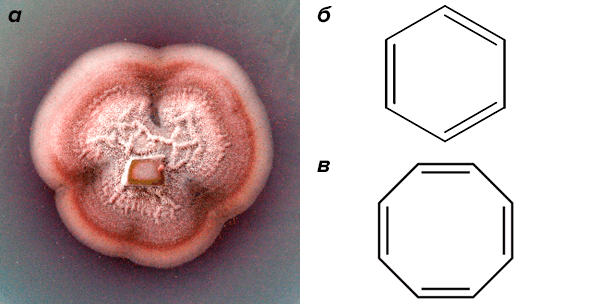
Рисунок 23. Вот оно, возможное решение топливного кризиса. а — грибок Gliocladium roseum, продуцент микодизеля. б — бензол. в — [8]-аннулен.
Чтобы не быть съеденным
Я с самого раннего детства интересовался насекомыми. И как, наверное, любого любителя насекомых меня восхищают приведеньевые — палочники и листовидки. Поразительный пример эволюционной адаптации! Привиденьевые — признанные мастера маскировки, имеющие детальное сходство с веточками и листьями деревьев.
Но не каждый палочник похож на палку. Палочнику Oreophoetes peruana (рис. 24), обитающему в горных лесах перуанских Анд, непросто замаскироваться с его броской окраской. Как же он защищается от хищников? Для этого он из особых желез выбрызгивает в них жидкость, содержащую незамещенный хинолин [23]. Хинолин (рис. 24) — азотистый гетероцикл, сырье химической промышленности, добывается из каменноугольной смолы. Наверное, нет учебника по органической химии для вузов, в котором это вещество не было бы упомянуто как типовое гетероциклическое соединение. Но хинолин имеет и практическое значение как сырье для получения многих красителей. А вот, оказывается, это еще и природный антифидант (вещество, неприятным запахом и вкусом защищающее от поедания).

Рисунок 24. Хинолин можно добывать не только из каменноугольной смолы, но и из... насекомых. Палочник Oreophoetes peruana вооружен химическим оружием, и маскировка ему ни к чему. Вверху слева — хинолин.
сайт hiveminer.com
И снова про алкилирующие агенты
В своих статьях я часто пишу об алкилирующих агентах — веществах, способных к обмену алкильных радикалов. Понятно, почему: попадая в организм, эти соединения алкилируют что попало, нарушая при этом структуру биологических молекул. К ним относятся вещества разных классов, в том числе диазосоединения.
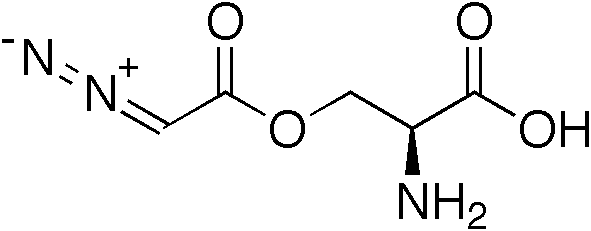
Диазосоединения (диазометан, диазоуксусный эфир — этиловый эфир диазоуксусной кислоты) — алкилирующие агенты, применяемые в органическом синтезе, реакционноспособные, взрывоопасные и токсичные вещества (рис. 25а). При работе с ними требуются повышенные требования к безопасности. К тому же эти реактивы долго не хранятся, и готовить их надо непосредственно перед синтезом.
Удивительно, но вещество, имеющее большое сходство с диазоуксусным эфиром, есть в природе. Антибиотик азасерин (рис. 25б), продуцируемый культурами Streptomyces fragilis, представляет собой сложный эфир диазоуксусной кислоты и аминокислоты L-серина [24].
Будучи, как и все диазосоединения, цитотоксичным веществом, азасерин рассматривается в качестве противоопухолевого агента. Кстати, в организме азасерин метаболизирует с образованием диазометана, который таким образом тоже можно причислить к природным веществам!
Новое о старом
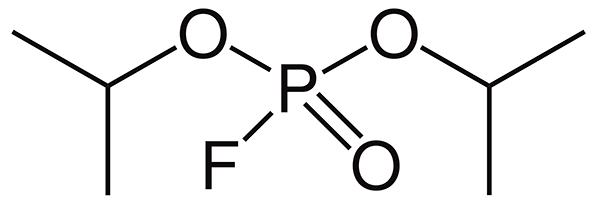
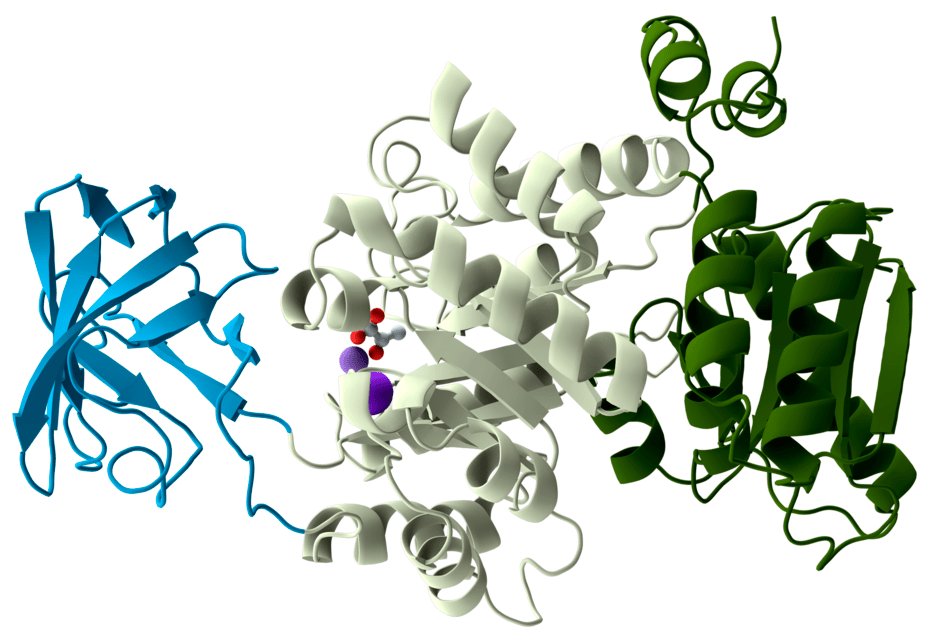
В статье [6] я уже говорил о фосфорорганических ядах. А началась их история с вещества под названием «диизопропилфторфосфат» (ДФФ) (рис. 26а). Его впервые синтезировали в гитлеровской Германии в 1938 году, и какое-то время рассматривали в качестве боевого отравляющего вещества. ДФФ имеет приятный запах цветущей яблони, но наслаждаться его ароматом не стóит: как все родственные соединения, он чрезвычайно токсичен. ДФФ, строго говоря, не является фосфорорганическим веществом: связи фосфор—углерод в нем нет. По этой причине токсичность его все-таки ниже, чем у синтезированных позже (все теми же немцами) табуна и зарина: будучи сложным эфиром, ДФФ гидролизуется и обезвреживается. ДФФ применяли и в качестве инсектицида, а сейчас данное вещество имеет научное значение как эталонный ингибитор холинэстераз.
ДФФ является эфиром изопропилового спирта и фторофосфорной кислоты. Фторофосфорная кислота — сильная двухосновная кислота, ряд свойств которой сближает ее с серной кислотой. В природе (по крайней мере, в живой) она не найдена. Но в старенькой (1967 года) статье, опубликованной коллективом авторов из университета штата Пенсильвания [25], сообщен любопытный факт. Объектом исследования авторов был фермент пируваткиназа (рис. 26б) мышц кролика. Фосфорилирование пировиноградной кислоты — фундамент, на котором держится вся биохимия. Метаболизм без этой реакции невозможен. Но позвольте, чего нового можно ждать от изученной вдоль и поперек реакции и катализирующего ее фермента?
Оказывается, даже хорошо изученные процессы могут преподносить сюрпризы. Неизвестно, что побудило авторов исследовать активность пируваткиназы при избытке фторид-ионов. Но оказалось, что в этих нестандартных условиях хорошо, казалось бы, известный фермент проявляет активность фторкиназы. То есть фосфорилирует ионы фтора и осуществляет синтез фторфосфата!
В наше время стало модно фантазировать на тему эволюции в будущем, происхождения новых удивительных животных и растений от ныне существующих через миллионы лет. Вот хороший задел. Можно представить себе, что случайно возникшая фторкиназная активность пируваткиназы будет подхвачена отбором, и возникнет новый фермент фторкиназа, для которого синтез фторфосфата будет доминирующим видом активности. И появятся живые организмы, защищающиеся от врагов при помощи ингибиторов холинестераз на основе фторфосфата. Чтобы понять, насколько этот сценарий реалистичен, достаточно вспомнить известное растение дихапеталум из Южной Африки, защищающее себя от поедания при помощи монофторуксусной кислоты, более токсичной, чем цианид!
Из лучших побуждений
Зачастую ядовитые вещества токсичны не сами по себе. Угрозу представляют так называемые «летальные метаболиты». Ферментные системы организма, подобно саперу, совершают непоправимую ошибку. Стремясь обезвредить чужеродное вещество и вывести его из организма (например, окислить и увеличить гидрофильность) они многократно увеличивают его токсичность.
Цианобактерия Aphanizomenon flos-aquae (рис. 27) продуцирует, наряду с целым рядом экзотических азотистых соединений, N,N-диметилформамид (ДМФА) [26]. Это вещество больше известно как широко используемый в промышленности полярный растворитель. Но в организме млекопитающих (в первую очередь, конечно же, людей, работающих с ДМФА на предприятиях) этот растворитель в ряд стадий трансформируется в опаснейшее соединение метилизоцианат (рис. 28) [27]. Это вещество легко вступает в реакции присоединения с образованием N-метилкарбаматов — эфиров метилкарбаминовой кислоты, не существующей в свободном виде. Многие производные метилизоцианата — популярные гербициды, такие как альдикарб, карбарил и ряд других. Собственно, ради производства этих гербицидов метилизоцианат и применяют в промышленности. И именно с его выбросом связана крупнейшая за всю историю техногенная катастрофа в индийском городе Бхопал (рис. 28).

Рисунок 27. Цианобактерия Aphanizomenon flos-aquae
сайт donfactor.com

Рисунок 28. Из самых лучших побуждений наш метаболизм может создать самые страшные вещества. Крупнейшей по числу жертв техногенной катастрофой стала авария на химическом предприятии Union Carbide в индийском городе Бхопал в 1984 г. Внизу слева — метилизоцианат.
сайт pikabu.ru
В этом городе действует химическое предприятие Union Carbide. 3 декабря 1984 года произошло нарушение в системе охлаждения одной из цистерн с метилизоцианатом. Вещество это очень летучее, кипит при 39 °С, и в условиях жаркого тропического климата все закончилось выбросом в атмосферу 42 тонн паров метилизоцианата. И гибелью многих тысяч людей. Об этих событиях сказано и написано много.
На самом деле, никто целенаправленно не исследовал образование метилизоцианата из метаболитов цианобактерий. Изучались только превращения ДМФА, выработанного в промышленном производстве. Здесь речь идет, в первую очередь, про саму возможность образования метилизоцианата из полностью природных источников без привлечения химической промышленности. Пожалуй, на практике это случается очень редко, да и вряд ли, скушав водоросль, можно получить дозировку ее метаболитов, способную вызвать отравление. Но для нас в первую очередь, важно, что потенциальный источник метилизоцианата — ДМФА — выделяется цианобактериями. То есть метилизоцианат и образующиеся из него в организме N-метилкарбаматы тоже являются природными веществами!
Не только о ядах
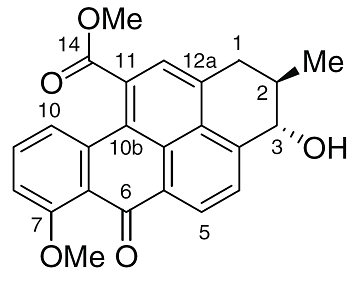
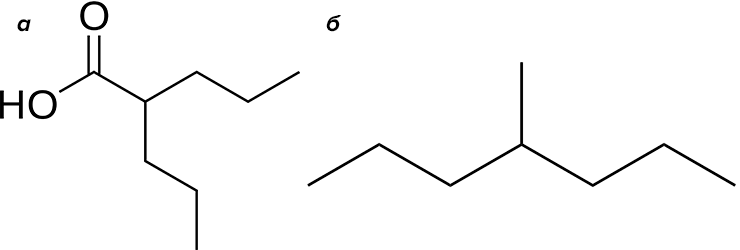
Конечно, не хочется говорить только о ядах. Иногда в организме могут возникать вещества, используемые в медицине. Вальпроевая (ди-н-пропилуксусная) кислота (рис. 29а) является известным противоэпилептическим препаратом. Механизм фармакологического действия вальпроевой кислоты до конца не изучен. Считается, что она ингибирует фермент ГАМК-трансферазу, что приводит к росту концентрации гамма-аминомасляной кислоты, известного и очень важного медиатора центральной нервной системы . Хотя структура этого вещества сходна со структурой природных жирных кислот (например, валериановой: собственно, название «вальпроевая» является сокращением от «пропилвалериановая»), сама вальпроевая кислота в природе не найдена. Тем не менее известно, что жирные кислоты образуются в результате метаболизма углеводородов. Вальпроевая кислота является одним из метаболитов 4-метилгептана (рис. 29а) [28]. 4-метилгептан, в свою очередь, содержится в семенах африканского масляного дерева Butyrospermum parkii L. (рис. 29б) [29]. Растет в Африке к югу от Сахары, известно под названиями «ши» и «карите». Из его семян добывают жирное масло с приятным ореховым вкусом, которое употребляют в пищу и используют в косметических кремах. Так вот, одним из летучих вкусовых компонентов этого, без сомнения, полезного продукта, является тот самый метилгептан, предшественник эндогенной вальпроевой кислоты.
Подробнее об этом важнейшем ферменте и его функциях — в статьях «Спокоен как GABA» [30] и «Эпилепсия, методы ее лечения и роль вальпроевой кислоты в терапии заболевания» [31].
Конечно, вальпроевой кислоты в организме образуется столь мало, что вряд ли можно говорить о каком-либо фармакологическом эффекте масла карите. Скорее, все сказанное имеет чисто теоретический интерес.
А вот если говорить о следующем герое нашего повествования, пиритионе, то его природный источник может иметь большое значение. Комплексное соединение пиритион цинка (рис. 30) впервые получили еще в 1930 году и с тех пор используют в качестве антибактериального и противогрибкового средства для наружного применения. Пиритион цинка является практически обязательной добавкой в шампуни и дезодоранты. Им лечат дерматиты. Кроме того, добавляют в краски для защиты от разрушения плесенью и водорослями. И вот оказалось, что лук стебельчатый Allium stipitatum (рис. 30) среди прочих метаболитов, содержащих серу, выделяет пиритион — лиганд, входящий в состав описываемого биоцида [32].

Рисунок 30. Лук и чеснок — всем известное народное средство от простуды. На фотографии — лук стебельчатый Allium stipitatum. Внизу справа — пиритион цинка.
Всем известны антисептические свойства лука и чеснока. Немалую роль в них играют пиритион и сходные с ним молекулы. Авторы статьи решили пойти еще дальше, и синтезировали аналоги метаболитов лука стебельчатого, которые, возможно, станут новым поколением антимикробных препаратов.
Тайны активных центров
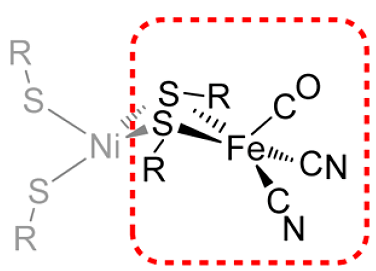
Рисунок 31. Активный центр фермента гидрогеназы представляет собой комплекс железа с угарным газом и цианидом
О том, что цианид и угарный газ — сильные яды, никому говорить не нужно. Это и так все знают. В статье [6] я уже рассказывал о механизме действия этих веществ — они образуют комплексные соединения с металлами в активных центрах белков (гемоглобина, некоторых ферментов), блокируя их работу. Но необходимо отметить, что некоторые микроорганизмы продуцируют цианид и монооксид углерода. Молекулы угарного газа при этом создают комплексы (карбонилы) с никелем и железом в активном центре фермента гидрогеназы, образующей молекулярный водород.
В советское время философы-материалисты популяризировали идею единства и борьбы противоположностей. Пожалуй, приведенный пример можно считать красноречивым примером торжества этой идеи. Активный центр гидрогеназы, включающий в себя угарный газ и цианид (рис. 31), прекрасно работает! Более того, эти лиганды (смертельно опасные во всех других случаях!) необходимы для работы фермента и поддерживают жизнедеятельность бактерий, сбраживающих органические вещества с выделением водорода.
Наверное, гидрогеназа — один из самых поразительных примеров в биохимии.
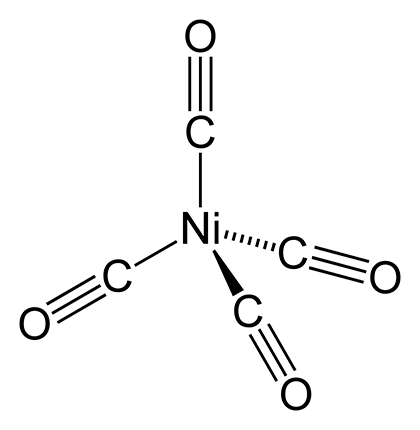
Рисунок 32. Тетракарбонил никеля
Но активные центры ферментов бактерий преподносят и другие сюрпризы. Тетракарбонил никеля (рис. 32), открытый Людвигом Мондом еще в XIX столетии, представляет собой комплексное соединение угарного газа и никеля. Причем никель в этом соединении имеет степень окисления 0, прямо как в куске металла. Это экстремально токсичное вещество, самовозгорающееся и даже взрывающееся на воздухе, а при нагреве разлагающееся с образованием сверхчистого металлического никеля. Токсические свойства тетракарбонилникеля очень похожи на свойства тетраэтилсвинца, о котором рассказывалось в [6]: непосредственное токсическое действие оказывает металл, а лиганды из молекул угарного газа служат «средством доставки». Однако, согласно некоторым данным, очень похожий по строению и свойствам на тетракарбонил никеля комплекс никеля в степени окисления 0 с одной молекулой CO и тремя тиольными группами цистеина образуется в качестве короткоживущего интермедиата в активном центре фермента дегидрогеназы угарного газа, ответственного за усвоение монооксида углерода бактериями [34]. На страничке англоязычной «Википедии» по этому поводу сказано: Although this mechanism is electronically balanced, the idea of a Ni0 species is highly unprecedented in biology («Несмотря на то, что в этом механизме полностью соблюдается баланс электронов, идея об образовании Ni0 является совершенно беспрецедентной для биологии»).
Конечно, оговоримся сразу: формирование карбонила нульвалентного никеля в активном центре фермента — гипотеза, которая может и не подтвердиться. Но если она подтвердится (может быть, при непосредственном участии тех, кто сейчас читает эту статью?), это, безусловно, будет беспрецедентный случай в биологии.
А фермент нитрогеназа, фиксирующий молекулярный азот, как выяснилось совсем недавно (и оказалось научной сенсацией), содержит в активном центре кластер карбида железа — экстремально редкую в живой природе структуру (рис. 33а) [35]. Карбид-анион С4− — это обычный компонент сплавов, катализаторов, сверхтвердых (почти как алмаз) и сверхтугоплавких (смешанный карбид гафния—тантала плавится при 4250 °С!) материалов. Но никто не ожидал встретить его в качестве естественного компонента живого организма. Ученые давно подозревали, что в центре каркаса из атомов железа и серы в составе нитрогеназы прячется легкий атом элемента из второго периода таблицы Менделеева. Думали, что это кислород или азот. А оказался углерод.

Рисунок 33. Карбид анион очень уместно смотрится в каком-нибудь тугоплавком материале. Но, оказывается, он присутствует и в активном центре фермента! а — активный центр нитрогеназы. Черными шариками обозначены атомы углерода, фиолетовыми — железа, желтыми — серы, оранжевый шарик — атом молибдена, синие — азота, красные — кислорода. б — при помощи фермента нитрогеназы бактерии-азотфиксаторы и состоящие с ними в симбиотических отношениях растения семейства бобовых связывают атмосферный азот и превращают его в биологически доступные формы. На фото — лядвенец рогатый в цвету.
Нечестная конкуренция
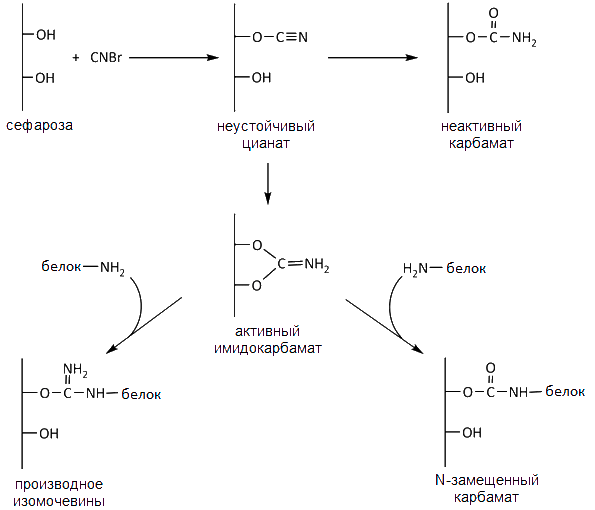
Бромциан — природное вещество! Подумать страшно! Бромциан (рис. 34а) давно применяется в аффинной хроматографии для иммобилизации белков на агарозе, поскольку легко присоединяется к биополимерам (рис. 34б). LD50 перорально бромциана для крыс составляет 25–50 мг/кг. Сильный лакриматор (слезоточивое вещество)! Поэтому работать с ним следует в вытяжном шкафу с соблюдением всех мер предосторожности и иметь под рукой противогаз. К тому же бромциан нестоек и может разлагаться со взрывом. Использовался в Первую мировую войну в качестве боевого отравляющего вещества.
Недавно стало известно, что диатомовые водоросли Nitzschia pellucida (рис. 35) (названные так в честь Фридриха Ницше, между прочим, хотя с токсическими свойствами данной водоросли это никак не связано) выделяют бромциан в качестве крайне токсичного метаболита [36]. А в присутствии избытка йодида они синтезируют еще более токсичный лакриматор йодциан.

Рисунок 35. Диатомовая водоросль Nitzschia pellucida — продуцент бромциана и йодциана
сайт diatomloir.eu
При помощи таких вот радикальных средств водоросли устраняют конкурентов (других диатомовых водорослей) в местах своего произрастания. Кстати, Nitzschia pellucida вдобавок продуцирует 1,2-дихлорэтан — растворитель, основу клеев для пластмасс и предшественник полуиприта!
Для профилактики
Даже такое агрессивное вещество, как молекулярный хлор, тоже выделяется в живых тканях! Хлор, Cl2 (рис. 36), — газ тяжелее воздуха, желто-зеленого цвета, со специфическим резким запахом. Один из самых сильных окислителей. Самый популярный дезинфицирующий агент (в виде водного раствора — хлорной воды). При помощи хлора отбеливают бумагу и ткани, обеззараживают питьевую воду. Очень токсичен, поражает в первую очередь глаза и легкие. Именно с молекулярного хлора началась история отравляющих газов в Первую мировую войну. В 1915 году хлор применили в качестве боевого отравляющего вещества в битве при Ипре.
Тем не менее надо иметь в виду, что токсичен именно молекулярный хлор. А в виде хлорид-аниона Cl− хлор является незаменимым компонентом нашего тела. Суточная потребность человеческого организма в хлорид-ионах составляет целых 4–6 граммов, хлор поступает с пищей в виде поваренной соли — хлорида натрия, присутствующей почти во всех продуктах питания.
К чему я рассказываю эти общеизвестные вещи? Вот сейчас перехожу к тому, что известно не всем. В лизосомах лейкоцитов млекопитающих (в том числе человека!) (рис. 36) присутствует фермент миелопероксидаза, которая окисляет хлорид-ионы до гипохлорита — аниона хлорноватистой кислоты HOCl. Цель этого очевидна: лейкоциты борются с инфекцией, а гипохлориты — это как раз замечательное дезинфицирующее средство. Но гипохлориты обладают высокой химической активностью, являются окислителями. Продуктами их реакций становятся новые дезинфицирующие агенты — например, хлорамины. И молекулярный хлор в том числе! Впрочем, это токсичное вещество в организме не накапливается — молекулы хлора существуют очень непродолжительное время, и само его присутствие выявляется по продуктам реакций присоединения и замещения [37].
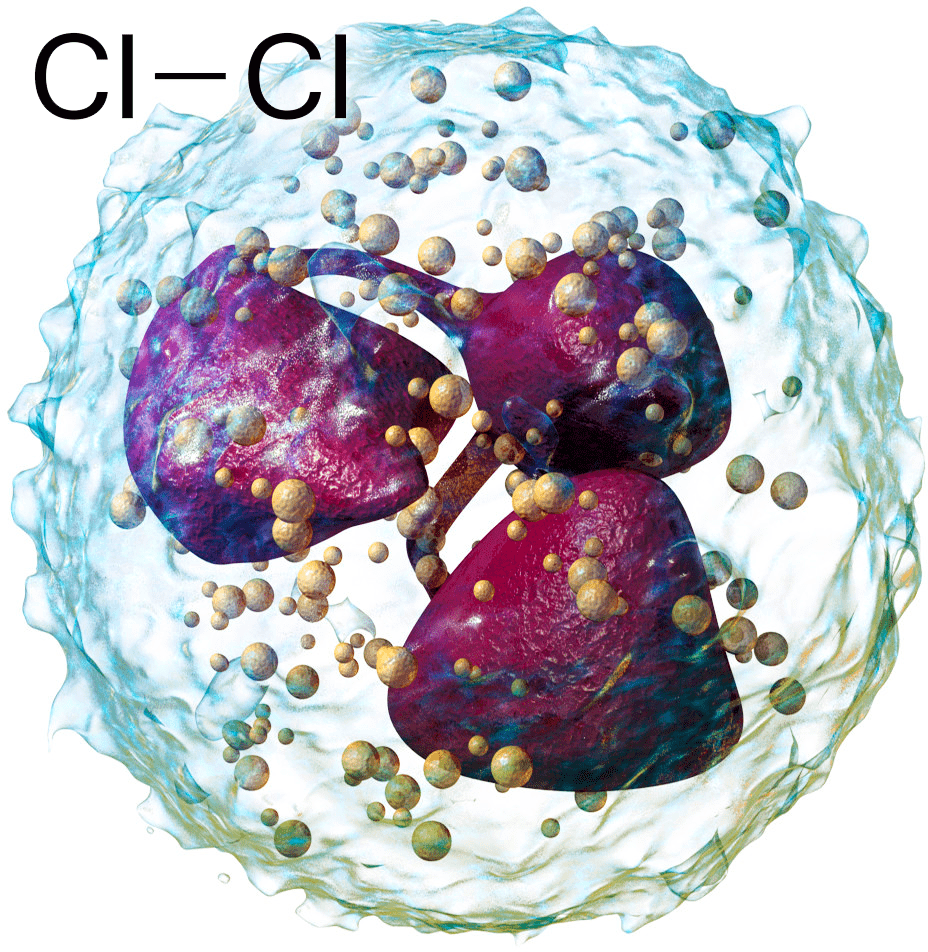
Рисунок 36. Хлор является признанным средством для дезинфекции. Но представить его в организме трудно. На рисунке — нейтрофил с сегментированным ядром: в цитоплазме этой клетки-защитника множество пузырьков лизосом, а в них среди прочего фермент миелопероксидаза. Вверху слева — молекулярный хлор.
сайты leucocitos.org и vectorstock.com (рисунок с изменениями)
Возвращение мышьяка
В статье [6] уже рассказывалось про один из излюбленных «детективных» ядов — цианид. Другим очень популярным средством отравления долгое время являлся мышьяк. Точнее, соли мышьяковой кислоты — арсенаты. Их-то и подсыпали с целью отравить. Арсенаты в организме человека вступают в метаболический путь восстановительного метилирования, конечным продуктом которого становится диметиларсиновая кислота — очень ядовитое вещество. Подобно ранее упоминавшимся фосфорорганическим соединениям, диметиларсинат является ингибитором холинэстераз — ферментов, обеспечивающих нервно-мышечную передачу сигналов. Вообще, мышьяк и фосфор это элементы-аналоги, и ряд их свойств (в том числе токсикологических) очень сходен. Еще у мышьяка есть нехорошее свойство накапливаться (аккумулироваться) в организме. Это облегчает процесс отравления: соединения мышьяка можно добавлять в продукты питания малыми дозами длительное время. Во времена, когда еще не существовало токсикологических экспертиз, это срабатывало — факт убийства было сложно доказать. Человек долго болел, и его смерть списывали на болезнь. В наше время у мышьяка есть вполне мирные сферы применения — из него, например, делают полупроводниковые материалы. Понятно, что с живой природой этот элемент ассоциируется слабо.
Тем не менее известен целый ряд природных веществ, содержащих мышьяк. Я не сильно ошибусь, если назову арсеницин А (рис. 37) самым удивительным из всех природных соединений.
Губка Echinochalina bargibanti (рис. 37), произрастающая в Тихом океане в районе острова Новая Каледония, содержит следовые количества антибиотика арсеницина А — метаболита уникальной структуры, единственного известного природного полиарсенита [38]. Даже один атом мышьяка в биологической молекуле — это удивительно, а в арсеницине — C3H6As4O3 — их четыре!

Рисунок 37. Природные молекулы состоят из углерода, кислорода, водорода и... мышьяка! На фотографии — губка Echinochalina bargibanti. Вверху слева — арсеницин А — пожалуй, самое необычное природное соединение.
Как и положено антибиотику, арсеницин А проявляет сильные бактерицидные и фунгицидные свойства. И кто знает, может быть, все вернется на круги своя. Ведь исторически соединения мышьяка применялись не только как яды, но и как лекарства! Мышьякорганическими препаратами лечили, например, сифилис. Впоследствии мышьяк из медицины был вытеснен более эффективными и менее токсичными препаратами. Возможно, такие соединения, как арсеницин, вновь вернут мышьяк в фармакологию?!
Как промышленность обогащает природную химию
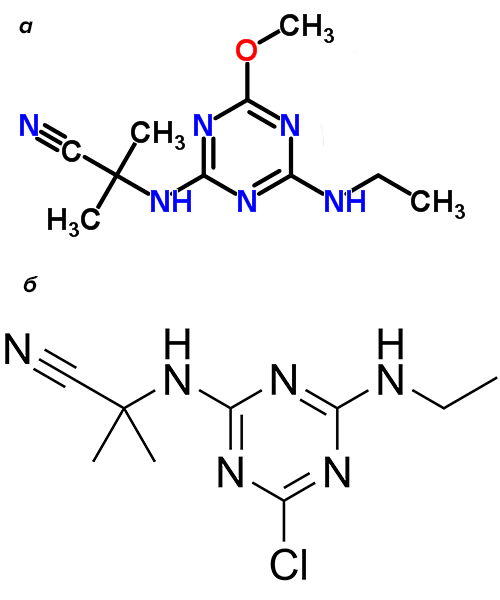
Из растущей в районе Парасельских островов (Южно-Китайское море) водоросли Halimeda xishaensis (рис. 38а) выделили алкалоид, по традиции получивший название, производное от названия источника, — «галимедин» (рис. 38б). Группа китайских исследователей считала это событие большим успехом. Галимедин оказался первым природным веществом, содержащим симметричный триазиновый цикл (симм-триазин). 1,3,5-триазин входит в состав многих гербицидов, таких как упоминавшийся в статье [6] атразин. Стало быть, и живая природа создает такие же молекулы!
Впрочем, триумф вскоре сменился сомнениями. Ряд исследователей обратил внимание на подозрительное структурное сходство вновь открытого алкалоида и гербицида цианазина (рис. 38б) — близкого аналога всё того же атразина. Фактически, галимедин — это тот же цианазин, только хлор в положении 2 триазинового кольца замещен метоксильной группой.
Надо сказать, что цианазин широко употребляется в сельском хозяйстве Китая, и вполне можно ожидать, что стоки с полей попадают в море, где произрастает галимеда. Возникло предположение, что галимедин — полуприродное вещество, метаболит цианазина [39]. Вероятно, в процессе метаболизма происходит гидролиз гербицида, и атом хлора замещается гидроксильной группой. А затем происходит метилирование гидроксила — тоже достаточно распространенный метаболический путь. То есть созданная человеком химическая индустрия увеличила разнообразие природных молекул! Конечно, «полуприродный» статус галимедина — только предположение. Чтобы доказать или опровергнуть его, следует изучить биосинтез этого метаболита. Если в природе возникают азиды и цианиды, то почему бы не появиться и симм-триазину?
А теперь расскажем о веществе, «полуприродный статус» которого твердо установлен. Все знают выражение о том, что сахар — наркотик. Сладкий вкус во рту автоматически поднимает настроение, придает бодрости и сил, притупляет чувство голода. Всё бы хорошо, вот только избыток сахара вреден для здоровья. Поэтому у медиков и специалистов пищевой индустрии всегда был сильный интерес к сахарозаменителям — веществам, обладающим сладким вкусом, но не усваивающимся организмом. Известно, что соленым вкусом обладает одно-единственное вещество — поваренная соль. Вкусом алкоголя — два близких соединения, этиловый и метиловый спирты. А вот сладкий вкус присущ громадному числу веществ, даже тех, чье химическое строение совсем не похоже на сахар. Поэтому в списке сахарозаменителей есть широкий выбор.
А началась их история с орто-сульфобензимида, синтезированного в XIX веке и получившего говорящее название «сахарин». Натриевая соль сахарина в 300 раз слаще сахара. Ощутимым вкусом обладают даже следовые количества этого вещества, то есть добавлять его в пищу можно совсем чуть-чуть, значительно меньше токсической дозы. К тому же сахарин хорошо растворим в воде и легко выводится из организма. Поэтому он стал первым сахарозаменителем. И употреблялся долгое время, пока ему на смену не пришли сладкие вещества нового поколения, такие как аспартам.
Но вот что удивительно. Оказалось, что в процессе биодеградации гербицида сульфометуронметила (метил-((((4,6-диметил-2-пиримидинил)-амино)-карбонил)-амино)-сульфонилбензоата) (рис. 39а) почвенными микроорганизмами среди прочих метаболитов образуется сахарин (рис. 39б)! [40]. Подсластитель из гербицида — это само по себе удивляет. Для нас же важно то, что теперь и сахарин можно отнести если не к природным, то к полуприродным веществам, продуктам метаболизма. Вот так человек разнообразит химию природных соединений!
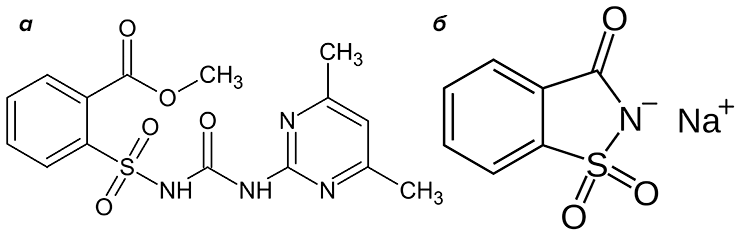
Рисунок 39. Как получить подсластитель из гербицида. а — сульфометуронметил, гербицид. б — сахаринат натрия, вещество в 300 раз слаще сахара!
Поразительное сходство
О вреде фталатов не слышал, наверное, только ленивый. Фталаты — соли фталевой (бензолдикарбоновой) кислоты, у которой есть три изомера: собственно фталевая, изофталевая и терефталевая кислоты, различающиеся расположением карбоксильных групп. Токсичность фталатов определяется их способностью имитировать действие стероидных гормонов, нарушать гормональный баланс. Самое главное в том, что эфиры фталевых кислот широко применяют в производстве пластмасс. Полиэтилентерефталат (полиэфир двухосновной терефталевой кислоты и двухатомного спирта этиленгликоля) (рис. 40) называют «бутылочным пластиком», поскольку из него изготавливают большую часть пластиковых бутылок (рис. 40). В Советском Союзе этот полимер назывался «лавсан».
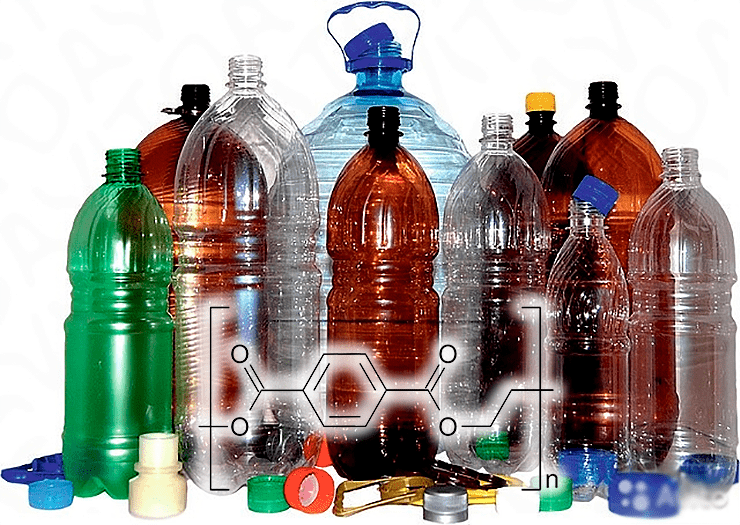
Рисунок 40. Ну очень известная пластмасса. Внизу — структура «бутылочного пластика» полиэтилентерефталата. Из него изготавливают очень популярную в наше время продукцию — пластиковые бутылки.
сайт avito.ru
Разумеется, терефталевая кислота не наносит вреда здоровью, пока она включена в полимер. А полимер достаточно устойчив к воздействию окружающей среды . Поэтому, главный вред пластиковых бутылок состоит не в загрязнении фталатами, а в их бесконтрольном накоплении в окружающей среде. А здесь все зависит от уровня культуры населения. Культурный, заботящийся о природе человек выбросит пустую бутылку в урну, а не на траву. В последнее время стали появляться специальные контейнеры для пустой пластиковой тары — и это большой прогресс в деле защиты окружающей среды.
Про то, как бактерии справляются с поеданием полиэтилентерефталата, можно с интересом почитать здесь: «Пластик на завтрак» [41], «А ты такой холодный, как... пластик в океане» [42] и «„Пластик, сэр!“, или Бактериальная диета в стиле хай-тек» [43].
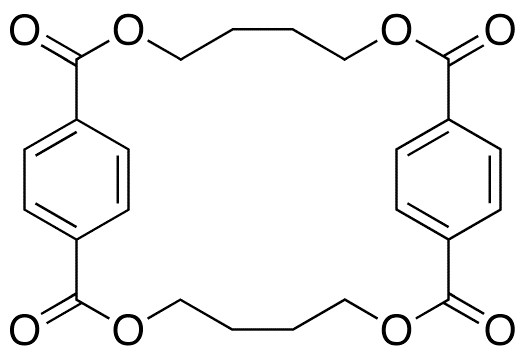
Удивительно, но вещества, близкие к бутылочному пластику, встречаются в природе. Бактерия Cytophaga sp. AM 13.1 (рис. 41а) продуцирует эфир терефталевой кислоты и двухатомного спирта (правда, не этиленгликоля, а 1,4-бутандиола, и сам эфир не линейный, а циклический). Это антисептик фарацин (рис. 41б) [44].
Ради хлеба насущного
В статье [6] рассказывалось о грибах ксилотрофах, усваивающих лигнин древесины, и их значение для биосферы. Рассказывалось в ней и о том, что лигнин — очень устойчивое и плохо поддающееся биологической деструкции вещество. И смотря на выглядывающие из лесного пня трутовики, мало кто задумывается над вопросом, как же грибам удается разрушать такой прочный материал, как древесина? Оказалось, что для этого им требуется внушительный химический арсенал, включающий такой агрессивный компонент, как свободные гидроксильные радикалы (рис. 42).

Рисунок 42. Чтобы разрушить трехмерную сеть лигнина, требуются очень изощренные методы. На фото — Phanerochaete chrysosporium на гнилом пне. Вверху справа — гидроксильный радикал.
сайт sliderbase.com
О свободных радикалах все наслышаны. Ряд ученых связывают с ними процесс старения. То есть радикалы (в том числе и гидроксильные) образуются в процессе жизнедеятельности любого организма. В клетках человека в процессе аэробного дыхания образуется целый спектр так называемых «активных форм кислорода»: пероксид, супероксид и прочие . Для защиты от этих, безусловно вредных, молекул организм содержит набор специальных ферментов: каталазы, пероксидазы, супероксиддисмутазы. Но не существует фермента, способного обезвредить гидроксил-радикал — самую агрессивную форму кислорода в организме. Он крайне нестабилен, и выделить его как самостоятельное вещество нельзя — период полужизни составляет всего миллиардную долю секунды. Это чрезвычайно сильный окислитель, оставивший далеко позади кислород и даже озон, и только совсем немного уступающий самому сильному окислителю в природе — молекулярному фтору. Гидроксильные радикалы очень реакционноспособны и реагируют буквально со всем, что есть в организме. Считается, что причиной лучевой болезни являются именно гидроксил-радикалы, образующиеся в результате радиоактивного расщепления (радиолиза) воды, из которой на 80% состоит наше тело. А единственной защитой от этого, пожалуй, самого агрессивного компонента нашего организма, являются антиоксиданты, такие, как уже упоминавшийся выше глутатион. Они принимают «удар» гидроксильных радикалов на себя.
Подробнее со всеми ими можно ознакомиться в статьях «Активный кислород: друг или враг, или о пользе и вреде антиоксидантов» [45] и «Антиоксиданты против пиелонефрита» [46].
Итак, гидроксил-радикалы образуются во всех живых клетках и являются «неизбежным злом», приводящим к повреждению этих клеток. Но, как оказалось, грибы ксилотрофы используют гидроксильные радикалы для разложения лигнина! Химики получают гидроксил-радикалы реакцией Фентона — разложением перекиси водорода в присутствии солей железа или марганца. Возбудитель белой гнили древесины, гриб Phanerochaete chrysosporium (рис. 42), выделяет в окружающее пространство глиоксаль и метилглиоксаль (тоже необычные для живых организмов вещества!) [47], при ферментативном окислении которых образуется перекись водорода, в присутствии ионов двухвалентного железа вступающая в реакцию Фентона (открытую невзрачным трутовиком задолго до человека) с выделением гидроксил-радикалов. С их помощью он и разрушает лигнин, служащий данному грибу единственным источником углерода. Гидроксильные радикалы представляют смертельную опасность для живых тканей, поэтому фанерохета продуцирует их на достаточно большом расстоянии от себя. Как результат, возникает белая гниль — лигнин, придающий древесине характерный желтовато-коричневый цвет, потребляется грибом, и остается белая, как бумага, целлюлоза (ее фанерохета не ест), которая уже не обладает прочностью нативной древесины.
Конечно, нет ничего удивительного в том, что на создание такого изощренного способа добывать пропитание ушли многие миллионы лет, о чем также было рассказано в [6].
А вот у бактерии Eubacterium acidaminophilum другая пищевая специализация. Она сбраживает аминокислоты и содержит мультиферментный комплекс — глицинредуктазу, превращающую аминокислоты глицин, саркозин и бетаин в ацетилфосфат [48], [49]. На первый взгляд, этот факт не сулит ничего интересного, ведь, в отличие от лигнина, аминокислоты обладают высокой пищевой ценностью и легко усваиваются. Но это только на первый взгляд!
Важнейшей задачей глицинредуктазы является превращение аминоуксусной кислоты в ацетильную группу. Оказалось, что ключевым полупродуктом данного превращения является кетен (карбометилен), Н2С=С=О, сильнейший ацетилирующий агент, газ с резким запахом, по токсическому воздействию сравнимый с фосгеном. В состав мультифермента входит белок, содержащий селен. В кислой среде от остатка Se-карбоксиметилселеноцистеина, входящего в активный центр, отделяются молекулы кетена и воды, с образованием связи S—Se (рис. 43). После этого кетен моментально присоединяется к сульфгидрильной группе цистеина ацетилтрансферазы, образуя S-ацетилцистеин. Поскольку образующийся кетен не покидает активный центр мультифермента, он не наносит вред клетке. Таким образом, глицинредуктазу можно уподобить чрезвычайно совершенному химическому заводу, не производящему вредные выбросы в окружающую среду, а сам кетен можно считать природным веществом.
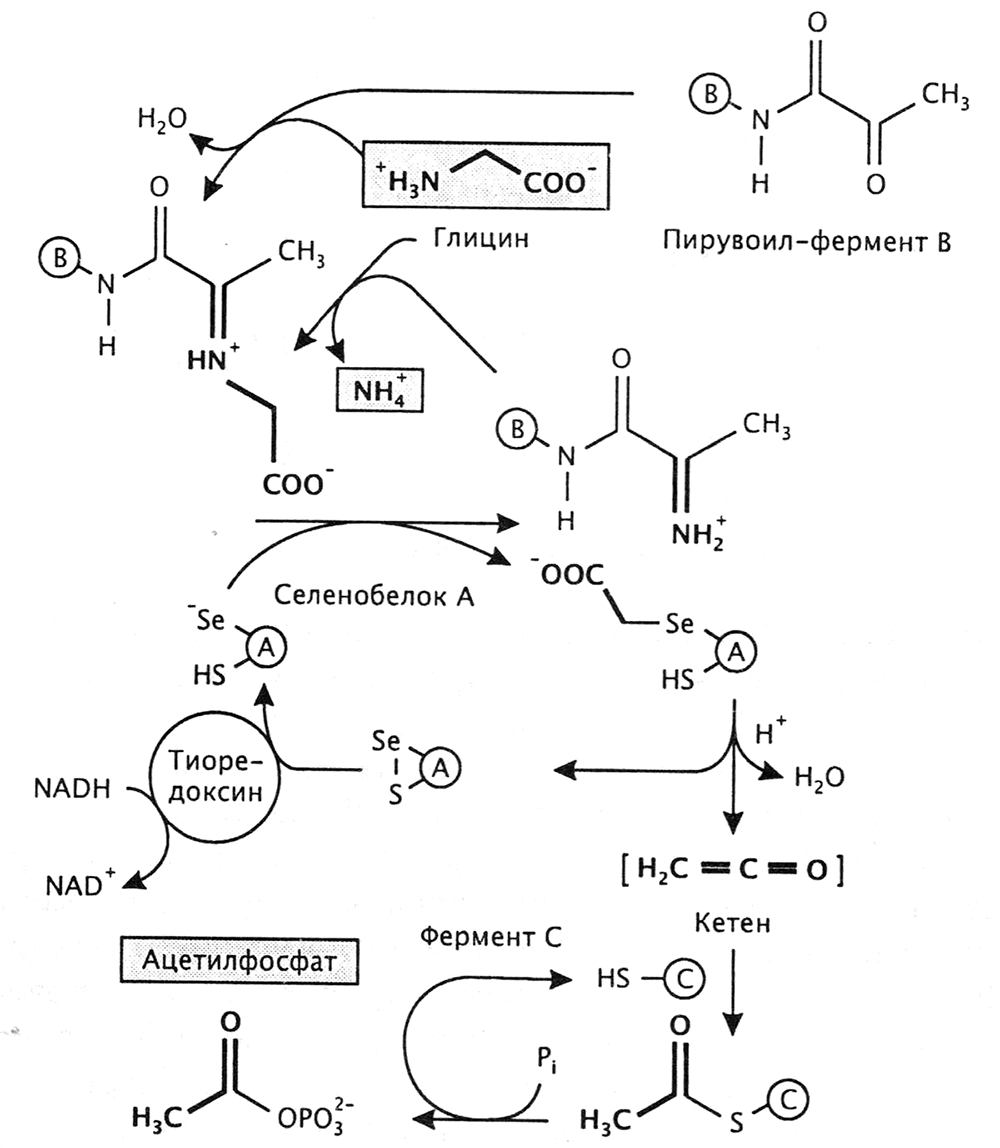
Рисунок 43. Механизм действия мультиферментного комплекса E. acidaminophilum, включающий образование высокореакционноспособного интермедиата — кетена
А что дальше?
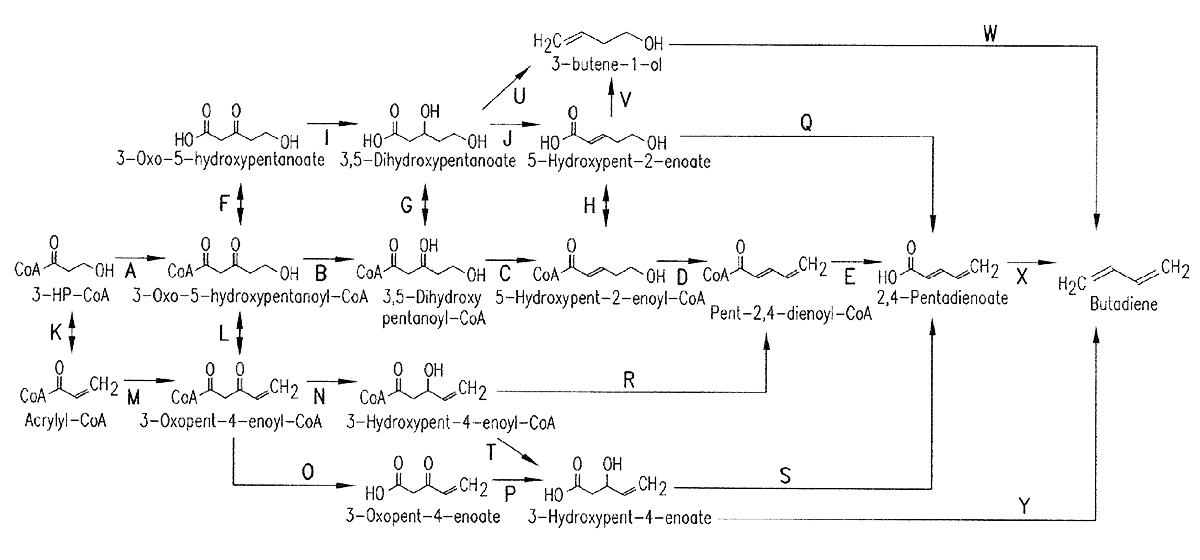
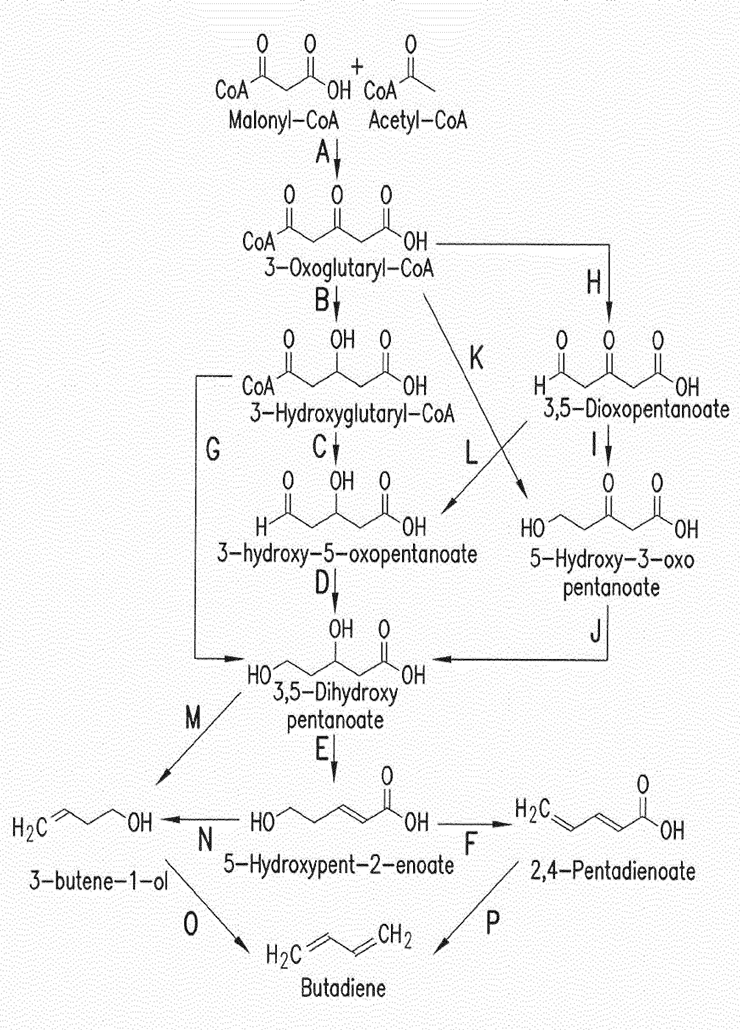
До сих пор речь шла об экзотических природных веществах. А ведь многие соединения, крупнотоннажно производимые промышленностью и имеющие большое практическое значение, в природе не найдены. Означает ли это принципиальную невозможность получения таких веществ при помощи живых организмов? Совсем не означает. Все органические вещества состоят из биогенных элементов, например, углерода. А это значит, что для их синтеза можно подобрать метаболический путь. В конце концов, все биологические молекулы когда-то не были биологическими, список природных молекул расширялся очень долго и постепенно в процессе эволюции. Методами генной инженерии уже получены микроорганизмы, продуцирующие ряд не встречающихся (или встречающихся очень редко) в природе веществ. Например, дивинил (1,3-бутадиен) — крупнотоннажное сырье в производстве каучуков и пластмасс, — не найден в живой природе. Хотя очень близкий по структуре 2-метил-1,3-бутадиен (изопрен, структурное звено натурального каучука, гуттаперчи и бесконечного многообразия терпенов и терпеноидов) широко представлен в мире растений, как в свободном виде, так и в виде производных. Мне попался на глаза вот такой прелюбопытный американский патент с описанием метаболических путей, ведущих к дивинилу (рис. 44) [50]. Разумеется (и в этом проявляется гениальная универсальность биохимии), предшественниками дивинила являются вполне себе природные молекулы, такие как ацетил-КоА и малонил-КоА. Задача исследователя в данном случае состоит в том, чтобы как пазлы сложить вместе куски геномов различных организмов и создать из уже существующих фрагментов новый, не существовавший до сих пор, метаболический путь.
Надо сказать, что это не единственный патент этого авторского коллектива. Ими запатентованы метаболические пути, ведущие к акриловой кислоте, бензолу, этиленгликолю, пропилену, гексаметилендиамину и капролактаму. По всей видимости, недалек тот день, когда расширение списка биологических молекул станет рутинным занятием.
Снова о своём
В статье «Биодеградация белого фосфора: как яд стал удобрением» [51] я рассказывал о своей работе — изучении биодеградации белого фосфора, одного из самых опасных загрязнителей окружающей среды. Разумеется, меня не мог не интересовать вопрос, а встречается ли элементный фосфор в составе живых организмов? Все-таки фосфор — биогенный элемент, и содержание его в живых тканях очень велико. В основном, конечно, в виде предельно окисленной формы — фосфата, — хотя изредка встречаются и природные фосфорорганические вещества.
В этом смысле, очень интересна работа коллектива из Индии, в которой сообщается, что плесневый гриб Aspergillus tubingensis TFR-5 накапливает в межклеточном пространстве наночастицы элементного фосфора, восстанавливая фосфат [52]! Частицы имеют средний размер чуть менее 30 нм и покрыты белковой оболочкой, из чего авторы делают вывод о ферментативном биосинтезе этих частиц. Если индийские авторы правильно интерпретировали результаты своих экспериментов, не допустив в них ошибок, то их работа — первое подтверждение того, что элементный фосфор является природным веществом биологического происхождения. К сожалению, несмотря на обилие примененных физических методов исследования наночастиц, авторы не указывают, какой аллотропной модификацией фосфора они являются. Еще бóльшее сожаление вызывает отсутствие более свежих публикаций, свидетельствующих о продолжении работ в этой области. Тем не менее их результат делает еще более убедительными аргументы в пользу биодеградации: если грибы способны синтезировать фосфор, значит, они должны и потреблять его со сравнительной легкостью.
Если поискать...
Проведенное перечисление наглядно демонстрирует тождество химических реакций, происходящих в реакторах предприятий и живых клетках. Многие вещества, считающиеся чуждыми природе и обязанные своим существованием исключительно человеку, в действительности постоянно присутствуют в биосфере, пусть даже в следовых концентрациях. Микроорганизмы-деструкторы с подобными веществами постоянно сталкиваются и способны их разлагать.
Поэтому биосфера готова к «встрече» с ними. На вещества любого строения находятся свои потребители из числа живых организмов — в первую очередь, конечно же, микробов.
Фактически, различие между «живой» и «неживой» химией основано не на составе веществ, а на их соотношении (естественно, что химическая промышленность производит больше формальдегида, чем аминокислот, а биосфера — наоборот, тем не менее следовые количества формальдегида всегда образуются в метаболизме). Невольно приходит мысль о дальнейшей бесперспективности разделения органической и биоорганической химий.
Сейчас набирает популярность такое научное направление, как метаболомика — поиск и классификация всех метаболитов, вырабатываемых конкретным организмом или видом. Будет ли когда-нибудь создан метаболом всей биосферы? Думаем, задачу эту никогда не решат полностью, но сбор информации уже ведется и продолжится далее. А результаты такого масштабного процесса могут оказаться самыми неожиданными.
Тем более что прогресс методов анализа не останавливается, а актуальность проблемы в дальнейшем станет только возрастать.
Литература
- Patrick M Grant, Jeffrey S Haas, Richard E Whipple, Brian D Andresen. (1997). A possible chemical explanation for the events associated with the death of Gloria Ramirez at Riverside General Hospital. Forensic Science International. 87, 219-237;
- T. R. Miller, R. Belas. (2004). Dimethylsulfoniopropionate Metabolism by Pfiesteria-Associated Roseobacter spp.. Applied and Environmental Microbiology. 70, 3383-3391;
- Роберт Вудворд: евангелист органической химии;
- E. Z Kurmaev, A Moewes, L Ouyang, L Randaccio, P Rulis, et. al.. (2003). The electronic structure and chemical bonding of vitamin B12. Europhys. Lett.. 62, 582-587;
- Биологический энциклопедический словарь (2-е изд., исправл.) / Гиляров М.С., Бабаев А.А., Винберг Г.Г., Заварзин Г.А. и др. М.: «Сов. энциклопедия», 1986. — с. 831;
- Биодеградация ксенобиотиков как самозащита природы;
- Maureen R. Gwinn, Douglas O. Johns, Thomas F. Bateson, Kathryn Z. Guyton. (2011). A review of the genotoxicity of 1,2-dichloroethane (EDC). Mutation Research/Reviews in Mutation Research. 727, 42-53;
- Frank Laturnus. (1996). Volatile halocarbons released from Arctic macroalgae. Marine Chemistry. 55, 359-366;
- M. B. Hossain, D. van der Helm, R. Sanduja, M. Alam. (1985). Structure of 6-azidotetrazolo[5,1-a]phthalazine, C8H4N8, isolated from the toxic dinoflaggelate Gymnodinium breve. Acta Crystallogr C. 41, 1199-1202;
- Kuenen J.G. and Jetten M.S.M. (2001). Extraordinary Anaerobic Ammonium-Oxidizing Bacteria. Unusual microbial metabolic process, although slow, can remove ammonium from wastewater in a single, oxygen-limited step. American Society of Microbiology News. 67, 456–463;
- Аммонийный датчик анаммокс-бактерии;
- John E. Walker, David L. Kaplan. (1992). Biological degradation of explosives and chemical agents. Biodegradation. 3, 369-385;
- Natalia K. Utkina, Vladimir A. Denisenko, Olga V. Scholokova, Marina V. Virovaya, Andrey V. Gerasimenko, et. al.. (2001). Spongiadioxins A and B, Two New Polybrominated Dibenzo-p-dioxins from an Australian Marine SpongeDysidea dendyi. J. Nat. Prod.. 64, 151-153;
- Xueshi Huang, Jian He, Xuemei Niu, Klaus-Dieter Menzel, Hans-Martin Dahse, et. al.. (2008). Benzopyrenomycin, a Cytotoxic Bacterial Polyketide Metabolite with a Benzo[a]pyrene-Type Carbocyclic Ring System. Angew. Chem. Int. Ed.. 47, 3995-3998;
- «Зеленые» революционеры;
- Роль слабых взаимодействий в биополимерах;
- Xiao-Hua Xu, Guang-Min Yao, Yan-Ming Li, Jian-Hua Lu, Chang-Jiang Lin, et. al.. (2003). 5-Fluorouracil Derivatives from the SpongePhakellia fusca. J. Nat. Prod.. 66, 285-288;
- Bram Van de Poel, Dominique Van Der Straeten. (2014). 1-aminocyclopropane-1-carboxylic acid (ACC) in plants: more than just the precursor of ethylene!. Front. Plant Sci.. 5;
- J. A. Swenberg, K. Lu, B. C. Moeller, L. Gao, P. B. Upton, et. al.. (2011). Endogenous versus Exogenous DNA Adducts: Their Role in Carcinogenesis, Epidemiology, and Risk Assessment. Toxicological Sciences. 120, S130-S145;
- Dongjin Ji, Youngkeun Yi, Ga-Hwa Kang, Yong-Hwa Choi, Pankyung Kim, et. al.. (2004). Identification of an antibacterial compound, benzylideneacetone, fromXenorhabdus nematophilaagainst major plant-pathogenic bacteria. FEMS Microbiology Letters. 239, 241-248;
- Bang-Hua Xie, Zhi Guan, Yan-Hong He. (2012). Promiscuous enzyme-catalyzed Michael addition: synthesis of warfarin and derivatives. J. Chem. Technol. Biotechnol.. 87, 1709-1714;
- G. A. Strobel, B. Knighton, K. Kluck, Y. Ren, T. Livinghouse, et. al.. (2008). The production of myco-diesel hydrocarbons and their derivatives by the endophytic fungus Gliocladium roseum (NRRL 50072). Microbiology. 154, 3319-3328;
- Eisner T., Morgan R.C., Attygalle A.B., Smedley S.R., Herath K.B., Meinwald J. (1997). Defensive production of quinoline by a phasmid insect (Oreophoetes peruana). J. Exp. Biol. 19, 2493–2500;
- Kei Wada, Jun Hiratake, Machiko Irie, Toshihiro Okada, Chiaki Yamada, et. al.. (2008). Crystal Structures of Escherichia coli γ-Glutamyltranspeptidase in Complex with Azaserine and Acivicin: Novel Mechanistic Implication for Inhibition by Glutamine Antagonists. Journal of Molecular Biology. 380, 361-372;
- Albert S. Mildvan, John S. Leigh, Mildred Cohn. (1967). Kinetic and Magnetic Resonance Studies of Pyruvate Kinase. III. The Enzyme-Metal-Phosphoryl Bridge Complex in the Fluorokinase Reaction*. Biochemistry. 6, 1805-1818;
- Valery M. Dembitsky, Ilia Shkrob, Ovadia Lev. (2000). . Journal of Chemical Ecology. 26, 1359-1366;
- H U Kafferlein. (2005). The use of biomarkers of exposure of N,N-dimethylformamide in health risk assessment and occupational hygiene in the polyacrylic fibre industry. Occupational and Environmental Medicine. 62, 330-336;
- Serve' M.P. (1993). A study of the effect of hydrocarbon structure on the induction of male rate nephropathy and metabolic structure. Final Technical Report For United States Air Force Grant No. AFOSR-89-0396 For The Period of June 1, 1989 -August 31, 1993. 61 p.;
- Stefanie Bail, Sabine Krist, Eliot Masters, Heidrun Unterweger, Gerhard Buchbauer. (2009). Volatile compounds of shea butter samples made under different production conditions in western, central and eastern Africa. Journal of Food Composition and Analysis. 22, 738-744;
- Спокоен как GABA;
- Эпилепсия, методы ее лечения и роль вальпроевой кислоты в терапии заболевания;
- Cynthia A. Danquah, Eleftheria Kakagianni, Proma Khondkar, Arundhati Maitra, Mukhlesur Rahman, et. al.. (2018). Analogues of Disulfides from Allium stipitatum Demonstrate Potent Anti-tubercular Activities through Drug Efflux Pump and Biofilm Inhibition. Sci Rep. 8;
- David Schilter, Thomas B. Rauchfuss, Matthias Stein. (2012). Connecting [NiFe]- and [FeFe]-Hydrogenases: Mixed-Valence Nickel–Iron Dithiolates with Rotated Structures. Inorg. Chem.. 51, 8931-8941;
- Paul A. Lindahl. (2004). Acetyl-coenzyme A synthase: the case for a Nip0-based mechanism of catalysis. J Biol Inorg Chem. 9, 516-524;
- J. A. Wiig, Y. Hu, C. C. Lee, M. W. Ribbe. (2012). Radical SAM-Dependent Carbon Insertion into the Nitrogenase M-Cluster. Science. 337, 1672-1675;
- B. Vanelslander, C. Paul, J. Grueneberg, E. K. Prince, J. Gillard, et. al.. (2012). Daily bursts of biogenic cyanogen bromide (BrCN) control biofilm formation around a marine benthic diatom. Proceedings of the National Academy of Sciences. 109, 2412-2417;
- S L Hazen, F F Hsu, D M Mueller, J R Crowley, J W Heinecke. (1996). Human neutrophils employ chlorine gas as an oxidant during phagocytosis.. J. Clin. Invest.. 98, 1283-1289;
- Ines Mancini, Graziano Guella, Maryvonne Frostin, Edouard Hnawia, Dominique Laurent, et. al.. (2006). On the First Polyarsenic Organic Compound from Nature: Arsenicin A from the New Caledonian Marine SpongeEchinochalina bargibanti. Chem. Eur. J.. 12, 8989-8994;
- Istv�n Ujv�ry. (2000). Semi-natural products and related substances as alleged botanical pesticides. Pest Manag. Sci.. 56, 703-705;
- Jeffrey J. Anderson, Joseph J. Dulka. (1985). Environmental fate of sulfometuron methyl in aerobic soils. J. Agric. Food Chem.. 33, 596-602;
- Пластик на завтрак;
- А ты такой холодный, как... пластик в океане;
- «Пластик, сэр!», или Бактериальная диета в стиле хай-тек;
- Mohamed Shaaban, Rajendra P. Maskey, Irene Wagner-Döbler, Hartmut Laatsch. (2002). Pharacine, a Naturalp-Cyclophane and Other Indole Derivatives fromCytophagasp. Strain AM13.11. J. Nat. Prod.. 65, 1660-1663;
- Активный кислород: друг или враг, или О пользе и вреде антиоксидантов;
- Антиоксиданты против пиелонефрита;
- Phil Kersten, Dan Cullen. (2007). Extracellular oxidative systems of the lignin-degrading Basidiomycete Phanerochaete chrysosporium. Fungal Genetics and Biology. 44, 77-87;
- Jan R. Andreesen. (1994). Glycine metabolism in anaerobes. Antonie van Leeuwenhoek. 66, 223-237;
- Ленгелер Й., Древс Г., Шлегель Г. Современная микробиология. Прокариоты (т. 1). М.: «Мир», 2005. — 654 с.;
- Burk M.J., Burgard A.P., Osterhout R.E., Sun J., Pharkya P. (2013). Microorganisms for the production butadiene and methods related thereto. Patent US 2013/0011891A1;
- Биодеградация белого фосфора: как яд стал удобрением;
- J. C. Tarafdar, Ramesh Raliya, Indira Rathore. (2012). Microbial Synthesis of Phosphorous Nanoparticle from Tri-Calcium Phosphate Using Aspergillus tubingensis TFR-5. j bionanosci. 6, 84-89.