
Добавки не будет: голодание продлевает мышам жизнь. А что насчет людей?
01 ноября 2018
Добавки не будет: голодание продлевает мышам жизнь. А что насчет людей?
- 3276
- 1
- 9
Все и так знают, что много есть — вредно. Разве что-то еще неясно?
-
Автор
-
Редакторы
Статья на конкурс «био/мол/текст»: «Кто ест мало, живет долго, ибо ножом и вилкой роем мы могилу себе», — говорит граф Калиостро в фильме Марка Захарова. Связь между количеством еды и продолжительностью жизни обнаружена даже у тех организмов, которые ножом и вилкой пользоваться не умеют. Сразу возникают вопросы: насколько мало нужно есть? Как это работает? И главное — что делать, если есть всё равно хочется?
Конкурс «био/мол/текст»-2018
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2018.

Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

Спонсором приза зрительских симпатий выступил медико-генетический центр Genotek.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Переедать действительно не стоит, это правда. Когда кто-то в нашем понимании «много ест», он получает больше энергии, чем тратит. При этом излишек энергии запасается в виде жира. Ожирение, в свою очередь, приводит с собой дружную компанию сопутствующих заболеваний. Но сейчас речь не об этом. Еще в 1935 году было обнаружено, что животные, которые едят меньше, чем тратят энергии, живут дольше своих сородичей, которые соблюдают баланс [1]. С тех пор таким нехитрым способом удалось продлить жизнь множества организмов, от дрожжей и червей до мышей и обезьян.
А что насчет людей?
В отличие от червя или мыши, с человеком сложно поставить контролируемый эксперимент длиной во всю его жизнь. Поэтому научно достоверных результатов у нас пока нет. Однако события XX века обеспечили нас данными, которые никто не заказывал [2]. Такими случайными экспериментами стали, например, мировые войны. Население некоторых стран не несло серьезных потерь в ходе боевых действий, но при этом испытывало дефицит пищи. Так, во время Первой мировой войны из-за прекращения торговли с США и Британией жители Копенгагена были вынуждены в течение двух лет есть меньше, чем обычно. После этого продовольственный советник правительства подсчитал, что смертность в столице Датского королевства сократилась на 34% [3].
В течение Второй мировой войны были ограничены в еде жители оккупированной Норвегии, и количество смертей, вызванных болезнями системы кровообращения, упало на 30% по сравнению с довоенным временем — по мнению норвежских исследователей, во многом благодаря вынужденной диете [4].
Третий непредвиденный эксперимент развернулся в Японии. Еще в конце ХХ века количество долгожителей на Окинаве было в 4–5 раз больше, чем в других цивилизованных странах. Смертность пожилых людей была ниже, а средняя продолжительность жизни — выше, причем не только по сравнению с другими странами, но и по сравнению с другими японскими островами. Оказалось, что типичный окинавский рацион (много овощей и фруктов, рыба, соя, рис) содержит меньше калорий, чем рационы прочих регионов Японии, не говоря уж о США [5]. Однако в 60-х годах американские солдаты привезли с собой культуру фастфуда; проникла она и на Окинаву. Как результат — в начале XXI века рожденные на Окинаве уже не могут рассчитывать прожить дольше других [6].
Мало есть — это сколько?
Главное — не путать ограничение калорий с голоданием и недоеданием. Во-первых, человек не должен голодать. Ученые говорят о сокращении калорийности рациона в среднем на 20–30%. То есть человек в таком случае потребляет на 20−30% меньше энергии, чем тратит. Возникает логичный вопрос: почему тогда человек не заканчивается совсем? Ниже мы расскажем, как при дефиците питания организм начинает расходовать ресурсы эффективнее. Во-вторых, нужно, чтобы рацион включал в себя все необходимые группы веществ: белки, жиры, углеводы, витамины и т.д. Это хорошо видно на приведенных выше примерах. Почему ученые отталкивались от историй с жителями Скандинавии во время мировых войн? Потому, что хоть они и испытывали ограничения в питании, их рацион всё еще был полноценным. У них была возможность есть, например, свежие овощи и рыбу. Та же история и с жителями Окинавы.
На самом деле запланированные эксперименты с людьми тоже проводили. Например, в рамках проекта CALERIE (Comprehensive Assessment of Long-term Effects of Reducing Intake of Energy, всесторонее исследование долгосрочных эффектов сокращения потребления энергии) добровольцы пробовали в течение нескольких месяцев потреблять на 25% меньше калорий и иногда заниматься физическими упражнениями [2]. Исследования эти недавние, поэтому данные о смертности появятся нескоро. Но уже по окончании первых экспериментов стало видно, что у тех, кто меньше ел, по сравнению с контрольной группой снизилась вероятность развития сердечно-сосудистых заболеваний и диабета: в крови уменьшилась концентрация соответствующих веществ-маркеров.
Исследовали и более суровые ограничения: в проекте Minnesota starvation experiment люди потребляли на 40% меньше необходимого (в среднем в день получали 1800 ккал, а тратили 3000) [7]. В этом случае исследователи как раз пытались воссоздать ситуацию голодания во время войны. Помимо улучшения некоторых метаболических показателей, результаты, как и следовало ожидать, выглядели не особенно ободряющими: слабость, отеки, депрессия, нарушения поведения… Впрочем, после возвращения к нормальному режиму питания эти симптомы исчезли. Но интересно, что примерно 50% участников эксперимента, достигнув 80 лет, прожили на восемь лет дольше ожидаемого для их поколения [2].
Как узнать, сколько энергии я трачу?
Если вы не участвуете в соответствующем эксперименте, измерить энергозатратность вашего образа жизни своими силами не получится. В лабораторных условиях есть несколько методик, большинство из которых сводится к измерению количества выделяемого человеком углекислого газа. Он образуется в результате дыхания клетки, то есть расщепления питательных веществ с высвобождением энергии. Например, можно поместить испытуемого в герметичную комнату и смотреть, как там будет изменяться концентрация углекислого газа. Правда, чтобы имитировать повседневную активность, в комнате придется установить тренажеры и беговые дорожки.
Чтобы не строить комнату, можно воспользоваться методом двойной меченой воды (рис. 1) [8]. Это молекула воды, состоящая из тяжелых изотопов водорода и кислорода. Мы вводим в организм меченую воду, а через некоторое время измеряем количество изотопов в крови. Со временем их будет всё меньше. При этом мы знаем, что водород может выходить из организма в основном в составе воды, а кислород — еще и в составе углекислого газа. Поэтому считаем, сколько всего кислорода потерял организм, и вычитаем количество потерянного водорода. Получаем количество углекислого газа, которое организм выдохнул, и его уже пересчитываем на количество затраченной энергии.

Рисунок 1. Метод двойной меченой воды. Человек получает тяжелые изотопы водорода и кислорода. Вычитая количество выведенного водорода из количества выведенного кислорода, можно получить количество образовавшегося углекислого газа —показатель энергозатрат организма.
Но что если у вас нет ни герметичной комнаты, ни меченой воды? Можно попробовать замерить, сколько вы едите обычно. В экспериментах с животными ученые измеряют потребление ad libitum, то есть до состояния насыщения. Мы не мыши, и есть нас часто заставляют не потребность в энергии, а многие другие факторы: привычки, социализация, депрессия и т.д. Тем не менее можно проследить, сколько еды вам нужно — в калориях, конечно же, — чтобы перестать чувствовать голод. Дальше из этого значения можно вычесть 20–25%. Так вы получите число калорий, которое нужно получать ежедневно, если вы решитесь влезть в шкуру окинавского долгожителя.
Какую еду нужно есть?
Клетки нашего организма могут переварить любые биополимеры, но с разной эффективностью и скоростью. Наиболее распространенная еда — глюкоза. Полная цепочка ее расщепления включает в себя анаэробный этап в цитоплазме (гликолиз) и процессы с участием кислорода в митохондриях (цикл Кребса и окислительное фосфорилирование). Можно остановиться сразу после гликолиза. Это окажется менее выгодно с точки зрения энергии, но займет меньше времени. Если же идти до конца, то энергии получается больше, но не сразу. С остальными вариантами еды «ускориться» не получится: аминокислоты и жирные кислоты сначала превращаются в промежуточный продукт, ацетил-коА, который участвует в митохондриальных процессах извлечения энергии [9]. То есть расщепление аминокислот и жирных кислот всегда происходит аэробно, с участием кислорода (рис. 2).

Рисунок 2. Метаболические пути разных продуктов питания. Основной путь — расщепление глюкозы. Пути расщепления белков и триглицеридов присоединяются к нему уже на аэробных стадиях. При этом все этапы процессов обратимы, кроме цикла Кребса и окислительного фосфорилирования (самый большой энергетический выход). Кетогенная диета (высокое содержание жиров и низкое — углеводов) приводит к накоплению кетоновых телец и активирует аэробный обмен веществ. На каждом этапе расщепления макромолекул параллельно с нуклеозидтрифосфатами образуются водородные эквиваленты. Поэтому отношение окисленных форм эквивалентов к восстановленным (например, NAD+/NADH) может служить маркером количества энергии в клетке и влиять на работу ключевых транскрипционных регуляторов (например, сиртуинов, см. ниже).
Клетки могут регулировать тип своего энергетического обмена, изменяя соотношение гликолиз / аэробное дыхание. Подкармливая их глюкозой, мы предлагаем им получать энергию более простым и менее эффективным путем. Поэтому, если мы хотим ограничить количество калорий, нужно заставить клетки использовать всю доступную энергию, а следовательно, снизить количество углеводов. В радикальном варианте это приводит к кетогенной диете, когда углеводов совсем мало, зато много жиров. Пользу этой диеты до сих пор оценить сложно. Ее давно применяют для лечения эпилепсии [10], и в профилактике нейродегенеративных заболеваний она себя показала неплохо [11]. Тем не менее ее довольно трудно выдерживать, а никаких данных о продолжительности жизни на ней пока нет. Итак, главное — сокращать количество углеводов, но при этом не допускать радикальных перекосов типа полного исключения углеводов из рациона.
Как часто нужно есть?
Само по себе ограничение калорий никак не связано с режимом питания. По крайней мере, если мы говорим о продлении жизни, а не о похудении или оздоровлении желудочно-кишечного тракта. Но в связи с ограничением калорий часто упоминают интервальное голодание. Идея последнего в том, что мы ограничиваем себя только в определенные промежутки времени — например, один или два дня в неделю. В результате активируются те же самые клеточные механизмы, что и при длительном ограничении калорийности рациона, просто происходит это с некоторой периодичностью. Последние исследования показывают, что оба метода эффективны, но ограничение калорий всё равно продлевает жизнь подопытных животных сильнее [12].
Каким образом ограничение калорий продляет жизнь?
Кажется, это самый сложный вопрос, и окончательный ответ на него всё еще ищут. Судя по всему, ограничение калорий переводит клетку в режим боевой готовности. Вот как это происходит. Когда клетке не хватает глюкозы, приходится использовать ее по «длинному» пути. Для этого митохондрии потребляют кислород, который неизбежно образует свободные радикалы — молекулы, активно вступающие в химические реакции. Свободные радикалы атакуют все окружающие молекулы, и в клетке начинают копиться повреждения. Это называют окислительным стрессом. Реакция клетки на стресс зависит от его тяжести, то есть количества радикалов. Если их слишком много, клетка может преждевременно состариться или покончить с собой. Слабый стресс, наоборот, может побудить клетку мобилизовать свои ресурсы — этот эффект называют гормезисом.
На сегодняшний день мы знаем три главных белка-«переключателя» [13]. Это киназа mTOR, инсулиноподобный фактор роста (IGF1) и гормон роста (соматотропин) [14]. Все они работают как сенсоры еды, реагируя на наличие в клетке самих питательных веществ (глюкозы и других мономеров) или их энергетических эквивалентов (например, АТФ). Если еда есть, то mTOR запускает синтез белка, гормон роста — рост клетки, IGF — поглощение веществ извне и запасание их внутри клетки. Все эти процессы приводят к накоплению в клетке свободных радикалов и дефектных белков — побочных продуктов интенсивного обмена веществ. Ограничение калорий снижает активность этих трех регуляторов и соответствующих сигнальных путей. При этом клетка начинает производить собственные антиоксиданты и запускает аутофагию — процесс частичного переваривания своих белков и органелл [15], [16]. Это позволяет избавиться от накопленных повреждений и стать устойчивее к стрессам (рис. 3).
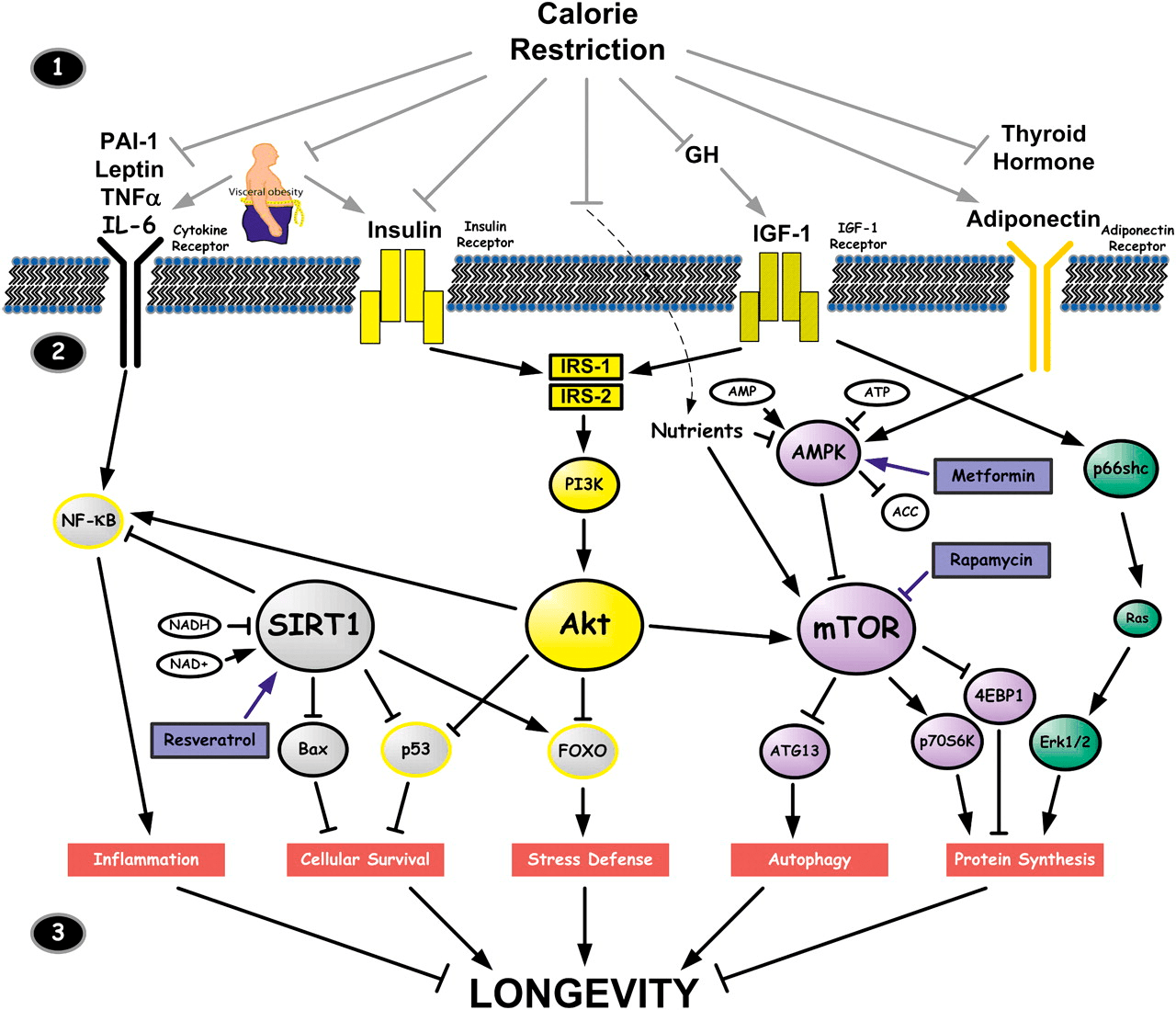
Рисунок 3. Влияние ограничения калорий на молекулярные механизмы, регулирующие продолжительность жизни. Универсальный эффект ограничения калорий объясняется тем, что оно меняет работу множества сигнальных путей одновременно. В частности, вмешивается в сигнализацию mTOR (ее блокирует AMPK, чувствительная к уровню АМФ), гормона роста (который индуцирует синтез IGF1), инсулина (который опосредованно активирует mTOR), провоспалительных цитокинов (которые выделяются сенесцентными клетками жировой ткани) и сиртуинов — гистоновых ацетилтрансфераз, мешающих работе проапоптотических генов и способствующих выживанию клеток.
Получается, что клетка становится здоровее и живет дольше при слабой интенсивности обмена веществ. Однако это верно лишь для взрослых организмов, в которых процессы роста и развития закончились. То есть один и тот же механизм, в котором белки-переключатели активируют обмен веществ, оказывается благоприятным для молодых особей и губительным для старых. Эту двойственность эффектов называют антагонистической плейотропией; в данном случае речь идет о временной плейотропии [17]. На этом понятии основана теория квазипрограммы старения, выдвинутая Михаилом Благосклонным: она заключается в том, что старение — это побочный эффект затянувшейся активной молодости [13]. У нее есть различные подтверждения: например, люди, чья молодость была не настолько активной из-за гормональных нарушений (пример — синдром Ларона, дефект рецептора гормона роста), реже болеют возрастными заболеваниями [18]. Согласно М. Благосклонному, главная наша проблема состоит в том, что нет никакого механизма, своевременно «выключающего» белки-переключатели, поэтому наш организм не узнает о том, что время активной молодости подошло к концу.
Есть ли еще плюсы в том, чтобы есть мало?
Конечно. Окислительный стресс влияет не только на скорость старения клеток. Например, он сопровождает многие нейродегенеративные заболевания. Поэтому ограничение калорий может помочь их предотвратить. И даже у здоровых людей, которые меньше едят, улучшаются вербальная память и деление стволовых клеток в мозге [11]. Кроме того, при недостатке еды у клеток усиливается чувствительность к инсулину [19]. Инсулин стимулирует захват клетками сахара из крови, а раз сахара мало, то по сигналу надо начинать хватать активнее. Это снижает риск развития сахарного диабета II типа [20], при котором клетки перестают реагировать на инсулин, и сахар в крови накапливается. Наконец, окислительный стресс лежит в основе воспаления, поэтому ограничение калорий приглушает иммунный ответ. Некоторые исследования показали, что кратковременное голодание до и после полостных операций улучшает их исход и заживление ран [20]. Ограничение калорий не только мотивирует к выживанию обычные клетки, но и бьет по опухолевым. У раковых клеток изменяется обмен веществ, они переключаются на быстрое расщепление глюкозы. Поэтому когда ее концентрация в крови падает, падают и шансы на выживание опухоли [21].
Что делать, если я не могу есть меньше?
Это действительно непросто: даже организаторы проекта CALERIE жалуются, что их волонтерам не удается в должной мере ограничивать себя в еде. Поэтому здесь можно посоветовать только тренировать силу воли или ждать более убедительных доказательств того, что ограничение калорий работает. Но если случилось так, что вам нельзя есть меньше по медицинским показаниям, всё же можно поискать выход. Существует несколько лекарственных аналогов голодания, но — будьте бдительны! — ни один из них пока не рекомендован к применению без достаточных показаний. Иными словами, похудеть и продлить жизнь одними таблетками, кажется, пока не получится.
Эффект, похожий на ограничение калорий, дает препарат рапамицин. Это очень многофункциональное вещество: изначально его открыли как антибиотик, потом обнаружили у него иммуносупрессивные свойства (и до сих пор его используют для предотвращения отторжения трансплантатов), а также выяснили, что он подавляет рост опухолей, блокируя mTOR (и сейчас его «родственники» — темсиролимус и эверолимус — одобрены в США для лечения рака) [21]. И наконец оказалось, что рапамицин продлевает жизнь мышам. Собственно, благодаря нему и был открыт белок mTOR, название которого расшифровывается как mammalian target of rapamycin — мишень рапамицина у млекопитающих. Вообще, у рапамицина есть довольно неприятные побочные эффекты (например, подавление иммунитета). Но в низких концентрациях он может быть менее опасен. Совсем недавно закончились первые клинические испытания аналогов рапамицина, которые повысили устойчивость пожилых людей к сезонным простудам и помогли им эффективнее отреагировать на прививки [22]. Поэтому теперь мы знаем, что такое лечение по меньшей мере безопасно, и можем ждать новые клинические исследования.
Есть и другие аналоги ограничения калорий. Например, метформин — препарат, который помогает похудеть при диабете II типа. Он может работать как аналог голодания, но до сих пор неизвестно, насколько он эффективен у здоровых людей, не страдающих диабетом. А жизнь он пока достоверно продлил только мышам [23]. Единственный препарат, который можно принимать без серьезных показаний, — ресвератрол. Но эффективность этой пищевой добавки пока не подтверждена клиническими исследованиями [24].
Так что же в итоге? Судя по всему, потреблять меньше калорий действительно полезно, если вы не страдаете тяжелыми заболеваниями. Но таблетками здесь не обойтись, поэтому придется напрячь силу воли. Или же записаться добровольцем на клиническое исследование — там за вами точно последят.
Первоначальная версия этой статьи была опубликована на портале «Чердак» [25].
Литература
- C. M. McCay, L. A. Maynard, G. Sperling, LeRoy L. Barnes. (1939). Retarded Growth, Life Span, Ultimate Body Size and Age Changes in the Albino Rat after Feeding Diets Restricted in Calories. The Journal of Nutrition. 18, 1-13;
- Jasper Most, Valeria Tosti, Leanne M. Redman, Luigi Fontana. (2017). Calorie restriction in humans: An update. Ageing Research Reviews. 39, 36-45;
- M. HINDHEDE. (1920). THE EFFECT OF FOOD RESTRICTION DURING WAR ON MORTALITY IN COPENHAGEN. JAMA. 74, 381;
- Axel Strm, R.Adelsten Jensen, M.D. Oslo, M.D. Oslo. (1951). MORTALITY FROM CIRCULATORY DISEASES IN NORWAY 1940-1945. The Lancet. 257, 126-129;
- B. J. WILLCOX, D. C. WILLCOX, H. TODORIKI, A. FUJIYOSHI, K. YANO, et. al.. (2007). Caloric Restriction, the Traditional Okinawan Diet, and Healthy Aging: The Diet of the World's Longest-Lived People and Its Potential Impact on Morbidity and Life Span. Annals of the New York Academy of Sciences. 1114, 434-455;
- Yasuo Kagawa. (1978). Impact of westernization on the nutrition of Japanese: Changes in physique, cancer, longevity and centenarians. Preventive Medicine. 7, 205-217;
- Leah M. Kalm, Richard D. Semba. (2005). They Starved So That Others Be Better Fed: Remembering Ancel Keys and the Minnesota Experiment. The Journal of Nutrition. 135, 1347-1352;
- D. A. Schoeller, E. van Santen. (1982). Measurement of energy expenditure in humans by doubly labeled water method. Journal of Applied Physiology. 53, 955-959;
- Нутригеномика: питание vs. заболевания;
- Эпилепсия, методы ее лечения и роль вальпроевой кислоты в терапии заболевания;
- A. H. Morgan, Z. B. Andrews, J. S. Davies. (2017). Less is more: Caloric regulation of neurogenesis and adult brain function. J Neuroendocrinol. 29, e12512;
- Sarah J. Mitchell, Michel Bernier, Julie A. Mattison, Miguel A. Aon, Tamzin A. Kaiser, et. al.. (2018). Daily Fasting Improves Health and Survival in Male Mice Independent of Diet Composition and Calories. Cell Metabolism;
- Mikhail V. Blagosklonny. (2012). Answering the ultimate question “What is the Proximal Cause of Aging?”. aging. 4, 861-877;
- Нутригеронтология: питание vs. старение;
- Аутофагия, протофагия и остальные;
- Нобелевская премия по медицине и физиологии 2016: за самоедство;
- Alexey Golubev, Andrew D. Hanson, Vadim N. Gladyshev. (2018). A Tale of Two Concepts: Harmonizing the Free Radical and Antagonistic Pleiotropy Theories of Aging. Antioxidants & Redox Signaling. 29, 1003-1017;
- Zvi Laron, Rivka Kauli, Lena Lapkina, Haim Werner. (2017). IGF-I deficiency, longevity and cancer protection of patients with Laron syndrome. Mutation Research/Reviews in Mutation Research. 772, 123-133;
- Amol Chaudhari, Richa Gupta, Kuldeep Makwana, Roman Kondratov. (2017). Circadian clocks, diets and aging. NHA. 4, 101-112;
- Andres E. Carrillo, Andreas D. Flouris. (2011). Caloric restriction and longevity: Effects of reduced body temperature. Ageing Research Reviews. 10, 153-162;
- Gelina S. Kopeina, Vyacheslav V. Senichkin, Boris Zhivotovsky. (2017). Caloric restriction - A promising anti-cancer approach: From molecular mechanisms to clinical trials. Biochimica et Biophysica Acta (BBA) - Reviews on Cancer. 1867, 29-41;
- Joan B. Mannick, Melody Morris, Hans-Ulrich P. Hockey, Guglielmo Roma, Martin Beibel, et. al.. (2018). TORC1 inhibition enhances immune function and reduces infections in the elderly. Sci. Transl. Med.. 10, eaaq1564;
- Alejandro Martin-Montalvo, Evi M. Mercken, Sarah J. Mitchell, Hector H. Palacios, Patricia L. Mote, et. al.. (2013). Metformin improves healthspan and lifespan in mice. Nat Comms. 4;
- Yi-Rong Li, Shiming Li, Chi-Chien Lin. (2018). Effect of resveratrol and pterostilbene on aging and longevity. BioFactors. 44, 69-82;
- Лосева П. (2018). Добавки не будет. «Чердак».







