
АМТ-061 — генная терапия, способная на революцию в лечении гемофилии
19 декабря 2019
АМТ-061 — генная терапия, способная на революцию в лечении гемофилии
- 2910
- 0
- 7
Современные генетические технологии на пороге того, чтобы избавить людей с гемофилией от этого тяжкого, мешающего нормальной жизни заболевания
иллюстрация Ирины Ефремовой
-
Автор
-
Редакторы
-
Иллюстратор
В 2018 году голландская компания uniQure запустила клинические испытания этранакогена дезапарвовека (АМТ-061) — препарата для генной терапии гемофилии B. Это лекарство может стать первой на рынке генной терапией гемофилии и привести к настоящему прорыву. Именно поэтому препарат получил от Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) специальный статус breakthrough therapy designation, обеспечивающий ускоренное рассмотрение препарата ведомством.
Современные лекарства
Спецпроект о современных лекарствах, истории их создания, методах разработки и тенденциях развития.

Партнер спецпроекта — компания Cytiva — образовалась в результате продажи подразделения GE Healthcare Biopharma корпорации Danaher Corporation. Cytiva — глобальный поставщик технологий и услуг, которые продвигают и ускоряют разработку и производство терапевтических средств. У компании богатое наследие, насчитывающее сотни лет. Клиенты Cytiva проводят мероприятия по спасению жизни, начиная от фундаментальных биологических исследований и заканчивая разработкой инновационных вакцин, биологических препаратов и новейших клеточных и генных терапий. Задача компании — предоставить инструменты и услуги, которые им необходимы, чтобы они работали лучше, быстрее и безопаснее, что приведет к лучшим результатам для пациентов.
Гемофилия и как ее лечат
Гемофилия — это редкое генетическое заболевание, при котором из-за дефицита факторов свертывания крови процесс нормальной коагуляции оказывается нарушенным, что приводит к кровотечениям и кровоизлияниям, иногда опасным для жизни и способным значительно ухудшить ее качество. Особенно распространены поражения суставов в связи с внутрисуставными кровотечениями. Сейчас в мире насчитывается более 187 000 человек с гемофилией, причем около 80% из них страдают от более распространенной разновидности болезни — гемофилии A [1].
Свертывание крови поражает своей сложностью и изяществом. Мы разбирали его в статье «Как работает свертывание крови?» [2]. — Ред.
Помимо распространенности, разновидности гемофилии различаются по типу недостающего фактора свертывания. Для гемофилии А — это фактор VIII, а для гемофилии B — фактор IX (рис. 1).

Рисунок 1. Схема каскада коагуляции крови. Каскад в норме запускается в случае повреждения стенки кровеносного сосуда и заканчивается образованием белка фибрина — основного компонента кровяного сгустка. Такой сложный каскад со множеством регуляторов необходим потому, что для организма опасны как кровотечения, так и повышенная свертываемость крови, приводящая к тромбозам. При недостаточности или мутациях в факторе VIII развивается гемофилия А, в факторе IX — гемофилия В, в факторе XI — самый редкий вид, гемофилия С.
Заместительная терапия
Гемофилию лечат сегодня главным образом инъекционным введением пациентам недостающих факторов свертывания. Такая терапия называется заместительной и практикуется еще с 50-х годов прошлого века, при этом технология, на которой она основана, с тех пор претерпела значительные изменения и улучшения. Это было достигнуто благодаря введению более тщательного скрининга донорской крови (на присутствие вирусных патогенов), технологий концентрирования плазмы крови (для инфузий в меньшем объеме), и, наконец, клонированию генов факторов свертывания VIII и IX, позволившему создать рекомбинантные «версии» этих белков, имеющие более эффективный профиль эффективности и безопасности [4], [5].
Прочитать об этом можно в статье «Биомолекулы»: «Три поколения лекарств» [4].
Тем не менее заместительную терапию сейчас трудно назвать идеальной, ведь получающие такое лечение продолжают испытывать периодические кровотечения, им необходимы достаточно частые переливания (до трех процедур в неделю), а также неотложная помощь при кровотечениях, возникших в результате травм [1]. Кроме того, у ряда пациентов, особенно с гемофилией А, вырабатываются нейтрализующие антитела к фактору свертывания, что делает инъекции неэффективными. Еще одна проблема — терапия факторами свертывания очень дорогая, ее стоимость составляет несколько сот тысяч долларов в год, а инъекции нужны пожизненно.
Не так давно началась разработка генной терапии для лечения гемофилии, что обещало стать настоящим прорывом, правда, результаты клинических испытаний были не всегда положительными [3]. О первых попытках такого рода и проблемах, с которыми столкнулись исследователи, «Биомолекула» уже писала [3].
Сегодня появление такого лечения стало ближе, и возможно сейчас мы стоим на пороге терапевтической революции.
Генная терапия: на переднем крае науки
Генная терапия словно бы создана специально для пациентов с такими наследственными заболеваниями, как гемофилия. Векторы на основе вирусов, попадая в клетки организма, переносят туда целевой генетический материал — внедренный исследователями ген, кодирующий отсутствующий (или дефектный) при определенной болезни белок. Биосинтез нужного белка в клетках позволяет нивелировать или значительно снизить последствия врожденного (или приобретенного) патологического процесса (видео 1).
Видео 1. Как работает технология переноса генов на базе вектора аденоассоциированного вируса
Сегодня на острие исследований генной терапии находится фармацевтическая компания uniQure — своего рода пионер в этой области: именно ей принадлежит первенство вывода на европейский рынок такого препарата, созданного на базе вектора аденоассоциированного вируса (AAV) . Семейство этих векторов — одно из самых эффективных и безопасных, и они используются ныне во множестве разрабатываемых и применяемых препаратов генной терапии. AAV не патогенны и могут быть сконструированы для внедрения в конкретные типы клеток и тканей, при этом срок их экспрессии может быть весьма длительным (до 10 лет), что делает их уникальными и часто предпочтительными для генной терапии (видео 1) [6].
Речь о препарате Glybera — для лечения дефицита липопротеинлипазы, — одобренном к применению в 2012 году. Это прорывное лечение было эффективным, однако из-за высокой стоимости и ограниченности применения было снято с рынка [4], [9].
Последним прорывом uniQure можно назвать разработку генной терапии гемофилии B — лекарства этранакоген дезапарвовек (АМТ-061) — препарата на базе вектора серотипа AAV5, который, как показали клинические исследования, имеет сниженную иммуногенность и потому более благоприятный профиль безопасности и эффективности в сравнении с другими генными терапиями на основе AAV [8].
Аденоассоциированные вирусы и AAV5, в частности, имеют высокое сродство к клеткам печени, а ведь именно там в норме вырабатываются факторы свертывания крови. Дополнительную специфичность экспрессии белка придает промотор, который активируется именно в печени (рис. 3).
Кроме того, AAV5 в АМТ-061 несет «улучшенную версию» гена фактора свертывания IX с двумя нуклеотидными заменами в последовательности ДНК, приводящими к замене лишь одной аминокислоты в структуре кодируемого им белка. Данная последовательность известна как вариант «Падуя», потому что он был разработан профессором Паоло Симони из университета Падуи. Эта мутантная версия обладает в 8–9 раз большей активностью в сравнении с «нативным» (дикого типа) фактором свертывания IX (рис. 3) [9], [10].
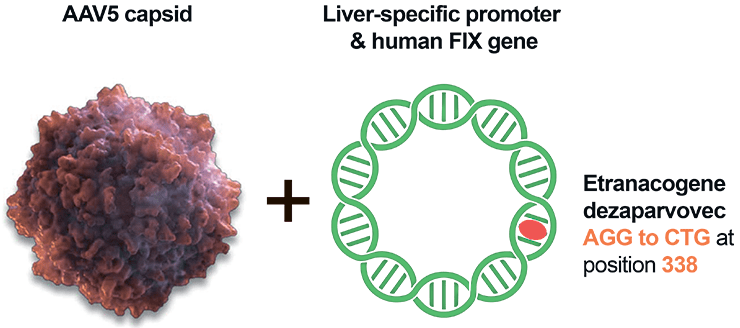
Рисунок 3. Вариант «Падуя»: замена двух нуклеотидов в последовательности кодирующего гена — аденина на цитозин и гуанина на тимидин — приводит к замене аргинина на лейцин в позиции 338 тяжелой цепи фактора IX. Такая мутация приводит к усилению специфической активности фактора свертывания в 8–9 раз в сравнении с «обычным» фактором IX. Кстати, генная последовательность «обычного» фактора IX (дикого типа) используется в генной терапии предыдущего поколения от uniQure — AMT-060, о которой ниже.
Данные исследований
8 декабря 2019 года uniQure представила обновленные данные продолжающегося открытого исследования фазы IIb , в котором три пациента с тяжелой гемофилией B и критически низкой активностью фактора IX (≤ 1%) получили однократную внутривенную инфузию АМТ-061. Согласно этим данным, по прошествии года средний уровень активности фактора IX у трех пациентов составил 41% от нормы, причем максимальная наблюдаемая активность у одного из пациентов дошла даже до 50% [11]. Это довольно впечатляющие цифры, особенно учитывая, что считающийся достаточным для устранения или значительного уменьшения риска кровотечений терапевтический порог составляет лишь 12% (рис. 6) [12].
О том, как проводят клинические исследования и из каких фаз они состоят, читайте наш спецпроект «Клинические исследования». — Ред.

Рисунок 6. Активность фактора IX в плазме пациентов в процентах от нормы (измерена по активированному частичному тромбопластиновому времени, aPTT)
При этом никто из пациентов не сообщил о каких-либо кровотечениях, и лишь одному потребовалась однократная инфузия фактора IX, что было необходимо в связи с операцией на тазобедренном суставе и со спонтанным кровотечением связано не было.
Приличным оказался и профиль иммуногенности, ведь у всех трех пациентов были антитела к AAV5, а двое ранее даже исключались из исследований генной терапии из-за наличия нейтрализующих антител к другому вектору AAV, но, несмотря на это, никому из них не потребовалась иммуносупрессия во время терапии АМТ-061.
Прогнозы
Клинические испытания демонстрируют высокий уровень эффективности и безопасности АМТ-061, что выглядит особо многообещающим, если учесть, что продолжающиеся испытания предыдущего кандидата (АМТ-060 ) также показывают замечательные данные, на основании которых можно прогнозировать и эффективность АМТ-061.
АМТ-060 — генная терапия первого поколения от uniQure, состоящая из вектора AAV5, несущего ген фактора IX дикого типа. В сравнении с АМТ-061 она менее эффективна: по данным исследований, средняя активность фактора IX за 3,5 года с начала применения АМТ-060 составила 7,5%.
Эти данные показывают, что пять пациентов не нуждаются в плановой заместительной терапии фактором свертывания IX даже спустя 3,5 года после начала лечения AMT-060. В uniQure полагают, что данные испытаний AMT-060 будут частью доказательств эффективности для одобрения к применению и этранакогена дезапарвовека, а демонстрируемые длительные лечебные преимущества АМТ-061 могут позволить этому лекарству стать первой и лучшей в своем классе генной терапией гемофилии В [11].
У читателя может возникнуть вопрос, почему генная терапия была в первую очередь разработана для гемофилии В, хотя гемофилия А — более распространенное заболевание? Этому есть простое объяснение: ген фактора VIII гораздо больше гена фактора IX (186 000 пар оснований по сравнению с 34 000 парами [13]), поэтому его нельзя целиком поместить в AAV-вектор, который обладает ограниченной емкостью. Однако разрабатывается генная терапия с укороченным вариантом фактора VIII [14], который, тем не менее, должен обеспечивать достаточную функциональность. Другой подход — попытки увеличить капсид вируса, чтобы в него помещалась ДНК большего размера [15].
Заключение
Несмотря на то, что этранакоген дезапарвовек пока испытывался лишь на нескольких пациентах, полученные в этих исследованиях данные уже выглядят крайне интригующе. Ведь гемофилию по сей день лечат только симптоматически, а АМТ-061, судя по всему, способен стать почти панацеей, ведь даже его менее эффективный предшественник позволил исключить заместительную терапию в течение нескольких лет. Такая многообещающая эффективность, скорее всего, позволит препарату быть и финансово рентабельным: эксперты уже прогнозируют объем продаж в 2024 году в размере $744 млн. Компания пока, конечно, не сообщает возможную стоимость своего препарата, но эксперты считают, что он может претендовать на цену в $1 млн, так как одна инъекция потенциально заменит много лет дорогостоящей заместительной терапии.
Удивительно, что решение проблемы под названием «гемофилия» может быть столь элегантно простым и, главное, совсем близким.
Литература
- Rodríguez Fernández C. (2018). How is biotech innovating to treat hemophilia? Let’s review. Labiotech;
- Как работает свертывание крови?;
- Сводка с генотерапевтических фронтов. Новая стратегия нейтрализации гемофилии;
- Три поколения лекарств;
- Hemophilia: from plasma to recombinant factors. (2008). American Society of Hematology;
- Mitha F. (2019). The return of gene therapy. Labiotech;
- Warner E. (2017). Goodbye Glybera! The world’s first gene therapy will be withdrawn. Labiotech;
- uniQure technology. uniQure;
- Rodríguez Fernández C. (2017). Dutch biotech plans pivotal clinical trial with first gene therapy for hemophilia. Labiotech;
- Elisabeth A. Spronck, Ying Poi Liu, Jacek Lubelski, Erich Ehlert, Sander Gielen, et. al.. (2019). Enhanced Factor IX Activity following Administration of AAV5-R338L “Padua” Factor IX versus AAV5 WT Human Factor IX in NHPs. Molecular Therapy - Methods & Clinical Development. 15, 221-231;
- uniQure announces one-year follow-up data from the phase IIb study of etranacogene dezaparvovec and long-term follow-up data for AMT-060 in patients with hemophilia B. (2019). GlobeNewswire;
- Дмитриев Р. (2019). uniQure: успехи генной терапии тяжелой гемофилии B. «Мосмедпрепараты»;
- Kitchens C.S., Kessler C.M., Konkle B.A. Consultative hemostasis and thrombosis. Elsevier, 2013;
- Paul Batty, David Lillicrap. (2019). Advances and challenges for hemophilia gene therapy. Human Molecular Genetics. 28, R95-R101;
- BIOCAD: взгляд изнутри.







