
Сколько можно съесть мышиного яду? Очерк о витамине D
07 сентября 2018
Сколько можно съесть мышиного яду? Очерк о витамине D
- 6708
- 7
- 5
Даже самые простые вопросы из учебника биохимии, которые кажутся давно исследованными, могут удивить, если покопаться в них с точки зрения эволюции живых существ.
иллюстрация Алены Беляковой
-
Автор
-
Редакторы
-
Иллюстратор
Этот рассказ начался с судебного разбирательства, где мне пришлось участвовать в роли эксперта в патентном споре. В чем было дело, я сказать не могу, да это и не важно. Главное для нас, что один из юристов спросил меня, дескать, раз между мышью и человеком такие биохимические отличия, как вы утверждаете, могли бы вы принять яд для грызунов? Полемику в стиле судебных саг из американских сериалов судья ему провести не дала, и вопрос повис в казенной атмосфере зала. Но, как ни странно, ответ у меня был.
Иногда можно кушать чернильницы.
Михаил Зощенко
Сейчас в продаже находится яд для грызунов, то есть, родентицид, летальная доза которого в пересчете на массу тела сильно различается у грызунов и людей. Точнее, такой параметр, как полулетальная доза (LD50 — доза, убивающая примерно половину испытуемых), у мыши составляет примерно 44 мг/кг массы тела, у собаки — вдвое больше, а у человека — вообще около 200 мг/кг веса [1]. Это вещество — не что иное, как холекальциферол.

Рисунок 1. Рыбий жир и выпивающий его ребенок, который не выглядит счастливым
Знаменитый витамин D3, который дают детям, «чтоб не было рахита» — верный спутник детства, препарат, который у всех на устах. Рыбий жир, содержащий этот витамин, давали советским детям в садах и школах до конца 1960-х годов, о чем с ужасом рассказывала моя мама (рис. 1). Сегодня этот малоприятный на запах и вкус продукт заменен лекарствами в разных формах, которые широко используются, в особенности, в близких к полюсам странах с дефицитом солнечного света.
Биохимия витамина D хорошо известна и входит во все профильные учебники (рис. 2). Если рассказывать кратко, то образующийся в каскаде синтеза холестерина 7-дегидрохолестерол под воздействием ультрафиолетового излучения (например, в коже у человека) преобразуется в провитамин D3, из которого спонтанно, без участия ферментов, получается тот самый холекальциферол. Для проявления клеточной активности этому метаболиту предстоит еще два преобразования — монооксигеназные, то есть встраивающие в углеводородный остов один атом кислорода, реакции. Их производят в печени и почках изоформы цитохромов P450 — представители огромного надсемейства содержащих гем ферментов, среди прочего, метаболизирующие большинство лекарств и прочих чужеродных органических соединений, попадающих в организм.
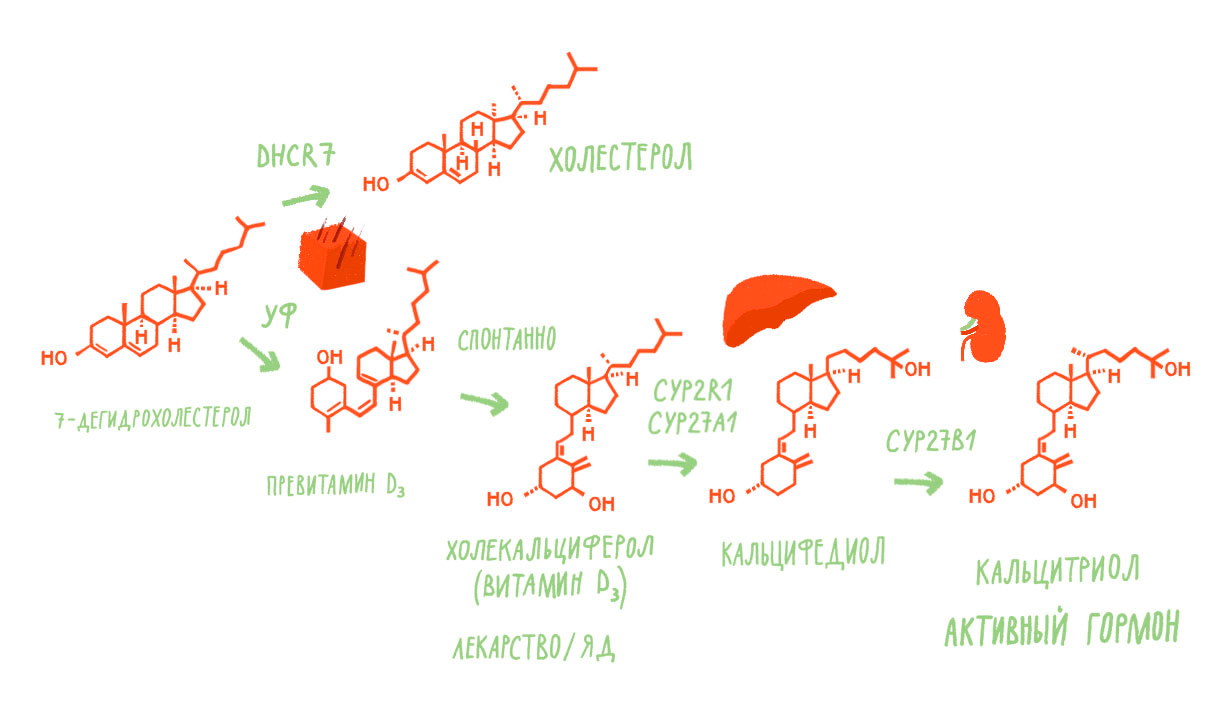
Рисунок 2. Каскад кальциферолов в организме человека
иллюстрация Алены Беляковой
Активный витамин D — кальцитриол — без труда проникает через мембраны клеток в ядро, где взаимодействует со своим рецептором. Образовавшийся комплекс способен выступать в роли транскрипционного фактора, обеспечивающего при связывании со своим «мотивом» в ДНК экспрессию ряда генов. Молекулярная биология витамина D хорошо описана в учебниках, и здесь мы не будем на ней останавливаться.
Лучше вернемся к ключевому этапу синтеза холекальциферола — воздействию на молекулу предшественника ультрафиолетового излучения. Именно недостаток солнечного света (например, при жизни в высоких широтах) рассматривают как основную причину детского авитаминоза — рахита, наиболее характерное проявление которого — нарушение образования костной ткани.
Участие ультрафиолета в метаболическом каскаде — уникальный этап, который оказался эволюционно древним. Например, он известен у большинства групп позвоночных. Вы скажете: «Но кошечки и собачки покрыты густой шерстью, а птички перьями. Как же у них происходит зависимая от солнечного света реакция?» Оказывается, 7-дегидрохолестерол у них выделяется различными кожными железами и облучается светом, находясь на шерсти или перьях. Затем они слизывают готовый провитамин, когда приводят себя в порядок. Но существуют млекопитающие, в силу своего образа жизни очень редко облучающиеся солнечным светом: днем они прячутся в укрытиях, из которых выходят только ночью. Более того, некоторые животные, например, голый землекоп, большую часть жизни проводят в полной темноте.
Как же землекоп решает проблему витамина D? Почти никак. В ходе эволюции он, несмотря на наличие рецепторов к нему, научился обходиться малыми концентрациями активного витамина. Иными словами, известные аномальным долгожительством землекопы [2] дефицитны по витамину D. Обратите внимание, что ключевые биохимические каскады могут функционировать по-разному у достаточно эволюционно близких животных, какими являемся мы и землекопы [3]. Это заставляет задуматься, можно ли проецировать механизмы долгожительства этого грызуна на молекулярную организацию человеческого организма.
Отметим по справедливости, что даже у землекопа каскад кальциферолов работает. В отсутствие ультрафиолета часть готового витамина животные получают из пищи. Домовые мыши, например, в диком виде тоже незначительно контактируют с солнечным светом. Тем не менее при дефиците витамина D, в том числе создаваемого искусственно путем мутации генов его метаболизма, у мышат развиваются симптомы, сходные с человеческим авитаминозом. Отличие заключается в том, что взрослые и старые мыши, в отличие от людей, похоже, прекрасно переносят дефицит витамина D [4].
А теперь вернемся к пламенной речи патентного юриста, с которой я начал свой рассказ. Итак, несмотря на то, что мышка использует каскад кальциферолов и ядерные рецепторы к их активной форме примерно так же, как мы с вами, концентрация этих витаминов в ее органах и тканях несколько меньше, чем у человека. Также, как говорилось вначале, у нее сильно отличается и токсичная доза холекальциферола в пересчете на площадь поверхности тела.
А вообще, почему витамин должен быть токсичным? Дело в том, что у жирорастворимых витаминов вообще довольно низкий порог гипервитаминоза, как и у любых проникающих через клеточные мембраны соединений. Последние, попав в клетку, обычно очень медленно выводятся в силу принципов работы выделительной системы, имеющей дело с гидрофильными веществами.
Изобретательный ум предложил воспользоваться различиями в активных и минимальных токсических концентрациях витамина D для разработки безопасного родентицида. Действительно, случайно приняв смертельную для грызунов дозу холекальциферола, ребенок или собака не умрут и, вероятно, даже не почувствуют недомогания.
Если, предположим, я съем 1 г мышиного яда с холекальциферолом, там будет 75 мг этого вещества. При одноразовом приеме такого количества витамина возможны небольшие, скоро исчезающие признаки интоксикации. При расчетной массе тела мыши в 19 г и летальной дозе для 50% животных (LD50) около 44 мг/кг по грубой оценке этой дозы хватит, чтобы убить примерно 40 мышей.
Еще несколько скучных цифр: с 50-процентной вероятностью человека массой 75 кг убьет 1500 мг холекальциферола. Этого хватит, чтобы с такой же вероятностью погубить двух небольших собак массой по 8,5 кг и целых 1810 мышей массой по 19 г (рис. 3) [1]! Вот почему в разумных количествах можно кушать мышиный яд ! И вот почему исследование, проведенное на мышах, хорошо бы повторить в клинике !
Но только тот, который в качестве активного вещества содержит один холекальциферол. На рынке много других ядов, более опасных для человека и домашних питомцев.
Я уверен, что читатель это отлично осознает, но это не понимал, точнее, делал вид, что не понимал, тот пресловутый юрист.
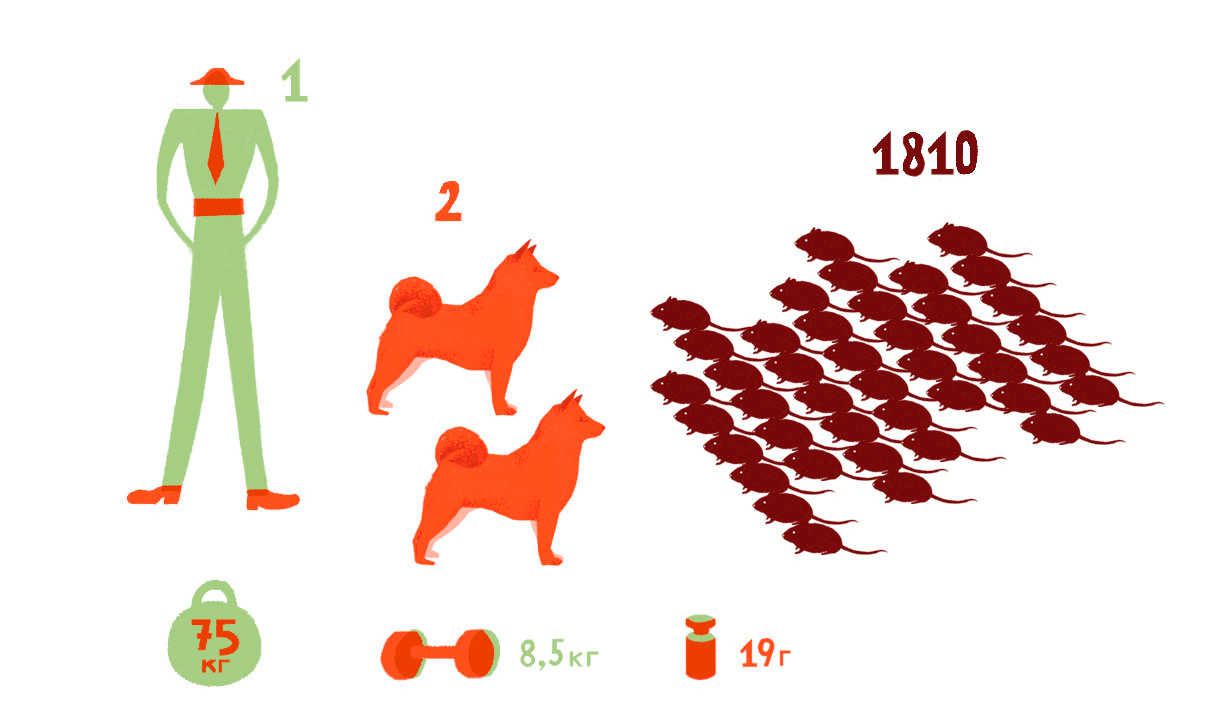
Рисунок 3. Сколько млекопитающих с 50-процентной вероятностью убьют полтора грамма витамина D3
иллюстрация Алены Беляковой
Завершу лирическим отступлением. «В далекой знойной Аргентине» местному населению была давно известна болезнь скота, которая, в том числе, сопровождалась избыточным окостенением суставов, что нарушало подвижность животных. В середине 20 века биохимики раскрыли механизм этого явления. Оказалось, болезнь возникала за счет передозировки аналогами кальцитриолов, которые естественным образом содержались в растении паслене восколистном (Solanum malacoxylon или Solanum glaucophyllum). Это растение — родственник картофеля и томата — встречается в предгорьях Анд в Аргентине и других странах региона. Хроническое потребление травы паслена приводит к передозировке аналога витамина D у копытных [5].
К удивлению исследователей , аналоги кальцитриола обнаружились и в других растениях, в частности, в злаке трищетиннике желтоватом (Trisetum flavescens) и даже в обычнейшем луговом растении Средней России — еже сборной (Daclylis glomerata) [6].
Возможно, те, кто хорошо знакомы с биохимией растений, не удивились: эти парни способны на сложный синтез самого изощренного аналога или ингибитора известных у животных молекулярных каскадов. Именно средства растительного происхождения заложили основу вначале эмпирической, а затем и доказательной фармакологии.
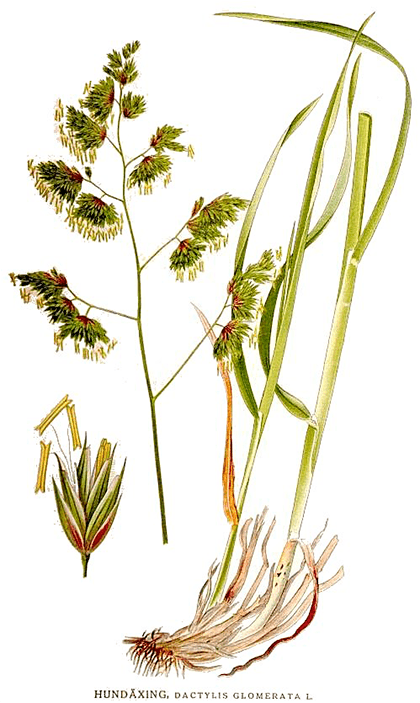
Рисунок 4. Ежа сборная. Автор рисунка: Карл Аксель Магнус Линдман. Bilder ur Nordens Flora, Stockholm, общественное достояние.
Что делают кальцитриолы в растениях, пока не понятно. Интересно, что последние, по имеющимся данным, освоили синтез аналогов витамина D без участия ультрафиолета, что, как я указывал вначале, недоступно животным [7].
Так что хорошо запомните ежу сборную (рис. 4). Если человечество все же доведет мир до первобытного состояния отключения электричества и гибели цивилизации в современном виде, мы, вероятно, можем давать младенцам вместо препарата холекальциферола экстракт этого обыкновенного растения, чтобы предотвратить рахит .
Не нужно прибегать к этому средству сегодня, поскольку на полках аптек находятся прошедшие клинические испытания препараты витамина D. Способы получения из частей ежи сборной таких препаратов пока не разработаны.
Литература
- McDowell L.R. Vitamins in animal and human nutrition. Iowa State University Press, 2000. — 793 p.;
- Преодолевшие старение. Часть II. Дети подземелья;
- Nicole M. Foley, Mark S. Springer, Emma C. Teeling. (2016). Mammal madness: is the mammal tree of life not yet resolved?. Phil. Trans. R. Soc. B. 371, 20150140;
- Sanjay M. Mallya, Kristin R. Corrado, Elizabeth A. Saria, Feng-ning Frank Yuan, Huy Q. Tran, et. al.. (2016). Modeling vitamin D insufficiency and moderate deficiency in adult mice via dietary cholecalciferol restriction. Endocrine Research. 41, 290-299;
- Boland R.L. (1988). Solanum malacoxylon: a toxic plant which affects animal calcium metabolism. Biomed. Environ. Sci. 1, 414–423;
- Raoul Y., Le Buolch N., Gounelle J.C., Marnay-Gulat C., Ourisson G. (1970). Substances antirachitiques des végétaux. Présence du cholécalciférol. Bull. Soc. Chim. Biol. 52, 641–657;
- Lucinda Black, Robyn Lucas, Jill Sherriff, Lars Björn, Janet Bornman. (2017). In Pursuit of Vitamin D in Plants. Nutrients. 9, 136.






